
Тимур Казанцев
Биохакинг на доступном
Связь размера тела и продолжительности жизни
Причем, здесь хотелось бы обратить внимание на 2 факта.
1. Периодически можно встретить такое мнение, что продолжительность жизни сильно коррелирует с размерами тела организма. Однако, это не так. Слоны, например, вес которых несколько тонн, живут 40–70 лет, в то время как упомянутые нами моллюски или саламандры весом 100 грамм живут более 100 лет.
Более того, по мере роста организма, размер долгоживущего животного может даже сыграть с ними в злую шутку и привести к смерти. Например, по мере увеличения возраста и массы некоторых акул или морских окуней, их скорость передвижения и маневренности снижается, им тяжелее догнать добычу и они попросту умирают от голода, а не от старости и возраста или каких-либо болезней.

3. Второй факт заключается в том, что даже внутри одного и того же вида могут быть подвиды, продолжительность которых сильно отличается друг от друга. Например, если взять разные подвиды морских ежей, то их продолжительность отличается на порядки:
Морские ежи:
– Lytechinus variegatus – 4 года
– Echinometra lucunter – 40 лет
– Strongylocentrotus franciscanus – 100–200 лет
Другой уже упомянутый нами пример – голые землекопы, которые могут доживать до 30 лет и более без видимых признаков старения организма, в то время как их ближайшие родственники – мыши, крысы и грызуны такого же размера – живут в среднем только 2–3 года.
Эти модели очень интересно исследовать – почему такие близкие родственники так сильно отличаются по продолжительности жизни? Какие механизмы внутри клеток позволяют существовать так долго?
Более подробно о связи между размером тела, скорости обмена веществ и продолжительности жизни, в моем посте: https://vc.ru/s/1830105-biohaking-na-dostupnom/899832-razmer-imeet-znachenie-paradoksnye-vyvody-o-razmere-skorosti-obmena-veshchestv-i-prodolzhitelnosti-zhizni
* * *
Ну как? Изменилось у вас отношение к старению после знакомства с этими видами, которые «плевать хотели» на смерть от старости и заболеваний?) Если некоторые виды живых организмов могут доказанно жить сотнями лет (причем у многих из них не обнаруживалось признаков износа организма, или существенных повреждений тканей, органов, клеток, окислительных повреждений), то получается можно считать, что никаких запретов на воспроизводство и существование клеток и организма в целом на протяжении долгих периодов не существует.
Именно в результате исследования этих «бессмертных видов» ученые стали подвергать сомнению упомянутые нами классические теории старения, обусловленные поломками и износом организма в результате возраста. Если есть организмы, которые могут жить и несколько сотен лет без поломок и признаков старения, то может быть ключевой фактор в продолжительности жизни или старении в чем-то другом?
Поэтому давайте теперь вернемся к другой большой группе теорий старения.
Теории запрограммированного старения
Данная группа теорий рассматривает старение как стратегию обновления поколений, которая помогает видам эволюционировать и адаптироваться к изменяющимся условиям окружающей среды. В соответствии с этой концепцией, наша первостепенная задача – достичь репродуктивного возраста, затем найти партнера для передачи своих генов следующему поколению.
Как только мы успешно выполнили эту роль, наша ценность для природы снижается. Возможно, мы остаемся полезными некоторое время после рождения детей, прежде всего для того, чтобы помочь им вырасти, стать независимыми для самостоятельной жизни. Но после того, как наш репродуктивный период завершается, мы становимся менее важными для природы.
Это объясняет, почему наш организм работает идеально до возраста примерно 25–35 лет. В этот период у нас отлично функционируют регенеративные процессы, мы быстро восстанавливаемся после большинства заболеваний. Однако после 30 лет эти способности начинают постепенно угасать. И если бы не достижения современной медицины, наша ожидаемая продолжительность жизни так и оставалась бы в районе 35–45 лет[20].
В этом контексте старение и смерть можно рассматривать как способ "очистки" популяции от особей, которые вышли из репродуктивного периода. При таком подходе старение и смерть выглядят не как несчастные случайности, а как важная часть естественного процесса, обеспечивающего плавную смену поколений и продолжение выживаемости вида.
А теперь конкретные инструменты как реализуется эта функция старения с точки зрения представителей теории запрограммированного старения.
И здесь тоже можно поделить теории на 2 подгруппы: первая подгруппа считает, что организм запрограммирован стареть; а вторая подгруппа считает, что мы стареем, потому что есть какой-то механизм, который запрещает нам / не дает нам чинить возникаемые поломки.
Теломерная теория старения
Одной из самых интересных и известных теорий старения является теломерная теория. Изначально ее основные положения выдвинул советский ученый Алексей Оловников в начале 1970-х годов, и только в 2009 году за ее доказанность и более точное определение механизма трем американским ученым была присуждена Нобелевская премия по медицине и физиологии.
В чем состоит суть этой теории?
Теломеры – это концевые участки хромосом, в которые упакованы наши ДНК. Теломеры можно сравнить с пластиковыми наконечниками на обувных шнурках. Если этот пластиковый наконечник на шнурке убрать, то шнурок начнет расплетаться и разлохмачиваться. Примерно то же самое происходит и с хромосами. Каждый раз при делении клеток, длина теломер укорачивается. Теломер хватает примерно на 50 делений клеток, этот предел назвали «пределом Хейфлика» в честь американского ученого Л. Хейфлика, который в 1960-х гг. обнаружил этот факт, что человеческие клетки могут делиться только ограниченное количество раз, и таким образом продолжительность их жизни «запрограммирована».
Когда теломеры укорачиваются настолько, что наступает предел Хейфлика, хромосомы начинают слипаться, ломаться, становятся более ломкими, клетки уже не могут делиться, и тогда они теряют жизнеспособность. И согласно теломерной теории, именно это и является причиной старения.
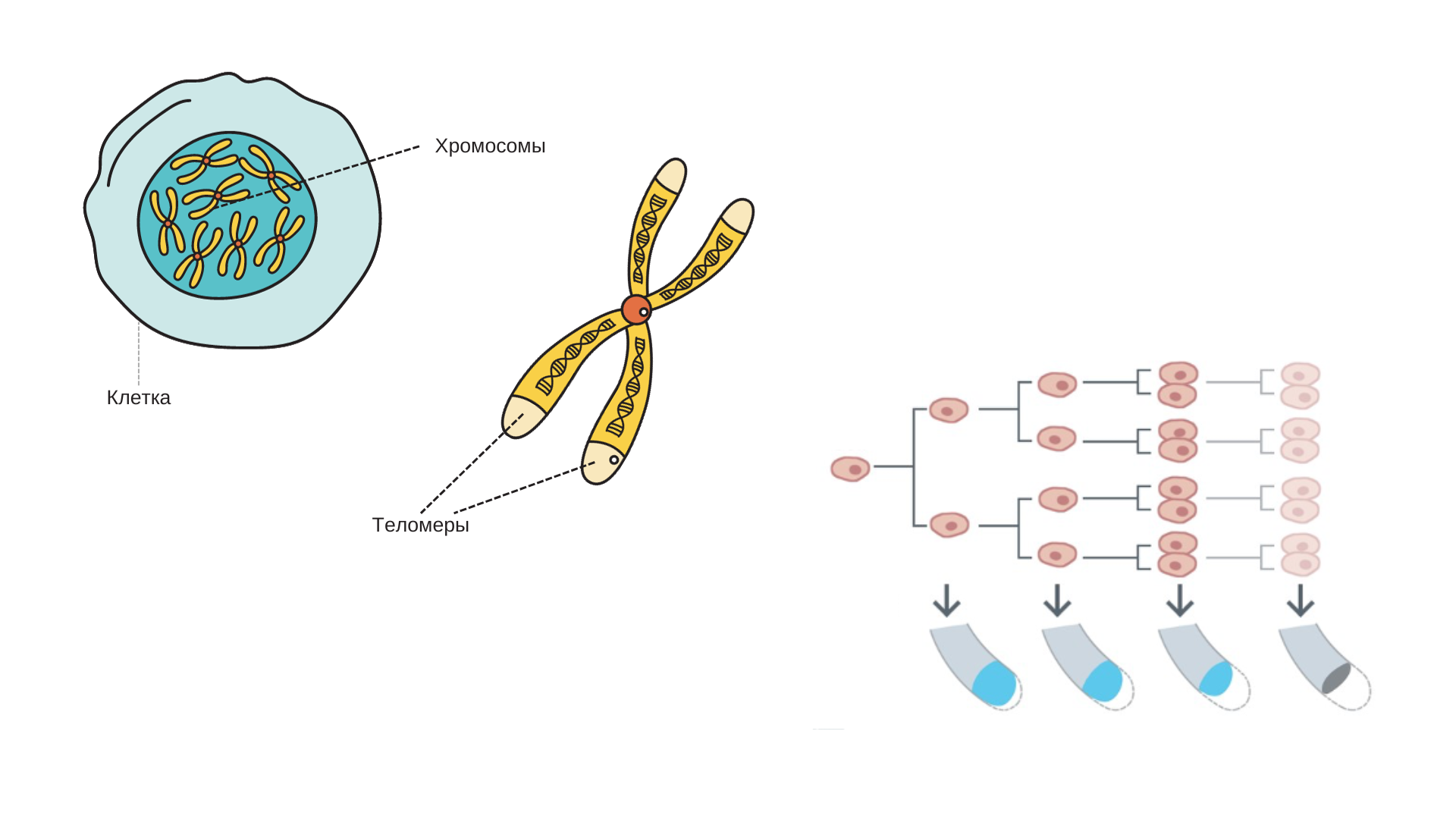
В целом теломерная теория звучит достаточно логично. Однако, некоторые факты сильно подшатывают ее возможность на то, чтобы быть ведущей теорией старения.
Во-первых, в наших клетках присутствует также фермент теломераза, который может достраивать укороченные концы хромосом – теломеры. Именно за его открытие и была присуждена Нобелевская премия в 2009 году. В большинстве клеток теломераза имеет низкую активность, а ее принужденная активация медицинскими способами может приводить к повышению риска рака. Поэтому, не все так однозначно.
Во-вторых, предел в 50 делений действует не для всех видов клеток (примерно только для 1/8 от всего количества клеток). Некоторые клетки (стволовые или раковые) могут делиться бесчисленное количество раз. А большинство клеток человека вообще постмитотические – т. е. они вышли из клеточного цикла и больше не обновляются или редко делятся после того, как они сформировались во время развития[21]. Постмитотические являются самые важные для организма клетки: например, нейроны не делятся совсем – они с нами с самого рождения. Кардиомиоциты – клетки сердечной мышцы также практически не делятся после возраста примерно в 15–20 лет. Если бы клетки сердца делились и регенерировались, то было бы прекрасно и у нас не было бы инфаркта миокарда.
Постмитотическими являются и клетки большинства желез. Например, тимус (центральный орган иммунной системы) не делится, и что бы мы ни делали с теломеразой, он будет только уменьшатся с возрастом.
Кроме всего этого, скорость укорочения теломер также может существенно различаться у людей одного и того же возраста, что указывает на важность других факторов, включая генетику и образ жизни, которые могут влиять на старение. Если сравнивать разные виды организмов между собой, то некоторые виды животных с высокой продолжительностью жизни могут иметь эквивалентную или даже меньшую длину теломер по сравнению с человеком. Такое расхождение позволяет предположить, что длина теломер не является единственным фактором, определяющим продолжительность жизни.
Поэтому теломерная теория достаточно интересна, она объясняет, почему некоторые клетки делятся ограниченное количество раз. Но эта теория сама по себе не может полностью объяснить такой сложный процесс старения, потому что управление теломеразой (для продления теломер делящихся клеток) может обернуться риском развития рака, а для большинства остальных клеток этот механизм вообще не играет никакой роли, потому что они не делятся или делятся очень редко.
https://www.youtube.com/watch?v=qcj0D-bkCPM – биолог о теломерной теории (видео, 5 мин)
https://ria.ru/20230819/telomery-1890440981.html – статья о Элизабет Пэрриш, которая стала «нулевой пациенткой» по удлинению своих собственных теломер
Нейроэндокринная теория старения
Нейроэндокринная теория старения, предложенная Владимиром Дильманом в 1954 году, утверждает, что старение вызвано прогрессирующей потерей чувствительности рецепторов гипоталамуса к гормональному фону организма.
Гипоталамус – часть мозга размером с грецкий орех, управляющая выработкой гормонов другими органами и железами. Дильман полагал, что прогрессирующая с возрастом потеря чувствительности гипоталамуса ведет к нарушению гомеостатического баланса и способности к точной регуляции, что приводит к уменьшению производства многих гормонов, вызывая болезни старения (диабет, ожирение, гипертония, климакс, атеросклероз, и т. д.).
Теория апоптоза
Эта концепция, также известная как принцип клеточного самоуничтожения, принадлежит известному академику В.П. Скулачеву. В соответствии с данной теорией, каждая клетка проходит через определенный (запрограммированный) жизненный путь, после чего умирает, освобождая пространство для новых клеток.
После того как клетка умирает, она "саморазлагается", и ее компоненты используются соседними клетками в качестве строительных блоков. Этот процесс также происходит с митохондриями, когда в них накапливается избыток свободных радикалов. Когда число умерших митохондрий становится слишком великим, продукты их распада вызывают апоптоз, то есть самоуничтожение.
В молодом возрасте количество умирающих клеток примерно равно количеству новообразующихся клеток, поэтому они просто заменяются (например, кожные клетки). Однако с течением времени число саморазрушающихся клеток становится больше, чем новых. Ткань и органы полностью не успевают восстановиться, они теряют свою функциональность, и частично начинают замещаться соединительной тканью (отсюда, в частности, фиброз легких и другие заболевания).
Иммунологическая теория старения
Данная теория предполагает, что постепенное снижение функции иммунной системы с возрастом является значительным фактором процесса старения. Эта теория основывается на наблюдении, что иммунный ответ у пожилых людей обычно слабее, чем у молодых, что приводит к увеличенной подверженности болезням и инфекциям.
Иммунная система – это сложная сеть клеток, тканей и органов, которые работают вместе, чтобы защитить организм от вредных вторженцев, таких как бактерии, вирусы и другие патогены. Однако с возрастом способность иммунной системы реагировать на эти угрозы уменьшается. Это связано с уменьшением числа иммунных клеток, снижением их способности эффективно общаться, а также общим ухудшением способности иммунной системы распознавать и устранять чужеродные вещества.
В результате пожилые люди становятся более подверженными инфекциям, раку, автоиммунным заболеваниям и другим проблемам со здоровьем. Кроме того, ослабленный иммунный ответ также влияет на способность организма восстанавливать поврежденные ткани, что ускоряет процесс старения.
Теория иммунного старения также предполагает, что хроническое воспаление, часто связанное со старением, является другим ключевым фактором в прогрессии возрастных заболеваний. Это постоянное слабое воспаление, известное как "инфламмэйджинг", считается фактором, который способствует развитию сердечно-сосудистых заболеваний, диабета, болезни Альцгеймера и других возрастных состояний.
Теория квази-запрограммированного старения (mTOR и IGF-1)
Согласно данной теории, выдвинутой профессором Михаилом Благосклонным, старение не является непосредственно запрограммированным в генетическом коде организма, но становится неизбежным побочным эффектом других генетических программ, задействованных в развитии и функционировании организма. Это возможно из-за того, что многие гены и механизмы, которые обеспечивают выживание и развитие в молодом возрасте, могут оказывать отрицательное влияние на организм в старости.
Одним из ключевых элементов этой теории является роль сигнального пути mTOR (мишень рапамицина млекопитающих). mTOR – это белок, играющий важную роль в регуляции роста и развития клеток. Он контролирует белковый синтез, обмен веществ и иммунный ответ, что делает его критически важным для эволюции и выживания организма в молодом возрасте.
mTOR важен для роста организма, но когда активность mTOR высока (например, когда в клетке много питательных веществ), аутофагия (переваривание пришедших в негодность белков и органелл) подавляется. А когда активность mTOR низкая (например, при голодании), аутофагия стимулируется. Таким образом, избыточная активность mTOR не дает очищаться клеткам и организму, поврежденные клетки и белки продолжают накапливаться, что может приводить к ускоренному старению и развитию возрастных заболеваний, таких как рак, диабет и болезнь Альцгеймера. Именно поэтому была найдена зависимость между блокировкой mTOR и увеличением продолжительности жизни[22]. Блокировка или подавление mTOR и включение процессов аутофагии достигается, в частности, путем голодания или его медикаментозными аналогами.
Другим виновником, согласно данной теории, является как ни странно, гормон роста (или пептид IGF-1, при содействии которого реализуется действие гормона роста в тканях). Было замечено, что люди, больные синдромом Ларона и имеющие форму карликовости за счет мутаций в рецепторе гормона роста, намного реже сталкиваются с заболеваниями, связанными со старением (рак и диабет) и доживают до вполне преклонного возраста.
Таким образом, в начале жизни mTOR (наряду с гормоном роста и инсулином) нам помогает, так как направлен на рост и развитие организма. Однако, когда мы вырастаем, этот сигнальный путь не выключается. И то, что помогало нам расти и выживать вначале, способствует ускорению старения в конце. Поэтому механизмы, ингибирующие (подавляющие) mTOR, а именно рапамицин или периодическое голодание, рассматриваются как одно из средств против старения, которые запускают в том числе и процессы аутофагии (клеточного очищения).
Если суммировать, основной смысл данной теории в том, что «старение – это на самом деле программа молодости, которую никто вовремя не отключил».
Более полное объяснение этой теории: https://nauka.tass.ru/sci/6820089
Обязательно почитайте, крайне интересно и заставляет задуматься.
Кстати, данная теория коррелирует с таким понятием как «антагонистический плейотропизм», концепт, который предполагает, что cтарение вызывается плейотропными (участвующих во многих процессах) генами, функции которых на ранних этапах жизни благоприятствуют приспособленности организма, в то время как на поздних эта функция пагубно сказывается на его приспособленности. Более подробно об антагонистическом плейотропизме можно почитать на моем канале[23]:
Эпигенетическая теория старения
Эпигенетическая теория старения – одно из наиболее перспективных направлений в современной генетике и биологии старения. Суть этой теории заключается в том, что процессы старения организма могут быть связаны не столько с изменениями в самом ДНК, сколько с модификациями, которые происходят вокруг него – эпигенетическими маркерами.
Эпигенетика – это наука, изучающая изменения в активности генов, которые связаны с изменениями метильного профиля нашего ДНК. Метильные группы, расположенные на цепочке ДНК, могут включать или выключать гены, которые производят нужные белки, из-за чего могут происходить те или иные изменения в функционировании нашего организма. Изменения метильного профиля могут быть вызваны различными факторами, включая возраст, образ жизни и окружающую среду.
Одним из ключевых моментов в эпигенетической теории старения является концепция "эпигенетического часов". Это метафора, которая описывает то, как эпигенетические изменения, происходящие в течение жизни организма, могут служить маркерами его возраста. Согласно этой теории, с течением времени эпигенетические маркеры могут накапливаться, вызывая изменения в работе генов и приводя к различным проявлениям старения. Это может включать в себя потерю эластичности кожи, снижение функции органов и систем, увеличение риска развития хронических заболеваний и т. д.
Однако, что особенно интересно в эпигенетической теории старения, так это то, что эти процессы потенциально обратимы. Исследования показывают, что изменение образа жизни, диеты или воздействие определенных веществ могут "сбросить" эпигенетические часы и вернуть клетки к более молодому состоянию.
Таким образом, эпигенетическая теория старения открывает новые перспективы для разработки методов предотвращения и лечения старения. Она предлагает возможность не просто замедлить процесс старения, но и в некоторой степени обратить его, что делает эту теорию особенно привлекательной для исследователей.
Более подробно о генетике и эпигенетике, о том, что такое эпигенетические маркеры и как можно теоретически обратить вспять эпигенетический возраст мы поговорим уже совсем скоро. А пока нельзя не упомянуть еще об одной интересной теории, которую нельзя причислить к чисто первой (классические теории износа) или второй (теории запрограммированного старения) группе теорий старения, потому что она фокусируется больше не на конкретных механизмах, а больше на фундаментальных и эволюционных причинах старения организмов.
Теория одноразовой сомы
Теория одноразовой сомы предполагает, что организм распределяет свои ресурсы между поддержанием и ремонтом своей сомы (тела), с одной стороны, и развитием и повышением репродуктивных способностей, с другой. Это происходит из-за ограниченности ресурсов и необходимости некоего компромисса в деле нахождения оптимального способа их использования.
В соответствии с теорией одноразовой сомы, виды и популяции, имеющие мало внешних угроз и низкую скорость размножения, должны намного больше инвестировать в свою защиту и ремонт своего организма (и как следствие их продолжительность жизни будет выше), нежели виды с короткой продолжительностью жизни и быстрым размножением.
Большинство исследований подтверждают эту теорию, показывая, что количество и активность хищников влияют на стратегию выживания популяции. Некоторые виды животных, такие как киты и акулы, смогли адаптироваться к условиям окружающей среды, став настолько крупными, что их размер отпугивает потенциальных хищников. Другие виды, например летучие мыши, приспособились к ночной активности и укрытию в пещерах. Эти особенности позволили им обеспечить себе продолжительность жизни, не омраченную постоянной тревогой о возможном нападении.
Исследования гуппи показывают, что продолжительность их жизни эволюционирует в ответ на изменения в смертности. Гуппи, живущие в условиях высокой смертности, меньше по размеру, растут быстрее, размножаются раньше и тратят больше ресурсов на размножение, чем те, кто живет в условиях низкой смертности.
Такое же предположение можно выдвинуть в отношении птиц и летучих мышей. За счет возможности летать и жить на деревьях или в скалах, у них уменьшается количество внешних угроз, и поэтому их продолжительность жизни зачастую выше, чем у наземных животных такого же размера. Обычные наземные мыши же обильно размножаются и достигают половой зрелости в возрасте всего пары месяцев. Они подвергаются нападению со стороны множества хищников, так что им выгоднее отдавать внутренние ресурсы на быстрое размножение, а не на борьбу со старением организма.
Проводились также исследования на двух группах виргинских опоссумов. Одна группа опоссумов, обнаруженная на острове, живет без природных наземных хищников, в то время как другая группа, обитающая на материке, сталкивается с пумами, лисами и рысями. Исследование показало, что островные опоссумы производят меньше потомства, чем материковые, и в большинстве случаев доживают до второго сезона размножения, получая еще один шанс на размножение[24]. При этом островные опоссумы меньше по размеру, их средний срок жизни на 25 % выше, а максимальный – на 50 % больше, чем у материковых.
Человек, как вид, также развил уникальные способы приспособления. Мы создали себе уютные жилища, научились защищаться от природных бедствий, разработали методы добычи и хранения пищи, изобрели способы лечения болезней, которые раньше угрожали нашему выживанию в раннем возрасте.
Создав безопасную среду, человечество смогло снизить давление на выживание до репродуктивного возраста. В свою очередь, это привело к смещению фокуса на продление жизни. В развитых странах мы наблюдаем тенденцию к отложению репродукции: многие люди теперь решают заводить семью и детей ближе к 30 годам, а не в 18. Если эта тенденция сохранится, то можно предположить, что через 20–30 поколений процесс старения будет еще больше отложен, а продолжительность жизни увеличится (хотя, скорее всего, заметную роль в этом все таки сыграют достижения науки и медицины).







