Саида Багавдиновна Ханмурзаева
Рациональная фармакотерапия болезней нервной системы
Снотворные средства
Эпизодические нарушения сна встречаются у 33 % людей в общей популяции, а после 65 лет этот показатель возрастает до 50–65 % [Ohayon M. M. 2002]. Нарушения сна могут быть в виде парасомний: снохождение у 2 % людей, сноговорение у 4 %, ночные страхи у 2 %, бруксизм (скрежет зубами) у 8 %, энурез у 5 %, ночные кошмары (частые у 6 %, время от времени у 29 %). Наиболее часто встречающиеся расстройствами сна – это инсомния (встречается у 9–15 % людей в популяции) и расстройства дыхания во сне (1–4 %) [Сомнология, 2016].
Снотворные средства (от лат. hypnotica; син. гипнотические средства, уст.) – группа психоактивных лекарственных средств, используемых для облегчения наступления сна и обеспечения его достаточной продолжительности, а также при проведении анестезии.
Инсомния (бессонница) характеризуется длительным засыпанием, частыми ночными пробуждениями, длительным бодрствованием в течение ночи, поверхностным сном, ранним утренним пробуждением, несмотря на достаточное время и подходящие условия для сна, что вызывает дневную сонливость, ухудшение памяти и внимания, снижение работоспособности, социальную дисфункцию [Пчелина П. В., 2018].
Таблица 1
Средства, вызывающие бессонницу [Лиманкина И. Н., 2008]
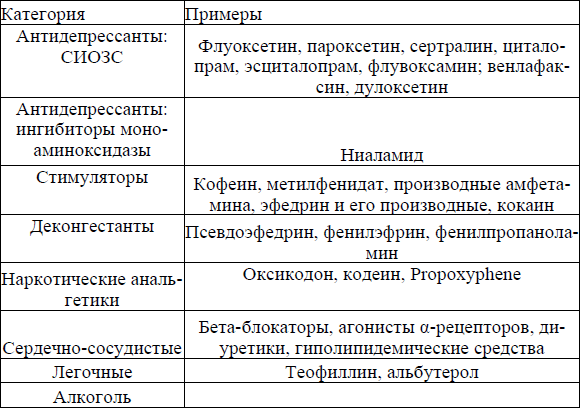
Основными ЛС для терапии инсомнии являются:
Антидепрессанты
Нейролептики
Противоэпилептические средства
При синдроме беспокойных ног рекомендованы: агонисты дофаминовых рецепторов, антиконвульсанты.
Парасомнии (кошмары) при неэффективности психотерапии устраняются седативными средствами.
При расстройствах поведения в быстрой фазе сна (сноговорение, крики и двигательная активность, нередко агрессивная и травмоопасная для самих пациентов и их близких, с последующим пробуждением) требуется назначение клоназепама или мелатонина.
Агонисты бензодиазепиновых рецепторов (АБР) или Ramelteon: золписет, Eszopiclone, залеплон и темазепы.
Седативные антидепрессанты, особенно при использовании в соединении с сопутствующей депрессией/тревогами: тразодон, амитриптилин, доксепин и миртазапины.
Комбинированные АБР или Ramelteon и седативные антидепрессанты.
Другие седативные агенты: антиэпилептические препараты (габапентин, тиагабина) и атипичные антипсихотики (кветиапин и оланзапин).
Антигистаминные средства или наркотики обезболивающего типа, а также растительные и другие вещества (например, валериана и мелатонин) не рекомендуются для лечения хронической бессонницы из-за недостаточной эффективности и безопасности.
Барбитураты, наркотики и хлоралгидрат не рекомендуются для лечения бессонницы.
Краткой/средней продолжительности действия АБР или Ramelteon: залеплон, золписет, Eszopiclone, триазолы и темазепы.
Zaleplon и Ramelteon имеют очень короткий период полураспада и, следовательно, могут уменьшить латентность сна, но мало влияют на пробуждение после начала сна; они также редко приводят к остаточной седации [Sateia MJ, 2017].
Eszopiclone и temazepam имеют более длительный период полураспада, позволяют добиться удлинения сна, и нередко вызывают остаточную седацию. Триазолам не считается первой линией снотворных средств.
Выбор конкретного АБР может включать в себя более длительное снотворное действие, такое как от эстазолов. Flurazepam редко назначают из-за его длительного периода полураспада. Бензодиазепины (например, лоразепам, клоназепам) также могут быть рассмотрены при лечении бессонницы. Тразодон имеет малую антихолинергическую активность по сравнению с доксепином и амитриптилином, и миртазапины связаны с увеличением веса [Sateia MJ, 2017].
Таблица 2
Снотворные средства [Лиманкина И. Н. 2008]
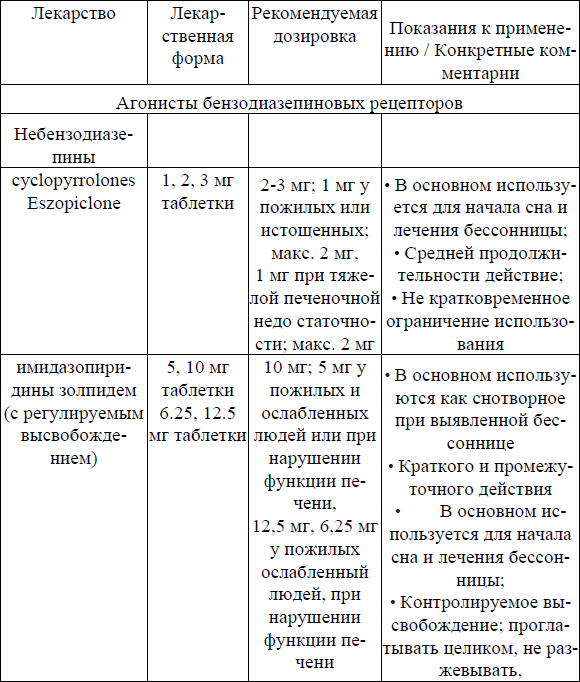

Общие характеристики снотворных средств:
• Прием на пустой желудок рекомендуется, чтобы усиливать эффективность.
• Не рекомендуется во время беременности или кормления грудным молоком.
• Следует проявить осторожность, если имеются симптомы депрессии, угнетение дыхательной функции (например, астма, ХОБЛ, синдром ночного апноэ), печеночная или сердечная недостаточность.
• Рекомендуется уменьшить дозу в пожилом возрасте.
• Безопасность / эффективность у пациентов <18 лет не установлена.
• Обратить внимание на психомоторику при одновременном приеме депрессантов ЦНС и / или употреблении алкоголя.
• Быстрое снижение дозы или резкое прекращение бензодиазепинов может вызвать синдром отмены, в том числе появление бессонницы, подобно тому, что возникает от барбитуратов и алкоголя.
Некоторые антидепрессанты (амитриптилин, доксепин, миртазапины, пароксетины, тразодон) используются в низких антидепрессивных дозах для лечения бессонницы.
Комбинация лекарственных препаратов из двух различных классов могут повысить эффективность путем охвата нескольких механизмов сна и бодрствования при минимизации токсичности, которые могли бы иметь место с более высокими дозами одного агента. Побочные эффекты могут быть сведены к минимуму также при использовании низких доз антидепрессантов.
Достаточно доказательств эффективности габапентина, тиагабина, кветиапина и оланзапина при лечении хронической первичной бессонницы. При их использовании в одиночку увеличивается риск побочных эффектов (например, припадки от тиагабина; дисметаболизм от кветиапина и оланзапина).
Хлоралгидрат, барбитураты, «небарбитураты и небензодиазепины» (мепробамат) не рекомендуются для лечения бессонницы, учитывая их значительные побочные эффекты, низкий терапевтический индекс, и вероятность развития привыкания и зависимости.
Антигистаминные средства и комбинация антигистамина с анальгетиком широко используются как средства от бессонницы. Доказательства их эффективности и безопасности является весьма ограниченными. Антигистаминные средства имеют серьезные побочные эффекты, связанные с их антихолинергическим свойством.
Алкоголь – наиболее распространенное средство от бессонницы при самолечении – не рекомендуется использовать из-за его короткой продолжительности действия, побочных эффектов на сон, обострения обструктивного апноэ во сне, а также возможности при злоупотреблении развития зависимости.
Очень немногие травяные или альтернативные методы лечения, которые были систематически оценены для лечения бессонницы. Из них наибольшее количество доказательств доступно в отношении экстрактов валерианы и мелатонина. Имеющиеся данные свидетельствуют о том, что валериана имеет небольшие, но последовательные эффекты на сон.
Мета-анализ показал, что мелатонин незначительно воздействует на латентность сна. Следует отметить, что некоторые из опубликованных исследований мелатонина оценивали его эффективность в качестве хронобиотического (фазосдвигающего) агента, а не в качестве снотворного.
При прекращении приема снотворного средства после использования в течение нескольких дней могут произойти возврат бессонницы (ухудшение симптомов с уменьшением дозы, как правило, длится 1–3 дня), потенциальные физические, а также психические эффекты отмены. Повторение бессонницы и снятие эффективности могут быть сведены к минимуму путем постепенного снижения как дозы, так и частоты приема. В общем, доза должна быть снижена путем увеличения длительности интервала между приемами, по крайней мере нескольких дней. Снижение частоты введения (например, каждый второй или каждой третьей ночи), чтобы свести к снижению дозы [Sateia MJ, 2017].
В целом, исследования не демонстрируют явное преимущество комбинированной фармакотерапии бессонницы над только когнитивно-поведенческой терапией.
Когнитивно-поведенческая терапия бессонницы представляет собой сочетание когнитивной терапии (психотерапевтический метод) в сочетании с поведенческой терапией (контроль факторов, ограничивающих сон) с или без релаксационной терапии.
Тесты для самоконтроля
Выберите два правильных ответа.
1. НЕДОСТАТКИ СНОТВОРНЫХ СРЕДСТВ ИЗ ГРУППЫ БАРБИТУРАТОВ:
1) нарушают процесс засыпания
*2) вызывают привыкание
3) нефротоксическое действие
*4) вызывают последействия
2. МЕХАНИЗМ СНОТВОРНОГО ДЕЙСТВИЯ БАРБИТУРАТОВ ОБУСЛОВЛЕН:
1) угнетением центральных адренорецепторов
*2) блокадой ГАМКА-рецепторов
3) гиперполяризацией мембран
*4) конформацией мембран нервных клеток и открытием хлорных каналов
3. СНОТВОРНЫЕ СРЕДСТВА:
*1) золпидем
*2) сибазон
3) эуфиллин
4) леводопа
4. ФЕНАЗЕПАМ ПРИМЕНЯЮТ ПРИ:
1) тяжелых поражениях почек
2) миастении
*3) бессоннице
*4) неврозах
5. СНОТВОРНЫЙ ЭФФЕКТ ВЫЗЫВАЮТ:
*1) зопиклон
2) леводопа
*3) феназепам
4) бемегрид
6. ПРОТИВОПОКАЗАНИЯМИ К НАЗНАЧЕНИЮ СНОТВОРНЫХ СРЕДСТВ ЯВЛЯЮТСЯ:
*1) нарушение дыхательной функции
*2) детям школьного возраста
3) эпилепсия
4) артериальная гипотония
7. ПРИ ОТРАВЛЕНИИ СНОТВОРНЫМИ ПОМОГУТ:
1) прокаин
2) пиридостигмин
*3) бемегрид
*4) кофеин в терапевтических дозах
8. СНОТВОРНЫЕ ПРЕПАРАТЫ В ЗАВИСИМОСТИ ОТ ДОЗЫ ОКАЗЫВАЮТ ДЕЙСТВИЕ:
*1) седативное
*2) снотворное
3) нейролептическое
4) анальгезирующее
9. СНОТВОРНЫЙ ЭФФЕКТ ВЫЗЫВАЮТ:
*1) зопиклон
2) леводопа
*3) феназепам
4) бемегрид
10. ПРИ ЛЁГКИХ ОТРАВЛЕНИЯХ СНОТВОРНЫМИ НАЗНАЧАЮТ:
1) кислотные растворы
2) обезболивающие средства
*3) адсорбируцие средства
*4) диуретики
11. ЗОЛПИДЕМ:
*1) снотворный препарат короткой продолжительности действия
*2) улучшает способность к засыпанию
3) применяют при дыхательной недостаточности
4) используют при нарушении функции печени
12. СПОСОБСТВУЮТ ОТКРЫТИЮ ХЛОРНЫХ КАНАЛОВ:
*1) золпидем
2) бемегрид
*3) диазепам
4) амантадин
13. К СНОТВОРНЫМ СРЕДСТВАМ ОТНОСЯТСЯ:
1) тиопентал натрия
2) фентанил
*3) зопиклон
*4) нитразепам
14. ПОКАЗАНИЯ К ПРИМЕНЕНИЮ НИТРАЗЕПАМА:
*1) нарушение сна
*2) эпилепсия
3) острая дыхательная недостаточность
4) усиление саливации
Психоаналептики
Эту группу психофармакологических препаратов объединяет возможность психоактивирующего ("психоэнергетического") влияния на психическую деятельность. В нее входят различные по клиническому эффекту и механизмам действия препараты из разных химических групп. По особенностям клинико-фармакологического действия различают тимоаналептики (антидепрессанты, психостимуляторы (психоактиваторы), актопротекторы и ноотропы [Александровский Ю. А., 2022].
Психостимуляторы
Психостимуляторы – психотропные вещества, активизирующие психическую и, в меньшей степени – физическую активность организма. Некоторые из них стимулируют высшие психические функции, ускоряют процесс мышления, быстро снимают усталость, сонливость и вялость, повышают мотивацию и работоспособность, повышают общительность, улучшают настроение, улучшают способность к восприятию внешних раздражителей (ускоряют ответные реакции, обостряют слух и зрение, возможность цветоразличения), повышают двигательную активность и мышечный тонус, улучшают координацию движений, повышают выносливость и немного физическую силу. Многие из препаратов этой группы способны вызывать наркотическое привыкание и пристрастие. К группе психостимуляторов могут относиться как лекарственные препараты, так и общедоступные средства (кофеин, никотин), а также запрещённые во многих странах вещества (кокаин, катинон, метамфетамин, амфетамин, однако амфетамины находят ограниченное применение в медицине в западных странах) [Психостимулятор, 2023].
Препараты других фармакологических групп, например, некоторые антидепрессанты, ноотропы, адаптогены (к примеру, женьшень, пантокрин, элеутерококк, также могут оказывать психостимулирующее воздействие [Психостимулятор, 2023].
Классические психостимуляторы усиливают катехоламиновую (дофаминовую и, менее значительно, норадреналиновую) нейротрансмиссию непосредственно повышая синаптическую концентрацию нейротрансмиттеров, и по большей части делятся на две категории: ингибиторы обратного захвата и стимуляторы выброса катехоламинов.
Ингибиторы обратного захвата блокируют транспортные белки, ответственные за транспорт высвобожденного нейротрансмиттера обратно в пресинаптический нейрон для устранения и переработки, тем самым повышая синаптическую концентрацию сего нейротрансмиттера. К ингибиторам обратного захвата дофамина относятся, среди прочих, наркотик кокаин, и лекарственные средства метилфенидат, модафинил, мезокарб и фепрозиднин.
Стимуляторы выброса, иначе, препятствуют концентрированию нейротрансмиттеров в везикулах и способствуют фосфориляции транспортных белков, что меняет направление транспорта из клетки наружу. Таким образом нейротрансмиттер постоянно «вытекает» из нервной клетки, даже при отсутствии сигнала, необходимого для везикулярного выброса. К стимуляторам выброса дофамина относятся в первую очередь производные амфетамина, включая метамфетамин и сам амфетамин.
Стимулирующее действие кофеина главным образом основано на блокировании рецепторов аденозина. Также кофеин способствует торможению активности фермента фосфодиэстеразы, разрушающего цАМФ и цГМФ, что приводит к их накоплению в клетках и вызывает адреналино-подобные эффекты.
В психиатрии психостимуляторы чаще всего применяются для терапии синдрома дефицита внимания и гиперактивности. Помимо этого, они эффективны при амотивационных состояниях и нарколепсии. При адинамической депрессии, чаще всего встречаемой при шизофрении, психостимуляторы могут сочетаться с антидепрессантами. Также показанием к применению являются апатоабулические, ступорозные и субступорозные состояния; невротические расстройства с заторможенностью; астенические состояния, сопровождаемые вялостью, апатией, сонливостью.
Показанием к применению психостимуляторов также является снижение способности к концентрации внимания, повышенная психическая утомляемость, снижение физической работоспособности и быстрая интеллектуальная истощаемость при нейроинфекциях, интоксикациях, черепно-мозговых травмах, нарушениях мозгового кровообращения, перенесённых соматических заболеваниях. Также психостимуляторы эффективны при астеноипохондрических и астено-депрессивных синдромах и алкогольном абстинентном синдроме после отнятия алкоголя. Могут применяться для повышения настроения и интереса к жизни у тяжёлых соматических больных с апатией и социальной отгороженностью [Психостимулятор, 2023].
Список психостимуляторов [Психостимулятор, 2023]:
• Фенилэтиламины, в частности
Амфетамины:
Амфетамин
Метамфетамин
MDMA (метилендиоксиметамфетамин)
Эфедрин и псевдоэфедрин
Фенилпроп аноламин
Пара-Метоксиамфетамин
Катиноны:
Катинон
Меткатин (эфедрон)
Мефедрон
Метилон
Флефедрон
Амфепрамон
Альфа-пирролидинофены
• Альфа-Пирролидинопентиофенон (a-PVP)
• 1 DPV (метилендиоксипировалерон)
Фентермин
• Оксазолины
4-Метиламинорекс
Аминорекс
Пемолин
• Производные пиперазина
мета-хлорфенилпиперазин
Бензилпиперазин
• АМПАкины
• Кокаин
• Модафинил
• Аминептин
• Норадреналин
• Кофеин
• Никотин
Астения характеризуется снижением физиологического резерва и функций многих систем организма, приводящий к повышенной уязвимости организма человека к воздействию эндо- и экзогенных факторов, с высоким риском развития неблагоприятных исходов для здоровья, потери автономности и смерти [Хроническая, 2020].
Развитие старческой астении (СА) сопровождается снижением физической и функциональной активности, адаптационного и восстановительного резерва организма, повышает риск развития неблагоприятных исходов – госпитализаций в 1,2–1,8 раза, развития функциональных дефицитов в 1,6–2,0 раза, смерти в 1,8–2,3 раза, физических ограничений в 1,5–2,6 раза, падений и переломов в 1,2–2,8 раза [Старческая, 2020].
По данным исследований распространенность СА среди проживающих дома людей 65 лет и старше в среднем составляет около 10,7 %, преастении – 41,6 %. Распространенность СА увеличивается с возрастом, достигая среди лиц 85 лет и старше 26,1 %. Синдром СА достоверно чаще диагностируется у женщин, чем у мужчин. В домах престарелых распространенность СА достигает 52,3 % [Старческая, 2020].
Рекомендуется прием препаратов витамина D (800–2000 ME) или его производных пациентам с синдромом старческой астении и дефицитом/недостатком витамина D <30 нг/мл (75 нмоль/л) с целью коррекции его уровня, профилактики падений и переломов и улучшения прогноза жизни (1В). Рекомендовано назначение антиостеопоротической антирезорбтивной терапии (алендроновой кислотой, золедроновой кислотой, деносумабом) пациентам с СА [Старческая, 2020].
Под утомляемостью, которая встречается в среднем у 40–60 % пациентов с болезнью Паркинсона (БП), понимают ощущение почти постоянной усталости, отсутствия энергии, физического и/или психического истощения.
Рекомендуется применение ингибитора моноаминоксидазы (тип В) разагилина в дозе 1 мг/сутки, антидепрессанта СИОЗС или СИОЗСН пациентам с утомляемостью и недостаточной коррекцией двигательных симптомов БП [Болезнь Паркинсона, 2022].
Тесты для самоконтроля
1. Указать психомоторные стимуляторы:
+ Фенамин
+ Меридил
– Аминолон
+ Сиднокарб
– Пирацетам
– Имизин
+ Кофеин
2. Какие механизмы действие психомоторных стимуляторов (фенилалкиламины и их аналоги)?
– Усиливают синтез норадреналина в центральных адренергических синапсах
+ Нарушают депонирование синтезированного медиатора + Тормозят обратный нейрональный захват медиатора и его экстранейрональное поглощение
– Повышают количество энергосубстратов в нейронах головного мозга
+ Ингибируют моноаминоксидазу
3. Какова реакция организма на системный прием психомоторных стимуляторов группы фенилалкиламинов?
– Кумуляция
– Сенсибилизация
+ Тахифилаксия
+ Лекарственная зависимость
4. Отметить основные показания к применению психомоторных стимуляторов
+ При остром отравлении алкоголем, наркотиками, снотворными
+ Нервно-психические заболевания, которые сопровождаются сонливостью, апатией и астенией
– Для постоянного повышения умственной и физической работе способности
+ Для устранения побочных эффектов при использовании средств угнетающего типа
– Для получения анорексигенного эффекта
+ Экстремальные условия для временного повышения умственной и физической работоспособности
5. В чем состоит механизм психостимулирующего действия кофеина?
– Возбуждает адренорецепторы
+ Блокирует аденозиновые рецепторы
+ Угнетает фермент фосфодиэстеразу
– Угнетает обратный нейрональный захват медиатора
– Способствует высвобождению медиатора из нервных окончаний
6. Отметить свойства, присущие общетонизирующим средствам:
+ Для получения эффекта требуется длительное назначение
– Эффект проявляется при однократном приеме
+ Тонизирующий эффект мягкий, без признаков возбуждения
+ Имеют низкую токсичность
– Вызывают пристрастие
+ Не вызывают пристрастия и привыкания
+ Имеют адаптогенные свойства
7. Что характерно для группы психомоторных стимуляторов?
+ Повышают умственную и физическую работоспособность при однократном приеме
+ Длительный прием приводит к истощению резервных возможностей организма
+ Снижают аппетит
+ Повышают возбудимость жизненно важных центров
+ Усиливают работу сердца и повышают артериальное давление
+ Возможно развитие лекарственной зависимости
– Лекарственную зависимость не вызывают
Антидепрессанты
Антидепрессанты – психотропные лекарственные средства, применяемые прежде всего для терапии депрессии, оказывающие влияние на уровень нейромедиаторов, в частности, серотонина, норадреналина и дофамина. У депрессивного больного они улучшают настроение, уменьшают или снимают тоску, вялость, апатию, тревогу, беспокойство, раздражительность и эмоциональное напряжение, повышают психическую активность и продолжительность сна, нормализуют аппетит (тимолептическое действие).
структуру
Антидепрессанты не вызывают улучшения настроения у человека, не страдающего депрессией.
Депрессивный эпизод (ДЭ) – аффективное расстройство, характеризующееся в типичных случаях снижением настроения, утратой интересов и удовольствия, снижением энергичности, которое может привести к повышенной утомляемости и сниженной активности. Отмечается выраженная утомляемость даже при незначительном усилии [Депрессивный, 2021]. К другим симптомам относятся сниженная способность к сосредоточению и вниманию; сниженные самооценка и чувство уверенности в себе; идеи виновности и уничижения (даже при легком типе эпизода); мрачное и пессимистическое видение будущего; идеи или действия, направленные на самоповреждение или суицид; нарушенный сон; сниженный аппетит [Международная, 1994].
Возникновение депрессивных расстройств детерминировано сочетанием множества факторов: биологических (конституционально-генетических), психологических и социальных. Среди биологических концепций традиционной является моноаминовая теория депрессии, согласно которой основным патогенетическим механизмом ее возникновения является недостаточность синаптической активности моноаминов (серотонина, дофамина, норадреналина) головного мозга [Депрессивный, 2021].
Антидепрессанты следует назначать в минимальных эффективных дозах; при отсутствии побочных эффектов или при редукции побочных эффектов в течение нескольких дней рекомендуется производить увеличение дозы в пределах стандартных дозировок до тех пор, пока симптоматика не начнет ослабевать. В случае отсутствия динамики или недостаточного эффекта (степень редукции симптоматики от 25 % до 50 %) через 3–4 недели рекомендуется наращивание дозы до максимальной [Депрессивный, 2021].
Тимоаналептический эффект обычно возникает через 3–4 недели лечения, однако в некоторых случаях, особенно при применении СИОЗС, улучшение развивается более постепенно и достижение полноценного эффекта наблюдается на 4–6-й или даже 8-й неделе. У большинства респондеров на терапию клиническое улучшение становится заметным уже в течение первых двух недель лечения. Обычно такой ранний ответ связан с более благоприятным прогнозом курсовой эффективности проводимой терапии.
Не существует доказательных данных о большей эффективности или более быстром начале действия антидепрессанта какого-либо одного класса, хотя при тяжелых, требующих госпитализации, депрессиях некоторые ТЦА (амитриптилин и кломипрамин) и венлафаксин оказываются несколько эффективнее, чем селективные ингибиторы обратного захвата серотонина (СИОЗС). В отношении антидепрессантов второго поколения сравнительный мета-анализ показал, что миртазапин, эсциталопрам, венлафаксин и сертралин были несколько более эффективны, чем дулоксетин, флуоксетин, флувоксамин и пароксетин [Депрессивный, 2021].
Антидепрессанты из классов СИОЗС, СИОЗСН, а также другие средства второго и третьего поколений в целом переносятся лучше, чем препараты первого поколения (ТЦА), что способствует уменьшению вероятности самостоятельного отказа пациентов от их приема.
Таблица 3
Рекомендуемые дозы антидепрессантов [Депрессивный, 2021]

Пациентам с легким ДЭ рекомендовано назначение антидепрессанта в пероральной форме: СИОЗС, с умеренным ДЭ – назначение СИОЗС, СИОЗСН, миртазапина, агомелатина и вортиоксетина, с тяжелой формой ДЭ без психотических симптомов – назначение антидепрессанта с широким спектром нейрохимического механизма действия: СИОЗСН, миртазапин, ТЦА, обладающих несколько большей эффективностью при депрессии тяжелой степени по сравнению с СИОЗС (1А). Предпочтение в силу лучшей переносимости следует отдать СИОЗСН (венлафаксин, дулоксетин, милнаципран) либо миртазапину, а потом ТЦА (имипрамин, амитриптилин, кломипрамин). СИОЗС и гетероциклицеские препараты первого поколения (пирлиндол, пипофезин, тразодон), обладающие несколько лучшей переносимостью, но и меньшей эффективностью, являются препаратами второго выбора [Депрессивный, 2021].
Стратегия перевода на терапию неселективными ингибиторами моноаминооксидазы не используется вследствие неблагоприятного соотношения риск-польза (в частности, возможности развития гипертонического криза). Тем не менее, в ряде случаев перевод на ИМАО-А, обладающие обратимым и селективным действием (пирлиндол), может дать быстрый положительный эффект, поскольку речь идет о совершенно другом механизме действия и стимулировании выброса в синаптическую щель всех трех моноаминовых нейромедиаторов.
Всем пациентам с резистентностью к антидепрессивной монотерапии рекомендована комбинированная терапия с использованием сочетаний антидепрессантов с комплементарными механизмами действия для достижения синергического тимоаналептического эффекта: комбинирование ТЦА и СИОЗС; комбинирование ингибитора обратного захвата моноаминов (СИОЗС, СИОЗСН или ТЦА) с антидепрессантами, блокирующими альфа-2-адренергические ауторецепторы (например, миртазапин, миансерин) (1А). К негативным сторонам данной стратегии следует отнести повышенный риск взаимодействий между используемыми препаратами, усиление побочных эффектов и более высокие экономические затраты. Наиболее значителен риск возникновения антигистаминовых побочных эффектов (прибавка веса и избыточная седация) и антихолинергических побочных эффектов (снижение концентрации внимания и спутанность). Следует избегать сочетания ИМАО-А с СИОЗС и другими серотонинергическими антидепрессантами (например, кломипрамин, венлафаксин) вследствие потенциальной возможности развития серотонинового синдрома [Депрессивный, 2021].
При присоединении любого антипсихотика 2 поколения возрастает общее число побочных эффектов, включая гиперпролактинемию, метаболические нарушения (увеличение массы тела, дислипидемия, нарушение углеводного обмена), лейкопению, седацию и сонливость, антихолинергические и экстрапирамидные побочные эффекты, что требует тщательной оценки отношения риск/польза при их использовании вместе с антидепрессантами.
При лечении терапевтически резистентной депрессии, рекомендуемой стартовой дозой арипипразола является 5 мг/сут с возможным последующим повышением дозы до максимальной 15 мг/сут. Наиболее частыми нежелательными явлениями при применении арипипразола являются экстрапирамидные расстройства, акатизия и увеличение веса. Рекомендуемой стартовой дозой кветиапина является 50 мг/сут с возможным повышением дозы до 100–300 мг/сут. Максимальная доза не должна превышать 600 мг/сут. При этом необходимо учитывать возможность появления седации и набора веса [Депрессивный, 2021].
При применении оланзапина в целях аугментации эффекта флуоксетина рекомендуемый диапазон доз составляет 5–10 мг/сут. Наиболее часто возникают такие побочные эффекты, как увеличение веса, седация и повышение пролактина. Что касается применения рисперидона при аугментации антидепрессивной терапии, рекомендуемой стартовой дозой является 0,5 мг/сут, диапазон доз составляет 0,25–3 мг/сут. Следует учитывать возможность развития гиперпролактинемии и экстрапирамидных расстройств.
Всем пациентам с резистентностью к антидепрессивной монотерапии рекомендована аугментация эффекта солями лития (лития карбонатом) в дозе >800 мг (или в дозе, достаточной для достижения концентрации лития в сыворотке >0,5 мкмоль/л) (1В).
Даже небольшие дозы солей лития (концентрация лития в сыворотке 0,5–0,8 ммоль/л) в течение нескольких дней могут привести к улучшению в состоянии больного. Курс терапии не превышает 2–4 недель, однако в случае достижения эффекта терапию следует продолжить в течение нескольких месяцев. Считается, что соли лития могут изменять рецепторную чувствительность постсинаптической мембраны и усиливать действие серотонина [Депрессивный, 2021].
Комбинировать антидепрессант с солями лития нужно осторожно, поскольку повышенные дозировки могут привести к развитию нейротоксических реакций (миоклония, атаксия, возбуждение, спутанность), а при сочетании с аминокислотой L-триптофаном (биологически активная добавка) («ньюкаслский» или «серотониновый» коктейль) – к серотониновому неврологическому синдрому. Кроме того, нежелательные явления при терапии солями лития включают кардиотоксичность, нефротоксичность, тиреотоксичность и прибавку веса. По причине узкого терапевтического диапазона требуется регулярный контроль концентрации лития в крови.
Пациентам с резистентностью к антидепрессивной монотерапии при наличии дополнительных симптоматических показаний (например, тревоги, фобиях, ипохондрических и психотических симптомах) рекомендована аугментация эффекта антипсихотиками 1 поколения, включая присоединение к антидепрессанту: – сульпирида (2В).
Пациентам с резистентностью к антидепрессивной монотерапии рекомендована аугментация эффекта антидепрессантов противоэпилептическими препаратами: ламотриджином в начальной дозе 25 мг/сут с постепенным повышением до 200 мг/сут (1А) или карбамазепином в дозе 400–800 мг/сут (2В) [Депрессивный, 2021].
Комбинация оланзапина с флуоксетином должна применяться с осторожностью у пациентов с избыточным весом, ожирением или метаболическим синдромом. Не показана комбинация оланзапина или рисперидона с карбамазепином, в связи с их интеркуррентным действием на уровне печеночных ферментов.
Период снижения дозы антидепрессанта может занимать нескольких дней, недель или даже месяцев, в зависимости от дозы, продолжительности лечения и фармакологических свойств препарата, а также особенностей состояния пациента. Необходимостьпостепенного снижения дозы обусловлена возможностью развития синдрома отмены. Риск развития синдрома отмены тем выше, чем больше выражены антихолинергические свойства препарата, выше используемая доза и чем длительнее период приема. Среди антидепрессантов новой генерации симптомы отмены наиболее характерны для венлафаксина и СИОЗС с коротким периодом полувыведения (пароксетина), и менее характерны для флуоксетина. Резкая отмена ТЦА может вызвать холинергический феномен «отдачи» (миалгия, схватывающие боли в животе) [Депрессивный, 2021].
Вопросы для самоконтроля
1. Флуоксетин:
A. Блокирует нейрональный захват норадреналина
Б. Блокирует нейрональный захват серотонина
B. Блокирует нейрональный захват серотонина и нарадреналина
Г. Ингибирует моноаминооксидазу
Д. Ингибирует моноаминооксидазу и катехоламин-орто- метилтрансферазу
2. Амитриптилин (все ответы верны, кроме одного):
A. Блокирует обратный нейрональный захват норадреналина и серотонина
Б. Относится к группе трициклических антидепрессантов
B. Обладает психоседативным действием
Г. Снижает концентрацию катехоламинов в синаптической щели
3. Моклобемид (все ответы верны, кроме одного):
A. Блокирует обратный нейрональный захват серотонина и норадреналина
Б. Обратимо ингибирует моноаминооксидазу А
B. Повышает психомоторную активность
Г. Тормозит метаболизм норадреналина, дофамина и серотонина
Д. Применяется при депрессии с гипомоторным компонентом
4. Неизбирательный ингибитор МАО – А и В изоформ:
A. Имизин
Б. Флуоксетин
B. Ниаламид
Г. Амитриптилин
5. Показания к применению антидепрессантов:
A. Неврозы и неврозоподобные состояния
Б. Депрессия, субдепрессия
B. Психозы с бредовым и галлюцинаторным компонентами