
Коллектив авторов
Внутренние болезни
Инфаркт миокарда
Определение. Инфаркт миокарда – это форма ишемической болезни сердца, в основе которой лежит развитие некроза значительного участка миокарда в результате остро возникших нарушений (обычно, полного прекращения) кровотока в одной из крупных коронарных артерий.
Распространенность. В нашей стране частота инфаркта миокарда в различных регионах колеблется от 2 до 5 на 1000 мужчин в год в возрасте от 25 до 64 лет. У женщин в доменопаузальном периоде инфаркт миокарда встречается в 4 раза реже, чем у мужчин. С наступлением менопаузы частота инфаркта возрастает, но не достигает таковой у мужчин. В последние годы в России отмечается рост заболеваемости среди лиц молодого возраста [Чазов Е. И., 1997].
Этиология. Поскольку развитие инфаркта миокарда связано с дестабилизацией течения атеросклероза, то все факторы риска атеросклероза могут рассматриваться и как факторы риска развития инфаркта миокарда.
Патогенез. Обычно инфаркт миокарда возникает в результате тромбоза коронарной артерии (90 – 95 % случаев), который чаще развивается в области измененной атеросклеротической бляшки (разрыв интимы, кровоизлияния). Возникновению локального тромбоза способствуют все факторы, повышающие наклонность к тромбообразованию. К их числу относятся изменения функционального состояния эндотелия или же деэндотелизация участка коронарной артерии, вазоспазм, изменения функциональной активности тромбоцитов с повышением их наклонности к тромбообразованию и освобождению биологически активных веществ, усиливающих коагуляцию и провоцирующих вазоспазм, повышение вязкости крови. Значительно реже инфаркт миокарда развивается при длительном вазоспазме. Исключительно редко причиной инфаркта миокарда может быть остро возникшее повышение потребности миокарда в кислороде при отсутствии адекватного увеличения коронарного кровотока из-за коронарного атеросклероза. Наконец, возможно развитие инфаркта миокарда и при отсутствии коронарного атеросклероза (воспалительные изменения коронарных артерий, их эмболии, чаще всего при инфекционном эндокардите). Но в этих случаях инфаркт миокарда является осложнением основного патологического процесса и не может рассматриваться как проявление ишемической болезни сердца.
Морфология. Морфологически инфаркт миокарда проявляется наличием очага некроза участка миокарда, кровоснабжаемого затромбированной ветвью коронарной артерии. Вокруг зоны некроза обычно выявляется так называемая периинфарктная зона, в которой наряду с некротизированными кардиомиоцитами определяются клетки с проявлениями дистрофии, а также интактные кардиомиоциты. Уже через несколько часов в зоне некроза появляются лейкоциты, и начинается формирование соединительной ткани. При типичном течении рассасывание некротических масс завершается через 7 – 14 дней, окончательное формирование рубца – через несколько месяцев.
Классификация. В основе классификаций инфаркта миокарда лежат величина некроза и его локализация. В нашей стране еще можно встретить разделение на субэпикардиальный, интрамуральный, субэндокардиальный и трансмуральный инфаркт, однако общепринятым является разделение на две формы инфаркта миокарда – с наличием зубца Q (Q-инфаркт миокарда) и без него (не Q-инфаркт миокарда).
Клиническая картина. Прижизненно по клиническим данным инфаркт миокарда впервые был диагностирован В. П. Образцовым и Н. Д. Стражеско в 1910 г.
В течении инфаркта миокарда различают 3 периода: острейший (продолжительностью до 3 часов), острый (до 10 дней) и подострый (до 4 – 8 недель). Некоторые авторы выделяют прединфарктный (диагностируется ретроспективно) и постинфарктный (до 6 месяцев) периоды.
Острейший период охватывает период времени от начала заболевания до начала формирования очага некроза. Клинические проявления определяются острым развитием ишемии значительного участка миокарда. Основным в клинике является болевой синдром (представлен у 80 – 95 % больных). Интенсивность болей широко варьирует, однако у большинства больных отмечаются сильные боли в прекардиальной области с широкой иррадиацией, реже боли локализованы в эпигастральной области (чаще – при инфаркте задней стенки). Боли, как правило, не купируются нитроглицерином и продолжаются более 30 минут. У 10 – 15 % больных инфаркт миокарда протекает без болей. У лиц пожилого возраста с предсуществовавшим кардиосклерозом основным проявлением инфаркта может быть острая левожелудочковая сердечная недостаточность. Инфаркт миокарда может проявляться резчайшей слабостью, синкопальным состоянием. Но приблизительно у 5 – 10 % пациентов острейший период может не сопровождаться субъективными нарушениями.
Практически у всех больных отмечаются разнообразные нарушения ритма, вплоть до фибрилляции желудочков, реже – нарушения проводимости (чаще – при задней локализации инфаркта). При обширном инфаркте возможно развитие кардиогенного шока и/или отека легких.
Физикальное исследование выявляет изменения числа сокращений сердца (тахикардия, брадикардия), глухость тонов, наличие патологических тонов (III, IV), аритмии, проявления застоя в малом круге кровообращения. На высоте болей возможно повышение артериального давления с последующим его снижением. При обширном инфаркте миокарда обычно отмечается гипотония.
Острый период.Вэтот период происходит резорбция очага некроза, и начинает формироваться рубец. Болевой синдром обычно отсутствует. В клинической картине доминируют проявления, обусловленные рассасыванием некротизированных масс (лихорадка). Наиболее частыми осложнениями этого периода являются аритмии, блокады, сердечная недостаточность, острая аневризма. Возможно формирование асептического перикардита и пристеночного эндокардита. У отдельных больных отмечается отрыв папиллярной мышцы, разрыв межжелудочковой перегородки. Одной из частых причин смерти в этот период является разрыв сердца.
Подострый период.Вподостром периоде самочувствие больных, как правило, остается удовлетворительным. Значительно уменьшается риск развития осложнений. Наиболее существенными из них являются формирование хронической аневризмы и развитие хронической сердечной недостаточности. Одним из редких осложнений этого периода является так называемый постинфарктный синдром (синдром Дреслера). Развитие синдрома связано с иммунными нарушениями в ответ на инфаркт миокарда. Синдром Дреслера проявляется перикардитом, реже – плевритом, с соответствующими клинико-лабораторными изменениями. У многих больных при этом выявляется эозинофилия.
Лабораторная и инструментальная диагностика. Развитие инфаркта миокарда сопровождается типичными лабораторными изменениями, обусловленными наличием воспаления и поступлением в кровь энзимов и специфических белков из очага некроза (табл. 1.10).
Таблица 1.10
Наиболее существенные гематологические и биохимические изменения при инфаркте миокарда
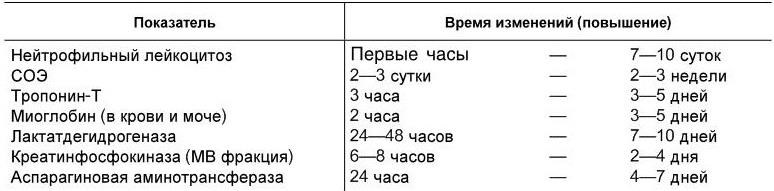
Среди различных маркеров некроза миокарда максимальной специфичностью и чувствительностью (100 %) обладает тропонин Т. Характерно также увеличение содержания фибриногена, С-реактивного белка, α2– и γ – глобулинов.
Электрокардиография наряду с биохимическими исследованиями относится к важнейшим диагностическим методам. Она позволяет не только констатировать наличие инфаркта, но определить его локализацию, распространенность. Типичными ранними ЭКГ-изменениями являются повышение сегмента ST с наличием гигантских зубцов Т, уменьшение вольтажа зубца R и появление патологического зубца Q (рис. 1.6). Нередко зубцы R и Т сливаются (монофазная кривая). Обычно уже к концу первых суток выявляется динамика обратного развития ЭКГ-изменений (уменьшение степени повышения ST, появление постепенно увеличивающихся отрицательных зубцов Т). У многих больных изменения на ЭКГ (наличие зубца Q или QS) остаются на многие годы.
При отсутствии зубца Q (QS) изменения ограничиваются конечной частью желудочкового комплекса: повышение ST или его снижение (депрессия). Депрессия ST характерна для субэндокардиальных изменений. При инфаркте без Q иногда выявляются лишь изменения зубца Т с быстрой (в течение нескольких дней) обратной динамикой.
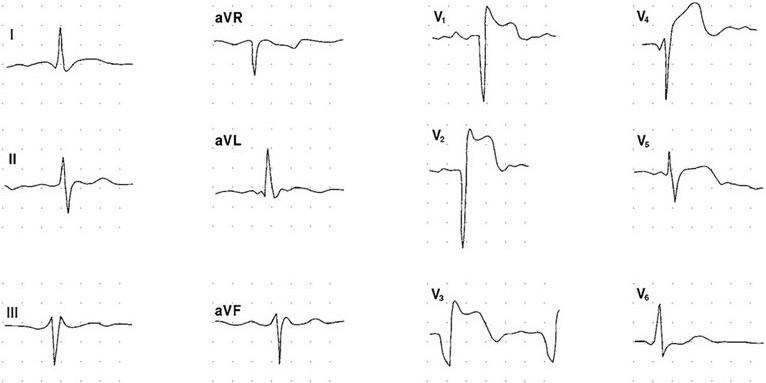
Рис. 1.6. ЭКГ-изменения у больного в острый период переднеперегородочного инфаркта миокарда.
Максимум изменений выявляется в отведениях V1 – 4: наличие зубца Q в V1 – 3, резкий подъем сегмента ST в V1 – 4
Топическая локализация инфаркта основывается на констатации максимальных изменений в определенных ЭКГ-изменениях (табл. 1.11).
Таблица 1.11
Топическая ЭКГ-диагностика инфаркта миокарда

При наличии нарушений ритма и проводимости на ЭКГ выявляются соответствующие изменения.
Трактовка ЭКГ-изменений затруднена у больных с предшествовавшими рубцовыми изменениями, при блокаде левой ножки и у лиц, имеющих кардиостимулятор (желудочковая стимуляция).
Эхокардиография. У больных инфарктом миокарда выявляется зона нарушений сократимости (а-, гипо- или дискинезия), у многих больных – уменьшение фракции изгнания. У лиц после эффективного тромболизиса нередко наблюдается существенное расширение зоны дискинезии, обусловленное временной утратой сократимости кардиомиоцитов (станнирование миокарда). Радионуклидные методы. Использование сцинтиграфии с меченными изотопами технеция и таллия позволяет визуализировать очаг некроза.
Диагноз основывается на анализе данных клинических, лабораторных и инструментальных исследований. В диагнозе отражается локализация инфаркта, его распространенность, осложнения.
Примеры формулировки диагноза:
1. Ишемическая болезнь сердца. Переднеперегородочный инфаркт миокарда 20.09.98. Фибрилляция сердца 21.09.98.
2. Ишемическая болезнь сердца. Задненижний инфаркт миокарда 10.10.98. Полная преходящая атриовентрикулярная блокада с 10.10.98. Временная кардиостимуляция (с 10.10.98 по 15.10.98). Хроническая сердечная недостаточность III ф. к. по NYHA.
Дифференциальный диагноз. При наличии болевого синдрома трудности возникают при других состояниях, протекающих с сильными болями в прекардиальной области.
Эмболия легочной артерии. Боли обычно сопровождаются резкой одышкой, снижением артериального давления, возможна кратковременная потеря сознания, в отдаленные сроки – кровохарканье. На ЭКГ нередко выявляются глубокие S1 и зубец QIII. В V1 – 3 возможно повышение ST, переходящее в отрицательный зубец Т. При крупных эмболиях отмечается смещение переходной зоны влево и пульмональные Р. Диагноз становится более очевидным при наличии тромбофлебита или других источников эмболии. Уточнение диагноза возможно при рентгенологическом, радионуклидном (легкие, сердце) исследовании и компьютерной томографии.
Острый перикардит характеризуется наличием лихорадки и воспалительных изменений крови уже во время появления болевого синдрома.
Боли обычно связаны с положением тела. На ЭКГ – подъем ST во многих отведениях без характерного для инфаркта миокарда дискордантного смещения ST. Типична очень быстрая динамика ЭКГ изменений с появлением отрицательного зубца Т. Диагноз уточняется при эхокардиографическом исследовании.
Расслаивающая аневризма аорты. Чаще возникает у больных с высокой артериальной гипертензией или с синдромом Марфана. Боли обычно иррадиируют в спину, сопровождаются жаждой, нередко уже в ближайшие часы появляются диастолический шум над аортой (недостаточность аортального клапана) и анемия. На ЭКГ отсутствуют специфические изменения. При повторном рентгенологическом исследовании может наблюдаться расширение тени аорты. Диагноз уточняется при компьютерной томографии и ангиографии.
Дифференциальный диагноз не ограничивается вышеперечисленными заболеваниями. Все заболевания, проявляющиеся болевым синдромом в прекардиальной области, могут быть причиной диагностических ошибок. При локализации болей в эпигастральной области дифференциальный диагноз проводят с перфорацией язвы, острым холециститом, панкреатитом, кишечной непроходимостью.
Течение. Инфаркт миокарда характеризуется высоким риском развития осложнений, некоторые из которых несовместимы с жизнью. Течение непроникающего инфаркта миокарда, как правило, благоприятное.
Прогноз и исходы. Прогноз больного и сегодня остается серьезным. Не менее 25 % больных погибают внезапно, до прибытия врача. Госпитальная летальность колеблется в пределах 7 – 15 %. В течение первого года после выписки из стационара умирают еще 5 % пациентов. Наиболее неблагоприятен прогноз больных с повторным инфарктом миокарда. Причиной смерти являются аритмии, кардиогенный шок, разрыв миокарда, в отдаленном периоде – хроническая сердечная недостаточность. Ближайший прогноз больных с непроникающим инфарктом миокарда существенно лучше, чем с проникающим. Однако почти у трети из них в течение последующего года отмечаются неблагоприятные исходы (дестабилизация течения стенокардии, инфаркт миокарда, внезапная смерть).
Лечение. Целью терапии является сохранение максимального количества жизнеспособного миокарда (ограничение очага некроза), профилактика и терапия осложнений.
Обязательна госпитализация в отделения (палаты) интенсивной терапии. При отсутствии осложнений длительность пребывания в отделении интенсивной терапии составляет 2 – 3 суток. В эти сроки больной соблюдает постельный режим. Постоянно мониторируется ЭКГ и при возможности – другие гемодинамические параметры.
Основная задача врача в острейший период – снятие болевого синдрома. С этой целью внутривенно вводятся наркотические анальгетики (морфин, промедол), проводится нейролептаналгезия (одновременное введение дроперидола – 1 – 2 мл 0,25 % раствора и фентанила 1 – 2 мл 0,005 % раствора). Эти препараты используются и на догоспитальном этапе.
При госпитализации в ранние сроки (до 8 часов) обязательной является тромболитическая терапия и антикоагулянтная терапия. Для тромболизиса используются стрептокиназа (стрептодеказа, целиаза), урокиназа, проурокиназа, тканевой активатор плазминогена. В России наиболее часто применяется стрептокиназа внутривенно. Первая доза (200 000 – 250 000 МЕ) вводится струйно для нейтрализации циркулирующих антител к стрептокиназе, после чего переходят на медленное введение в течение 1 – 2 ч. Суммарная доза не превышает 1 000 000 – 1 500 000 МЕ. Стрептокиназа обеспечивает восстановление коронарного кровотока у 50 – 60 % пациентов, урокиназа и тканевой активатор плазминогена – в 60 – 70 %.
Абсолютные противопоказания для тромболитической терапии: обширная травма или хирургические вмешательства в течение 2 предшествовавших месяцев, инсульты – в течение 6 месяцев, наличие высокой артериальной гипертензии, язва желудка или 12-перстной кишки, кровотечения или геморрагический диатез при госпитализации, дополнительно для стрептокиназы – аллергические реакции, анафилаксия.
Одновременно со стрептокиназой вводится внутривенно гепарин (однократно – 10 000 ед., затем около 1000 ед. капельно в час). В последующие 7 – 10 дней гепарин (или низкомолекулярные гепарины) вводят подкожно (доза гепарина не превышает 10 000 ед. 2 раза в день, под контролем свертываемости крови).
Обязательным компонентом терапии являются нитраты (при отсутствии гипотонии). Они могут назначаться как внутрь в обычных терапевтических дозах, так и вводиться длительно капельно внутривенно (под контролем артериального давления). Нитраты уменьшают работу сердца, снимают коронароспазм, увеличивают коронарный кровоток, особенно – субэндокардиальный.
При терапии больных широко используются β-адреноблокаторы, не обладающие внутренней симпатомиметической активностью, в обычных терапевтических дозах. Их использование существенно улучшает ближайший и отдаленный прогноз (снижение летальности на 20 – 25 %), преимущественно, из-за антиаритмического и антиишемического действия. Основные противопоказания – брадикардия, гипотония, нарушения проводимости, бронхиальная астма, выраженная сердечная недостаточность.
В настоящее время уже с первого дня госпитализации назначаются дезагреганты, преимущественно, аспирин в дозе 100 – 125 мг в сутки при отсутствии противопоказаний. Достаточно широко в комплексной терапии используются ингибиторы ангиотензинпревращающего фермента. Показания к их назначению – сердечная недостаточность или же систолическая дисфункция миокарда (фракция изгнания < 45 %). Вполне допустимо применение кальциевых антагонистов, предпочтительнее – дигидропиридины длительного действия (амлодипин, фелодипин) или же медленно всасывающиеся формы нифедипина (коринфар-ретард, адалат SR, осмо-адалат), верапамил и дилтиазем с учетом известных противопоказаний.
Присоединение осложнений является показанием для их терапии. При фибрилляции желудочков – дефибрилляция, при резкой брадикардии при нарушении проводимости – атропин внутривенно и временная кардиостимуляция, при жизнеугрожающих аритмиях – антиаритмические препараты (лидокаин, амиодарон, соталол, β-адреноблокаторы). При наличии истинного кардиогенного шока используются адреностимуляторы (допамин, добутамин капельно внутривенно) в сочетании с глюкокортикоидами (преднизолон, гидрокортизон внутривенно), а также контрпульсация. У больных с острой сердечной недостаточностью препаратами выбора являются петлевые диуретики внутривенно (фуросемид до 100 и более мг), нитраты внутривенно (нитроглицерин, динитраты, нитропруссид натрия), ингаляция кислорода. Нежелательно применение сердечных гликозидов.
Лечебную физкультуру начинают при отсутствии болей и осложнений уже на второй день после госпитализации. В нашей стране используются режимы 3 – 4-недельной стационарной реабилитации.
В большинстве западных стран длительность стационарного лечения не превышает 7 суток при неосложненном заболевании, широко используются ангиопластика, стентирование, а при наличии специальных показаний – аортокоронарное шунтирование. К сожалению, в условиях современной экономической ситуации в России эти методы недоступны абсолютному большинству больных.
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ
Определение. Инфекционный эндокардит – заболевание, клинические проявления при котором обусловлены локализацией инфекционного агента на клапанных структурах сердца, пристеночном эндокарде или эндотелии прилежащих к сердцу крупных сосудов.
Распространенность. Истинная распространенность инфекционного эндокардита неизвестна. По данным различных авторов, она колеблется в пределах 0,16 – 1,0 на тысячу госпитализированных больных. В последние годы во всех странах отмечается значительное увеличение количества больных инфекционным эндокардитом. Это обусловлено частым использованием инвазивных методов диагностики и лечения (многочасовое наличие катетеров в сосудах), широким распространением операций на сердце, увеличением числа «внутривенных» наркоманов.
Инфекционный эндокардит может возникнуть в любом возрасте, хотя с наибольшей частотой он развивается у лиц среднего и пожилого возраста (исключение составляют наркоманы). Чаще заболевают мужчины (соотношение мужчины: женщины равно 2 – 3: 1). Наиболее высок риск развития эндокардита у лиц с приобретенными и врожденными пороками сердца, у пациентов, имеющих искусственные клапаны или ранее перенесших инфекционный эндокардит.
Этиология. Возбудителем заболевания может быть любой инфекционный агент (бактерии, грибы, сальмонеллы и др.), но у абсолютного большинства больных (около 95 %) развитие заболевания обусловлено бактериальной инфекцией, наиболее часто – зеленящим стрептококком (30 – 60 %), стафилококком (30 – 40 %). В последние годы существенно увеличилась частота инфекционного эндокардита, вызванного грамотрицательной флорой (синегнойная палочка, энтеробактерии) и грибами. Грибковый эндокардит наиболее часто возникает у больных после протезирования клапанов сердца. По данным различных лабораторий, у 5 – 25 % больных даже при повторных посевах крови возбудителя обнаружить не удается, что чаще всего обусловлено предварительной антибактериальной терапией.
Патогенез. В развитии заболевания решающее значение имеют два фактора: наличие возбудителя в крови (бактериемия) и условий, благоприятствующих его оседанию (колонизации) на эндокарде (эндотелии).
Кратковременная бактериемия достаточно часто возникает в организме (экстракция зубов, воспалительные заболевания, операции и инструментальные процедуры на органах урогенитального тракта и др.).
Обычно инфекционный агент достаточно быстро исчезает из крови и уничтожается. Наиболее существенными факторами, способствующими колонизации возбудителя, является его вирулентность и изменения эндотелия (повреждение). Повреждение эндотелия чаще отмечается у пациентов с пороками сердца, особенно при наличии значительного градиента давления между двумя камерами (пороки аортального и митрального клапана, дефект межжелудочковой перегородки). Гемодинамический удар о стенку в сочетании с нарушениями кровотока (турбулентность) создают благоприятные условия для повреждения эндотелия и формирования в местах повреждений стерильных микротромбов (небактериальный тромботический эндокардит). Небактериальный тромботический эндокардит часто возникает также после операций на сердце, при длительном наличии в сосудах катетеров. При наличии абактериальных тромбов инфекционные агенты оседают на них. Так возникает локальный инфекционный очаг в сердечно-сосудистой системе. Риск инфицирования эндотелия значительно возрастает при поступлении в кровоток инфекционных агентов, обладающих высокой адгезивностью.
Дополнительным фактором, способствующим возникновению инфекционного эндокардита, является снижение противоинфекционной защиты организма (хронические заболевания, длительная терапия цитостатиками, глюкокортикоидами, антибиотиками).
Длительное наличие инфекционного агента в организме в сочетании с постоянной антигенной стимуляцией продуктами распада тканей приводят к выработке антител против этих антигенов с увеличением в крови количества циркулирующих иммунных комплексов и их отложением в органах и тканях. Присоединение иммунного компонента при инфекционном эндокардите приводит к изменению клинико-лабораторных проявлений заболевания (васкулиты, нефрит, асептический миоперикардит).
Морфология. При инфекционном эндокардите выявляются типичные морфологические изменения: наличие полипозных инфицированных образований (вегетаций) с некрозами прилежащих тканей, формированием изъязвлений, перфорацией и надрывами клапанов. Нередко выявляются абсцессы в области клапанных колец, реже – в миокарде. При присоединении иммунных нарушений наблюдаются типичные для васкулита и нефрита морфологические изменения (отложения иммунных комплексов в субэндотелии, мезангии с типичными вторичными пролиферативно-воспалительными и некротическими изменениями).
Классификация инфекционных эндокардитов отражает исходное (до начала заболевания) состояние сердечно-сосудистой системы, этиологию, локализацию патологического процесса, остроту течения, наличие осложнений (табл. 1.12).
Таблица 1.12
Классификация инфекционного эндокардита
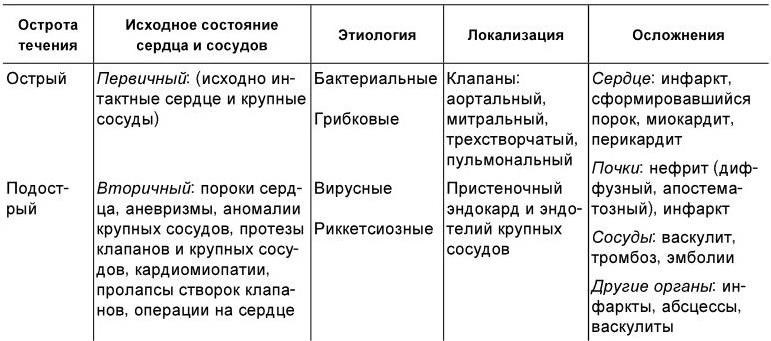
С учетом исходного состояния сердечно-сосудистой системы различают первичный и вторичный инфекционный эндокардит. Первичный эндокардит возникает при исходно интактном сердце, вторичный – у больных с предсуществовавшими изменениями сердца и крупных сосудов (пороки, кардиомиопатии, аневризмы и др.).
Острый инфекционный эндокардит является одним из проявлений острого сепсиса. Поэтому под термином инфекционный эндокардит обычно подразумевают заболевание подострого течения (в прошлом использовался термин подострый инфекционный эндокардит).
Клиническая картина. Клинические проявления чрезвычайно разнообразны – от картины сепсиса до малосимптомного течения. Малосимптомное течение более характерно для лиц пожилого возраста и пациентов с предсуществовавшей сердечной недостаточностью.
Клиническая картина инфекционного эндокардита складывается из проявлений, обусловленных наличием инфекции, локализацией местных изменений (формирование недостаточности пораженного клапана), иммунологическими нарушениями и осложнениями.
Наиболее характерным признаком инфекционного эндокардита является повышение температуры (наблюдается у 85 – 92 % пациентов). Гектическая лихорадка более типична для эндокардита, вызванного стафилококком, кишечной и синегнойной палочкой. При наличии провоцирующего события (экстракция зуба, инфицированная рана и др.) лихорадка появляется через 1 – 2 недели. Лихорадка обычно сочетается с ознобами, потливостью, недомоганием, артралгиями и миалгиями, ухудшением аппетита.
Приблизительно у трети больных выявляются проявления геморрагического диатеза, обусловленные повышением проницаемости сосудистой стенки и васкулитами. У 10 – 20 % больных возникают эмболии (в мозг, почки, сердце, легкие и в другие органы) с возможным формированием абсцессов, у 80 – 90 % пациентов отмечаются проявления сердечной недостаточности. При физикальном исследовании обращает на себя внимание бледность больных, наличие петехий (на конъюнктиве, слизистых, коже), пятен Джейнуэя (мелкие геморрагические высыпания на ладонях и стопах), узелков Ослера (мелкие болезненные узелки на пальцах).
При исследовании сердечно-сосудистой системы наблюдается тахикардия и проявления, связанные с локализацией патологического процесса на клапанах, скоростью и выраженностью формирования недостаточности клапана, а также предсуществовавшей патологией. Как правило, выявляется различная степень кардиомегалии, при аускультации – данные за наличие формирующейся недостаточности пораженного клапана. Достаточно характерна динамичность аускультативных изменений. У ряда больных шумы могут появляться или резко изменяться внезапно (перфорация, отрыв створки, разрыв хорды). При выраженной аортальной недостаточности будут представлены и ее периферические симптомы (быстрый пульс, высокое пульсовое давление, пульсация крупных артерий).
Наличие сердечной недостаточности и эмболий проявляется соответствующими изменениями (гепатомегалия, отеки, застой в легких). Приблизительно у 1/3 больных выявляется спленомегалия.
Лабораторная и инструментальная диагностика. При исследовании крови отмечается нормохромная анемия, сдвиг лейкоцитарной формулы влево при повышенном или нормальном количестве лейкоцитов, тромбоцитопения, увеличение СОЭ. Биохимические данные характеризуются воспалительными изменениями (наличие С-реактивного белка, повышение фибриногена, α2– и γ – глобулинов, положительная тимоловая проба), у 50 % больных выявляется ревматоидный фактор, увеличение количества циркулирующих иммунных комплексов, снижение титра комплемента, у отдельных больных – ложноположительная реакция Вассермана.
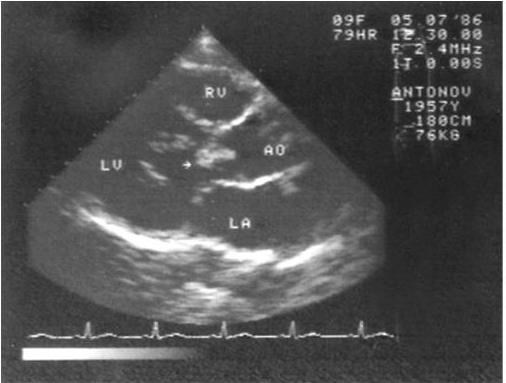
Рис. 1.7. Эхокардиограмма больного инфекционным эндокардитом. Вегетация (указана стрелкой) на аортальном клапане
Наиболее существенным методом диагностики являются повторные посевы крови. Забор крови желательно производить до начала антибактериальной терапии из разных вен в количестве 10 – 15 мл 3 – 5 раз с интервалом не менее 15 мин. при остром эндокардите и 3 – 5 проб с интервалом 4 – 6 ч – при подостром. Положительными считаются результаты, при которых рост одного и того же возбудителя отмечается в большинстве проб. При бактериальном эндокардите при соблюдении всех правил забора и культивирования крови возбудитель выявляется у 90 – 95 % больных, предварительно не получавших антибиотики. Отрицательные результаты обычно отмечаются у больных, длительно получавших антибактериальную терапию, а также при грибковых и вирусных миокардитах. Поэтому в целом частота отрицательных результатов посевов крови составляет около 20 – 35 %.
Присоединение гломерулонефрита проявляется типичными изменениями мочи (протеинурия, наличие эритроцитов и цилиндров).
Результаты рентгенологического и ЭКГ-исследования отражают изменения сердца, обусловленные формулирующимся пороком и предсуществовавшей патологией.
Наиболее информативным инструментальным методом исследования является эхокардиография, особенно транспищеводная, выявляющая достаточно мелкие вегетации (не менее 5 мм) и сопутствующие изменения клапанного аппарата (рис. 1.7). Вегетации обычно появляются не раньше, чем через 2 недели после начала заболевания и длительно сохраняются после выздоровления (несколько месяцев). Ультразвуковое исследование, как правило, выявляет увеличение размеров селезенки.
Диагноз инфекционного эндокардита считается достоверным при наличии лихорадки, шума в сердце, эмболий, бактериемии, вегетаций по данным эхокардиографического исследования. При необнаружении вегетаций диагноз оценивается как вероятный, а наличие лихорадки неизвестного генеза в сочетании с эмболиями и/или шумом в сердце является критерием возможного инфекционного эндокардита.
В диагнозе необходимо отразить характер заболевания (первичный, вторичный), при положительных результатах посевов – этиологию, характер предсуществовавшей патологии, локализацию местных изменений, осложнения.
Примеры формулировки диагноза:
1. Первичный инфекционный эндокардит, вызванный зеленящим стрептококком, аортальная недостаточность.
2. Вторичный инфекционный эндокардит митрального клапана. Сложный митрально-аортальный порок ревматической этиологии. Эмболический инфаркт миокарда 12.07.98. Сердечная недостаточность III ф. к. по NYHA.
Дифференциальный диагноз. Поскольку проявления инфекционного эндокардита чрезвычайно разнообразны, то его приходится дифференцировать со многими заболеваниями. Это диффузные заболевания соединительной ткани, васкулиты, лимфомы и другие злокачественные новообразования. У лиц с ревматическими пороками сердца появление симптомов инфекционного эндокардита нередко длительно трактуется как рецидив ревматизма. У любого больного с лихорадкой невыясненного происхождения необходимо исключить инфекционный эндокардит.
Решающее значение в постановке правильного диагноза имеет ежедневная внимательная аускультация сердца (появление новых шумов регургитации или изменения характера предсуществовавших шумов), данные эхокардиографического и бактериологического исследований.
Течение. Острый инфекционный эндокардит протекает по типу острого сепсиса. Особенности течения подострого эндокардита обусловлены характером возбудителя, путем его поступления, возрастом больных и наличием сердечной недостаточности. В частности, для грибкового эндокардита характерны крупные вегетации, выявляемые при эхокардиографическом исследовании, эмболии крупных артерий большими эмболами и быстрое разрушение клапана. Инфекционный эндокардит наркоманов обычно локализован на трехстворчатом, реже – пульмональном клапане и часто осложняется повторными эмболиями в малый круг кровообращения.


