
Василий Анатольевич Шуваев
Миелопролиферативные новообразования
В исследовании PACE, по результатам которого понатиниб был зарегистрирован FDA, была оценена безопасность и эффективность применения понатиниба у 449 пациентов с хроническим миелолейкозом (ХМЛ) в хронической фазе (ХФ-ХМЛ, 267 пациентов), фазе акселерации (ФА-ХМЛ, 83 пациента) или при бластном кризе (БК-ХМЛ, 62 пациента) и у пациентов с положительным по филадельфийской хромосоме острым лимфобластным лейкозом (Ph+ОЛЛ, 32 пациента), с резистентностью или непереносимостью предшествующей терапии ингибиторами тирозинкиназы (ИТК) (дазатинибом или нилотинибом) или с наличием мутации T315I [49].
В общей сложности 55 % пациентов на момент включения в исследования имели одну или несколько мутаций киназного домена BCR::ABL. По результатам пятилетнего наблюдения из 267 оцененных пациентов с ХФ ХМЛ 60 % достигли БЦО, 40 % БМО и 24 % МО4.5. Общая пятилетняя выживаемость составила 73 %, прогрессирование в ФА и БК произошло у 3,4 % пациентов. Пациенты с ХФ-ХМЛ, у которых в анамнезе была терапия меньшим количеством ИТК, чаще достигали гематологических, цитогенетических и молекулярных ответов. Из больных ХФ-ХМЛ, получавших ранее один, два, три или четыре ИТК, соответственно, 75 % (12 из 16 пациентов), 68 % (66 из 97 пациентов), 44 % (63 из 142 пациентов) и 58 % (7 из 12 пациентов) достигли БЦО на фоне терапии понатинибом. Из больных ХФ-ХМЛ, у которых на момент включения в исследование не было мутаций, 49 % (66 из 136 пациентов) достигли БЦО.
Наиболее частыми серьезными нежелательными явлениями на фоне терапии понатинибом были: пневмония (7,3 %), панкреатит (5,8 %), боли в животе (4,7 %), фибрилляция предсердий (4,5 %), повышение температуры тела (4,5 %), инфаркт миокарда (4,0 %), окклюзии периферических артерий (3,8 %), анемия (3,8 %), стенокардия (3,3 %), снижение количества тромбоцитов (3,1 %), фебрильная нейтропения (2,9 %), артериальная гипертензия (2,9 %), ишемическая болезнь сердца (2,7 %), застойная сердечная недостаточность (2,4 %), нарушение мозгового кровообращения (2,4 %), сепсис (2,4 %), флегмона (2,2 %), острая почечная недостаточность (2,0 %), инфекция мочевыводящих путей (2,0 %) и повышение активности липазы (2,0 %). Выраженные окклюзии артерий сердца, головного мозга и периферических артерий на фоне терапии препаратом были зарегистрированы у 10 %, 7 % и 9 % пациентов, соответственно. Выраженные венозные тромбоэмболии на фоне терапии отмечали у 5 % пациентов. В целом, окклюзии артерий регистрировали у 25 % пациентов, получавших препарат в рамках исследования 2 фазы, при этом серьезные нежелательные реакции были зафиксированы у 20 % пациентов. Окклюзии артериальных сосудов отмечались чаще при повышении возраста пациента, а также у пациентов, имевших в анамнезе ишемию, артериальную гипертензию, сахарный диабет или гиперлипидемию.
По результатам клинических испытаний нилотиниб, дазатиниб и бозутиниб имеют сопоставимую терапевтическую эффективность [50–53]. Сравнительные исследования эффективности применения ИТК2 в первой линии терапии ХМЛ, по сравнению с иматинибом, показали более быстрое достижение ответов при использовании ИТК2. В исследовании ENESTnd применение нилотиниба позволило через два года терапии достичь БМО у 67–71 % больных в сравнении с 44 % больных в группе иматиниба [54, 55]. Сравнение дазатиниба с иматинибом в первой линии также показало преимущество в достижении БМО к 2 годам лечения: у 64 % больных, получавших дазатиниб и у 46 % больных на терапии иматинибом [56, 57].
Применение ИТК2 в качестве второй линии терапии ХМЛ оказалось эффективным как при непереносимости, так и при резистентности к иматинибу. По результатам исследования нилотиниба у 172 пациентов в ХФ ХМЛ при резистентности или непереносимости иматиниба БЦО был достигнут у 59 % больных, при этом ПЦО наблюдался у 44 % пациентов [58]. Применение дазатиниба во второй линии терапии у 186 больных в ХФ ХМЛ при непереносимости или резистентности к иматинибу позволило добиться БЦО у 59 % больных, при этом у 49 % больных цитогенетический ответ был полным [59, 60]. Использование дазатиниба в ФА и БК позволило достичь БЦО у 25 % больных [61–63]. Бозутиниб также является эффективным при неудаче терапии иматинибом: из группы 288 больных ХМЛ к двум годам терапии 53 % больных достигли БЦО, в том числе БМО наблюдался у 26 % пациентов [64]. Результаты исследования BFORE сравнения с иматинибом показали, что БМО к 12 месяцам терапии был достигнут у 47.2 % при лечении бозутинибом и у 36,9 % в группе иматиниба, ПЦО был получен у 77,2 % при использовании бозутиниба и у 66,4 % пациентов, получавших иматиниб [53].
Выбор препарата для терапии хронического миелолейкоза
Необходимо отметить, что абсолютных противопоказаний для использования любого препарата ингибиторов тирозинкиназ нет. При выборе конкретного препарата для назначения больному ХМЛ необходимо учитывать фазу заболевания, сопутствующую патологию и риск развития побочных эффектов в процессе терапии, а также спектр мутаций гена BCR::ABL.
Терапия ИТК должна назначаться с учетом относительных противопоказаний, обусловленных сопутствующими заболеваниями для каждого из ИТК:
• нилотиниб: панкреатит, декомпенсированный сахарный диабет, окклюзионная болезнь периферических артерий и ишемические поражения сосудов [65, 66];
• дазатиниб: декомпенсированные сердечно-сосудистые заболевания, хронические заболевания легких, аутоиммунные нарушения, желудочно-кишечные кровотечения в анамнезе [67–69];
• бозутиниб: тяжелое нарушение функции печени и почек [45].
• понатиниб [47]: инфаркт миокарда, инсульт в анамнезе или процедура реваскуляризации; тяжелая или очень тяжелая гипертриглицеридемия; печеночная недостаточность; тяжелая почечная недостаточность; наличие вирусного гепатита В (HBV); панкреатит и злоупотребление алкоголем в анамнезе; одновременное применение с умеренными и мощными ингибиторами CYP3A и умеренными и мощными индукторами CYP3A; одновременное применение с препаратами, снижающими свертываемость крови, у пациентов с повышенным риском геморрагических осложнений; наследственная непереносимость лактозы, дефицит лактазы и глюкозо-галактозной мальабсорбцией.
Все ИТК следует применять с осторожностью у пациентов с удлиненным интервалом QT, а также с клинически выраженной сердечной недостаточностью, дисфункцией левого желудочка, аритмиями.
Мутации тирозинкиназного домена BCR::ABL
Исследование на предмет выявления мутаций BCR::ABL в момент диагностики следует проводить только больным с ФА и БК. При неэффективности или недостаточном ответе на терапию первой и последующих линий выполнение анализа на мутации в гене BCR::ABL является обязательным во всех случаях [15, 19]. Наиболее частые точечные мутации BCR::ABL и чувствительность их к воздействию ИТК приведены в табл. II-5 [41].
Таблица II-5. Мутации BCR::ABL и чувствительность к ИТК

Различные мутации придают разную чувствительность опухолевым клеткам к конкретным ИТК. Современные рекомендации по тактике действий при выявлении конкретных мутаций гена BCR::ABL следующие (табл. II-6).
Таблица II-6. Тактика действий при выявлении резистентных мутаций BCR::ABL [16]

* данные относительно чувствительности к бозутинибу при мутациях BCR::ABL ограничены, по некоторым данным in vivo мутации E255K и в меньшей степени E255V могут быть плохо чувствительны к бозутинибу [16].
Терапия всеми ИТК первого и второго поколения (иматиниб, нилотиниб, дазатиниб, бозутиниб) неэффективна при наличии мутации T315I. При выявлении данной мутации ранее было однозначно показано прекращение терапии ИТК, поиск HLA-идентичного донора и выполнение алло-ТКМ. В настоящее время препаратом, при применении которого показана возможность получения цитогенетических и молекулярных ремиссий у части больных ХМЛ с мутацией T315I, является понатиниб (Айклусиг, Iclusig®), в исследовании PACE у пациентов с ХФ ХМЛ и мутацией T315I БЦО был достигнут у 72 %, ПЦО у 70 %, БМО у 58 %, МО4 у 45 %, МО4,5 у 38 %, что даже превышало вероятность достижения ответов у пациентов без мутации T315I [70]. В качестве сдерживающей терапии также используются гидроксимочевина, курсы малых доз цитозара, курсы полихимиотерапии, интерферонотерапия. Проведенное в РФ исследование сравнения использования при выявлении мутации T315I сдерживающей терапии и алло-ТКМ показало отсутствие существенных различий в общей выживаемости [71]. Таким образом, при выявлении мутации T315I наиболее целесообразно использование понатиниба, если же это невозможно, то необходима оценка рисков и доступности проведения алло-ТКМ. При высоких рисках летальности при трансплантации проведение сдерживающей терапии является разумной альтернативой.
Мониторинг и оценка эффективности терапии хронического миелолейкоза
Для оценки эффективности терапии необходимо проводить своевременный мониторинг гематологических, цитогенетических и молекулярно-генетических показателей (таблица II-7) [15, 19, 33]. Для раннего выявления возможной токсичности терапии показан также регулярный физикальный осмотр, мониторинг биохимических показателей крови, ЭКГ.
Таблица II-7. Частота динамического обследования больных ХМЛ, получающих ИТК [15, 19, 33]

Последние рекомендации ELN2020 рекомендуют проведение только молекулярного мониторинга, при наличии атипичного транскрипта BCR::ABL рекомендуется использование FISH [16]. Однако, полный отказ от проведения цитогенетического мониторинга представляется необоснованным. Таким образом будут пропущены дополнительные (ДХА, в Ph+) и другие хромосомные аберрации (в Ph-) клетках, которые могут иметь прогностическое значение.
Результаты терапии у больных ХМЛ оцениваются по данным гематологического, цитогенетического и молекулярного методов исследования (таблица II-8). В зависимости от степени подавления опухолевого клона выделяют различные виды ответа [15, 19, 33].
Таблица II-8. Виды ответа на терапию при ХМЛ [15, 19, 33]

1 В случае, если стандартное цитогенетическое исследование (СЦИ) неинформативно, определение полного цитогенетического ответа может быть основано на результатах FISH (анализ не менее 200 ядер) при этом количество клеток, несущих химерный ген не должно превышать 1 %.
2 Для стандартизации результатов необходим пересчет каждого результата в международную шкалу (IS). С целью исключения внутрилабораторной вариабельности изменение уровня BCR::ABL менее чем на 1 log нуждается в подтверждении при повторном анализе.
Оценка ответа на таргетную терапию ИТК первой и второй линии больных в ХФ ХМЛ в соответствии с рекомендациями ELN2020 приведены в табл. II-9 [16].
Таблица II-9. Рекомендации по оценке ответа на терапию ИТК первой и второй линии больных в ХФ ХМЛ [16]

* ДХА – Дополнительные хромосомные аберрации
Рекомендации по лечению больных ХМЛ в ХФ с использованием ИТК в первой и второй линиях терапии ХМЛ представлены в табл. II-10 [15, 19]. Рекомендации по тактике лечения ХМЛ при использовании только молекулярного мониторинга приведены в табл. II-11 [17].
Таблица II-10. Рекомендации по лечению больных в хронической фазе ХМЛ в зависимости от длительности и характера ответа на терапию ИТК в первой и второй линиях лечения [15, 19]




1 При наличии факторов предупреждения у больных, получающих ИТК2 в первой линии возможно увеличение дозы нилотиниба до 800 мг/сут, дазатиниба до 140 мг/сут.
2 При неудаче терапии иматинибом предпочтительней смена терапии на ИТК2, чем повышение дозы иматиниба. При отсутствии ПГО показана смена терапии. При наличии факторов предостережения (высокая группа риска Sokal, ДХА в Ph+ клетках) предпочтительнее смена терапии. При наличии возможности больных с неудачей терапии целесообразно включать в клинические исследования новых методов экспериментальной терапии ХМЛ.
3 При выполнении только молекулярного анализа рекомендуется повторное исследование в течение 1–2 месяцев для подтверждения результата.
4 В двух последующих определениях, в одном из которых уровень BCR::ABL ≥ 1 %.
Таблица II-11. Тактика терапии пациентов в хронической фазе ХМЛ при использовании только молекулярного мониторинга в зависимости от уровня экспрессии BCR::ABL (IS) и длительности терапии [17]

При недостаточной эффективности или непереносимости терапии первой линии при выборе ИТК для смены терапии необходимо учитывать анамнез лечения, в том числе наблюдавшиеся побочные эффекты, сопутствующую патологию, результаты определения мутационного статуса BCR::ABL. При неудаче терапии иматинибом необходима смена терапии на ИТК2. Повышение дозы иматиниба до 600–800 мг/сут может являться только временной мерой в условиях ограниченного доступа к ИТК2.
При неудаче лечения первой и второй линии четких рекомендаций по ведению больных, получающих последующие линии терапии, нет. В рекомендациях ELN2020 четких определений оптимального ответа или неудачи терапии нет. Указано, что уровень BCR::ABL>1 % или цитогенетический ответ менее чем полный (Ph>0 %) являются недостаточными для оптимальной выживаемости [16].
При неудаче двух линий терапии, а также при прогрессировании в продвинутые фазы на фоне терапии ИТК вопрос о выполнении алло-ТКМ необходимо решать незамедлительно, так как этот метод является единственным, способным в этой ситуации дать шанс на длительную безрецидивную выживаемость.
Лечение больных ХМЛ в продвинутых фазах заболевания (ФА и БК) имеет свои особенности (табл. II-12). Необходимо применение максимальных доз ИТК, возможно сочетание ИТК и химиотерапии. Первоочередной задачей является перевод заболевания в хроническую фазу и достижение максимально возможного эффекта терапии. При возможности необходимо проведение алло-ТКМ.
Таблица II-12. Рекомендации по лечению больных ХМЛ в фазах акселерации и бластного криза [15, 19]

Показанием к проведению аллогенной трансплантации костного мозга или гемопоэтических стволовых клеток периферической крови (алло-ТКМ) у больных в ХФ ХМЛ является резистентность ко второй линии терапии ИТК, выявление мутации T315I. Пациентам в ФА и БК ХМЛ рекомендуется проведение алло-ТКМ от родственного либо неродственного донора сразу после достижения второй ХФ на фоне ИТК и/или сочетания ИТК с химиотерапией [15, 19]. Общие рекомендации по показаниям к проведению HLA-типирования, поиску донора и выполнению алло-ТКМ приведены в таблице II-13.
Таблица II-13. Показания к HLA-типированию, поиску донора и проведению аллогенной трансплантации костного мозга / гемопоэтических стволовых клеток при ХМЛ [15, 16, 19]

1 Рекомендации применимы к больным, которые по возрасту и функциональному состоянию являются кандидатами для проведения алло-ТКМ.
2 Факторы риска при алло-ТКМ общества EBMT [72]:
• хроническая фаза 0 баллов, фаза акселерации 1 балл, бластный криз 2 балла;
• возраст менее 20 лет 0 баллов, 20–40 лет 1 балл, более 40 лет 2 балла;
• время от постановки диагноза до Алло-ТКМ менее 1 года 0 баллов, более 1 года 1 балл;
• HLA-идентичный сиблинг 0 баллов, другие доноры 1 балл;
• пара донор-женщина реципиент-мужчина 1 балл, 0 баллов для других сочетаний донор-реципиент.
Современное медикаментозное лечение больных ХМЛ является высокоэффективным у подавляющего большинства больных. Имеющиеся рекомендации по контролю нежелательных явлений ИТК и возможность альтернативного выбора препаратов позволяет практически полностью сохранить физическое состояние и повседневный уровень активности больного.
Для сохранения принципа максимального и постоянного воздействия на опухолевый клон важно свести к минимуму побочные эффекты терапии, учитывая небходимость длительного приема препаратов.
Побочные эффекты лечения хронического миелолейкоза и методы их коррекции
Токсичность терапии на фоне применения ИТК можно разделить на гематологическую и негематологическую. Общие рекомендации по коррекции нежелательных явлений при лечении ХМЛ приведены ниже [73].
Гематологическая токсичность
Частым побочным эффектом лечения ИТК является снижение показателей крови. Анемия любой степени во всех фазах ХМЛ не является показанием к прерыванию терапии ИТК. Необходимо дополнительное обследование пациента для исключения других причин анемии, с учетом клинической ситуации (анализ крови на обмен железа, фолаты, витамин В12, гемолитические тесты и др.). При клинически значимых проявлениях анемического синдрома показаны заместительные трансфузии эритроцитной массы.
При нейтропении и тромбоцитопении 1–2 степени в любой фазе ХМЛ снижения дозы ИТК и перерывов в лечении не требуется. В ХФ ХМЛ при нейтропении и/или тромбоцитопении 3–4 степени показана временная отмена ИТК с контролем клинического анализа крови один раз в неделю. После восстановления абсолютного числа нейтрофилов до уровня более 1,0 × 109/л, тромбоцитов более 50 × 109/л необходимо возобновить терапию ИТК:
• если перерыв в лечении составлял менее 2 недель, то терапия возобновляется в прежней дозе, при перерыве более 2 недель – в сниженной на один уровень дозе (см. табл. 4 – дозы ИТК);
• если доза ИТК ранее была снижена, при стабильных показателях гемограммы через 1 месяц целесообразно возвращение к стандартной дозировке;
• при длительных нейтропениях возможно кратковременное применение гранулоцитарного колониестимулирующего фактора (Г-КСФ): филграстим в дозе 5 мкг/кг/сут подкожно, при отсутствии эффекта от введения Г-КСФ необходима редукция дозы или смена ИТК;
• при длительных повторных цитопениях необходимо провести обследование (миелограмма, гистологическое исследование костного мозга) с целью исключения прогрессирования заболевания, развития фиброза костного мозга.
В ФА и БК ХМЛ даже при наличии нейтропении и тромбоцитопении 3–4 степеней с целью индукции ремиссии в течение первых 4 недель терапия ИТК не должна прерываться. При тромбоцитопении 3–4 степени, геморрагическом синдроме показаны трансфузии тромбоцитного концентрата. Определенную пользу для продолжения терапии ИТК, при коррекции тромбоцитопении 3–4 степени, не обусловленной прогрессированием заболевания может принести введение агонистов рецепторов тромбопоэтина [73]. Следует отметить, что показание для использования данных препаратов в настоящее время официально не зарегистрировано и должно осуществляться только при наличии жизненных показаний для купирования тромбоцитопении с целью продолжения терапии ИТК. Если миелосупрессия сохраняется после 1 месяца терапии, то необходимо выполнение стернальной пункции с подсчетом миелограммы для исключения прогрессирования заболевания:
• при числе бластов менее 5 % и снижении клеточности костного мозга следует прервать терапию; контроль клинического анализа крови проводить не реже 1 раза в неделю; возобновить терапию после восстановления абсолютного числа нейтрофилов более 0,5х109/л и тромбоцитов более 50х109/л; при повторном возникновении миелосупрессии доза ИТК должна быть снижена; при длительных и/или повторных эпизодах нейтропении и отсутствии бластоза в периферической крови и костном мозге возможно применение Г-КСФ;
• при наличии более 5 % бластов и гиперклеточном костном мозге должен быть обсужден вопрос об изменении тактики терапии:
– при терапии иматинибом переход на терапию ИТК2;
– при терапии ИТК2 смена препарата;
– проведение другого вида терапии (химиотерапия, экспериментальное лечение).
Негематологическая токсичность
Помимо гематологической токсичности терапия ИТК может осложняться и другими побочными эффектами, связанными лишь с относительной селективностью ИТК и возможностью влияния на широкий спектр тирозинкиназ, регулирующих различные процессы жизнедеятельности организма. Наиболее частыми побочными эффектами лечения ИТК являются тошнота, рвота, диарея, задержка жидкости с развитием отеков, кожная сыпь, зуд, слабость, нарушения сна, боли в мышцах и суставах. Особенное значение данные побочные явления приобретают в связи с необходимостью постоянного приема препаратов ИТК. Даже небольшая выраженность постоянно существующих побочных эффектов может приводить к снижению приверженности к лечению (комплаентности) – пропускам приема либо снижению дозы препарата пациентами, что ведет к снижению эффективности терапии.
Общая тактика ведения больных при различных проявлениях негематологической токсичности на фоне ИТК представлена в табл. II-14. Перерывы в лечении и снижение дозы допустимы при длительных и/или повторных эпизодах токсичности 2 степени и при однократной токсичности 3–4 степени. Непереносимость терапии ИТК возможно констатировать при длительном (более 2–3 мес.) сохранении явлений токсичности 2 ст. при условии адекватной сопроводительной терапии, а также при повторных явлениях токсичности 3–4 степени. Непереносимость терапии является показанием к переводу на другой ИТК, так как профиль негематологической токсичности у препаратов разный, и перекрестная непереносимость минимальная.
Таблица II-14. Общая тактика терапии при негематологической токсичности ИТК

Одним из наиболее актуальных дополнений последних версий рекомендаций по диагностике и лечению ХМЛ является включение раздела, посвященного методике ведения пациентов ХМЛ в ремиссии без лечения (РБЛ). В этот период у пациентов с длительным глубоким молекулярным ответом (ГМО) отменяется прием препаратов – ингибиторов тирозинкиназ и больной остается только под частым молекулярным мониторингом минимальной остаточной болезни. В случае повышения уровня экспрессии BCR::ABL более порогового значения, обычно МО4,0 или БМО, таргетная терапия возобновляется.
В настоящее время уже накоплено достаточно результатов клинических исследований возможной отмены терапии у больных со стойким длительным глубоким молекулярным ответом – ведение ремиссии ХМЛ без лечения [74–77]. Успешные результаты этих исследований, в том числе подтвержденные и в отечественных работах [78], в виде сохранения ответа у большой части (39–67 %) пациентов при крайне низком риске прогрессирования заболевания сделали возможным включение данного раздела в клинические рекомендации.
Условия для включения пациентов в ХМЛ в РБЛ в соответствии с рекомендациями ELN2020 следующие [16].
• Обязательные:
– первая хроническая фаза;
– мотивированный пациент с хорошей коммуникацией;
– доступ к высококачественной ПЦР с использованием Международной шкалы (IS) с быстрым получением результатов;
– согласие пациента на более частый мониторинг после прекращения лечения, ежемесячно в течение первых 6 месяцев, каждые 2 месяца в течение 6–12 месяцев, затем каждые 3 месяца.
• Минимально допустимые:
– первая линия терапии, вторая линия только в случае непереносимости первой линии терапии;
– типичные транскрипты BCR::ABL e13a2 или e14a2;
– продолжительность терапии ИТК >5 лет (>4 лет для ИТК2);
– продолжительность глубокого молекулярного ответа (МО4.0 или лучше) >2 лет.
• Оптимальные:
– продолжительность терапии ИТК >5 лет;
– продолжительность глубокого молекулярного ответа >3 лет, если МО4.0;
– продолжительность глубокого молекулярного ответа >2 лет, если МО4.5.
Оценка возможности применения методики РБЛ в клинической практике по рекомендациям NCCN приведена в табл. II-15 [17].
Таблица II-15. Возможность применения РБЛ в клинической практике (рекомендации NCCN) [17]

Все зеленый свет: рекомендация рассмотреть отказ от терапии ИТК.
Любой желтый свет: отказ от терапии ИТК рассмотреть только при очень значимых обстоятельствах (например, значительная токсичность или планируемая беременность.
Любой красный свет: отмена ИТК не рекомендована, исключая клиническое исследование.
Краеугольным камнем методики РБЛ является частый молекулярный мониторинг экспрессии BCR::ABL:
• ежемесячно в течение первых 6 месяцев;
• каждые 2 месяца в течение 6–12 месяцев;
• затем каждые 3 месяца.
Интересным побочным эффектом отмены терапии ИТК являются мышечные боли, наблюдающиеся у 20–30 % пациентов после прекращения приема ИТК. Предполагается, что возникновение данного побочного эффекта связано с дисбалансом цитокинов и носит временный характер. Однако выраженность болей у некоторых пациентов требовала возобновления приема ИТК.
Потеря БМО при молекулярном мониторинге, подтвержденная в двух последовательных исследованиях является показанием к возобновлению терапии тем же самым ИТК, который пациент принимал до включения в РБЛ.
Беременность и отцовство
В соответствии с инструкциями по применению ИТК, беременность является противопоказанием к терапии. Всем пациентам, принимающим ИТК, показана эффективная контрацепция.
Пациенткам, планирующим беременность, необходимо быть информированными о потенциальном тератогенном действии иматиниба; мало изученном действии ИТК2 при беременности и описанном эмбриотоксическом действии; вероятности самопроизвольного прерывания беременности; возможности рецидива ХМЛ при отмене терапии на период беременности даже при наличии ПМО; небольшом количестве наблюдений случаев беременности при ХМЛ.
В рекомендациях ELN2020 включен раздел, посвященный беременности и отцовству больных ХМЛ [16]. Риск генотоксичности для мужчин при приеме иматиниба, нилотиниба, дазатиниба и бозутиниба признан низким, прекращения приема препаратов во время планирования отцовства не требуется.
Для женщин рекомендации по впервые выявленному ХМЛ во время беременности должны быть индивидуальными. При наличии продвинутых фаз ХМЛ – прерывание беременности. Все ИТК противопоказаны во время беременности, хотя иматиниб безопасно использовался во время второго и третьего триместра беременности.
Требования к женщинам, планирующим беременность, такие же, как и при использовании методики ремиссии без лечения. При потере БМО, но сохранении ПЦО, во время беременности имеется вероятность продолжения наблюдения до родов без необходимости возобновления лечения. Женщины, потерявшие БМО, но не забеременевшие должны возобновить лечение, возможно более активным ИТК, для достижения более устойчивого ответа для повторной попытки отмены и беременности.
У женщин, планирующих беременность и не имеющих глубокого молекулярного ответа лечение может быть заменено на интерферон-альфа или могут быть рассмотрены альтернативные методы беременности.
С терапевтической целью у пациенток с ХМЛ и беременностью могут использоваться антиагреганты (ацетилсалициловая кислота) и/или низкомолекулярные гепарины при тромбоцитозе. Лейкаферез и препараты интерферона-альфа расцениваются как относительно безопасные во время беременности. Вскармливание противопоказано при приеме ИТК.
В рамках научно-исследовательской работы нами была разработана программа диагностики и лечения ХМЛ, включающая методику РБЛ.
Особенностью разработанной программы лечения ХМЛ было использование раннего переключения между линиями таргетной терапии при отсутствии оптимального ответа на таргетную терапию.
Для оптимального ответа на первую линию терапии ИТК необходимо наличие:
• ПГО в течение первых 3 месяцев;
• ПЦО в течение первых 6 месяцев;
• БМО в течение первых 12 месяцев.
Для соответствия оптимальному ответу второй линии терапии ИТК считали необходимым достижение:
• на 3 месяца лечения раннего молекулярного ответа (BCR::ABL ≤ 10 %) и / или малого цитогенетического ответа (Ph+ <65 %, МЦО);
• на 6 месяцев лечения раннего молекулярного ответа BCR::ABL ≤ 10 % и / или частичного цитогенетического ответа (Ph+ ≤35 %, ЧЦО);
• на 1 год лечения BCR::ABL ≤ 1 % и / или полного цитогенетического ответа (Ph+ 0 %, ПЦО);
• в любое время после года терапии достижение БМО (на 3 месяца терапии достижение раннего молекулярного ответа (BCR::ABL ≤ 0,1 %).
В обычной практике смена терапии проводится при констатации неудачи терапии. Во вновь разработанной программе переключение между линиями лечения проводится при отсутствии оптимального ответа, то есть у больных с неудачей терапии и у пациентов с наличием факторов предостережения. Таким образом, доля пациентов, которым проводится смена терапии существенно увеличивается.
В общем виде разработанная программа лечения представлена на рисунке II-2.
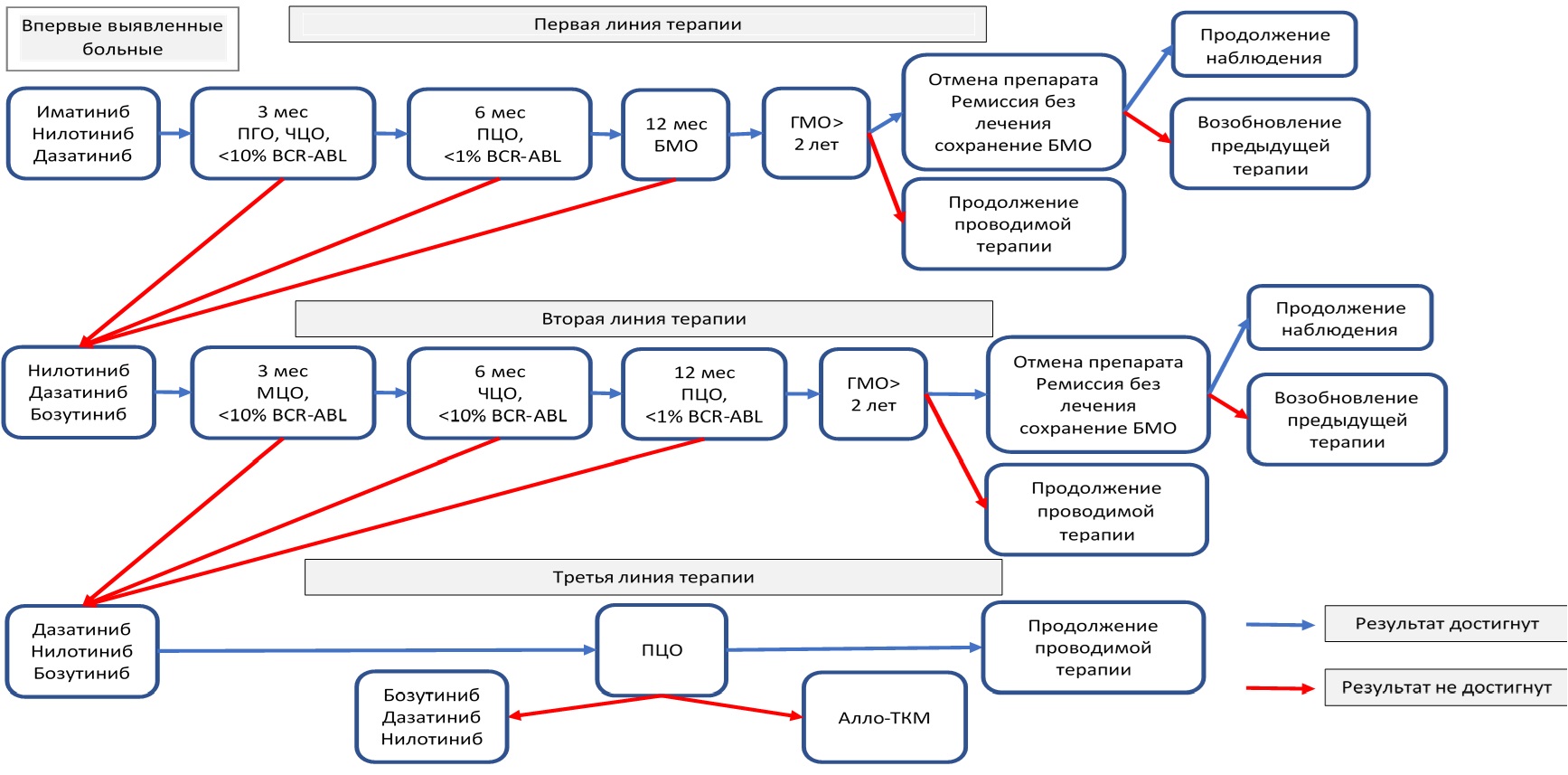
Рисунок II-2. Программа лечения ХМЛ с методикой ведения больных в фазе ремиссии без использования ингибиторов тирозинкиназ (ремиссии без лечения).
При достижении продолжительного (не менее 3 лет) стабильного глубокого молекулярного ответа (МО4,0 и глубже) больные ХМЛ могли быть переведены в режим без лечения (РБЛ).
В этом случае лечение ИТК прекращалось и проводился мониторинг уровня BCR::ABL с момента прекращения приема ИТК по следующей схеме: в течение первых 6 месяцев 1 раз в месяц; в течение второй половины первого года (с 7-го до завершения 12 месяца) 1 раз в 1,5 месяца; затем 1 раз в 3 месяца.
При повышении относительного уровня BCR::ABL/ABL более 0,1 % терапия ИТК возобновлялась с периодическим контролем BCR::ABL не реже чем в 3 месяца до повторного достижения и подтверждения БМО, затем 1 раз в 6 месяцев при его сохранении. Нами была проведена апробация разработанной программы и фармакоэкономическая оценка её эффективности.
Всего в исследование было включено 307 пациентов с диагнозом ХМЛ. Группа сравнения (исторического контроля) состояла из 216 больных, 91 пациент был включен в группу исследования. Результаты первичной диагностики приведены в таблице II-16.
Диагностика и лечение пациентов в группе исследования проводилось по вновь разработанной программе. Всем больным после установления диагноза назначались ингибиторы тирозинкиназ: первого поколения – иматиниб 79 (87 %) пациентам и второго поколения – нилотиниб 9 (10 %) и дазатиниб 3 (3 %) больным. Для анализа эффективности таргетной терапии в группе сравнения использовались только результаты лечения пациентов, получавших ингибиторы тирозинкиназ.
Таблица II-16. Клинические показатели пациентов с ХМЛ на момент первичной диагностики

* сравнение между частотами ХФ и ФА+БК, **сравнение между частотами низкая+промежуточная и высокая
Группы пациентов значимо различались по срокам от установления диагноза до начала таргетной терапии: медиана составила 2,0 месяца для группы сравнения и 0,5 месяца для группы исследования.
Вторая линия терапии проводилась в группе сравнения 76 больным (нилотиниб – 54, дазатиниб – 19, бозутиниб – 2, иматиниб – 1); в группе исследования 46 пациентам (нилотиниб – 26, дазатиниб – 19, иматиниб – 1).
Сроки от установления диагноза до начала таргетной терапии второй линии статистически значимо различались между группами: медиана составила 49,5 месяцев для группы сравнения и 8,0 для группы исследования.
Третья линия таргетной терапии была использована в группе сравнения у 32 больных (нилотиниб – 6, дазатиниб – 25, бозутиниб – 1); в группе исследования у 19 пациентов (нилотиниб – 1, дазатиниб – 10, бозутиниб – 5, понатиниб – 3). Сроки от установления диагноза до начала таргетной терапии третьей линии статистически значимо различались между группами: медиана составила 81,3 месяца для группы сравнения и 26,4 месяцев – для группы исследования.


