
Марат Зиявдинович Саидов
Клеточные и молекулярные механизмы патогенеза иммуновоспалительных ревматических заболеваний
1.3. ГЗТ-гранулёмы
По определению “гранулёма – это компактная (организованная) совокупность зрелых, активированных мононуклеарных фагоцитов и лимфоцитов, которая необязательно сопровождается дополнительными признаками, такими как некроз” и далее “гранулёма отличается от хронического воспалительного инфильтрата характерной организацией зрелых макрофагов в компактную структуру”. Макрофаги приобретают вид “эпителиоидных” клеток, которые в силу невыясненных причин могут организовываться в гигантские, многоядерные клетки по типу гигантских клеток Лангханса. Можно сказать, что гранулёмы при ИВРЗ являются выражением иммунологической активности КВИ [63,116].
Несмотря на то, что история изучения гранулём и гранулематозного воспаления насчитывает более 150 лет, патофизиологический и иммунологический смысл этой структуры осознан не до конца. Считается, что, в целом, предназначение гранулём – это защита от внутриклеточных патогенов и отграничение очага гранулематозного воспаления. Однако идентифицировать этиологически важный патогенный агент в ревматических гранулёмах не удаётся. Гранулёмы при ИВРЗ относят к клеточной гиперергической реакции врождённого и адаптивного иммунитета, вбирающие в себя признаки продуктивного воспаления in situ. Гранулёмы, или узелки, сравнивают с обоюдоострым мечом, влияющим как на элиминацию этиологического агента, так и на тканевую деструкцию [168].
Кандидатными триггерами ревматических гранулём и аутоиммунного ответа могут быть продукты дезорганизации соединительной ткани, в частности, очаги фибриноидного некроза. На рис. 10 представлена патоморфологическая картина ревматоидного узелка при ревматоидном артрите (слева), а также гранулёмы в миокарде при ревматической лихорадке. Видно, что мононуклеарные клетки, прежде всего, клетки макрофагально-моноцитарного ряда и лимфоциты в составе КВИ, четко располагаются вокруг очагов фибриноидного некроза.
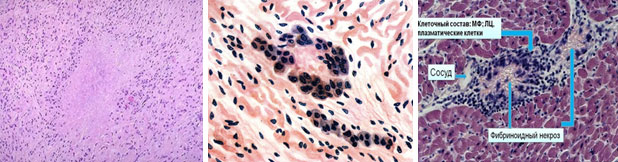
Рис. 10. Слева ревматоидный узелок (Х100). Справа два снимка гранулёмы в миокарде при ревматической лихорадке. В центре гранулём продукты распада основного вещества соединительной ткани, вокруг мононуклеарная инфильтрация (Х200), по материалам [14]
Характерной чертой формирования гранулематозного воспаления при ИВРЗ является присутствие признаков гиперергического клеточного иммунного ответа, или, иными словами, гиперчувствительности замедленного типа (ГЗТ), в которой центральная роль принадлежит клеткам макрофагально-моноцитарного ряда. К признакам ГЗТ при гранулематозном воспалении при ИВРС относят активированное состояние клеток в составе гранулём, их компактное расположение, обеспечивающие межклеточные контакты, прежде всего, макрофагально-лимфоцитарные, трансформация макрофагов в эпителиоидные клетки, продукция широкого спектра провоспалительных цитокинов, провоспалительных хемокинов, ростовых факторов, факторов ангиогенеза, интерферонов. Именно поэтому этот тип гранулём носит название ГЗТ-гранулём.
Этапность формирования ГЗТ-гранулём и клеточный состав определяет спектр провоспалительных хемокинов, источниками которых являются активированные клетки макрофагально-моноцитарного ряда, Т-лимфоциты, эндотелиоциты. В составе гранулём находят макрофаги (CD68+), моноциты (CD14+), Т-лимфоциты (включая CD4+Th1, CD4+Th17, CD8+), плазмацитоидные и миелоидные дендритные клетки (CD205+), В-лимфоциты, естественные киллеры (CD56+), нейтрофилы, эозинофилы [114,116]. Находящиеся в очаге гранулематозного воспаления антиген-специфические CD4+клетки дифференцируются в Th1 CD4+субпопуляцию – эффекторов ГЗТ, с последующей продукцией провоспалительных цитокинов IL-1α, IL-1β, IL-6, IL-4, IL-12, TNF-α, IFN-γ, провоспалительных хемокинов – IL-8, СС-хемокинов, хемоаттрактантного моноцитарного белка 1 (МСР-1), макрофагального воспалительного протеина 1α (MIP-1α), иммунорегуляторных цитокинов – IL-10, IL-12, а также матриксных металлопротеиназ (ММР1–9), витронектина, остеопорина, фибронектина. В продукции указанных растворимых факторов активное участие принимают Мф, ДК и гигантские клетки [102,103].
Подобный широкий хемо-цитокиновый спектр обеспечивает дополнительное привлечение провоспалительных клеток in situ. Стимулом для дифференцировки CD4+клеток в направлении Th1 является продукция клетками макрофагально-моноцитарного ряда IL-12 и IL-18, а также продукция естественными киллерами IFN-γ [74,84].
Подчеркнём важное качество ГЗТ-гранулём. Речь идёт о том, что описанная выше последовательность дезорганизации соединительной ткани сопровождается сопряжённой клеточной реакцией и на этапе фибриноидных измненений и фибриноидного некроза эта клеточная реакция может приобретать вид ГЗТ-гранулём. Участки дезорганизации соединительной ткани одновременно служат источником ауто-АГ. Заметно усиливаются АГ-зависимые контакты Мф с лимфоцитами. Наиболее ярко эти процессы представлены в гранулёмах Ашофа-Талалаева при ревматической лихорадке. Тот факт, что клетки макрофагально-моноцитарного ряда, в типичном выражении, веерообразно располагаются вокруг центрального участка фибриноидного некроза, подчёркивает возможность контакта АПК с продуктами дезорганизации соединительной ткани с потенциально ауто-АГ свойствами.
Сказанное иллюстрируется картиной гранулёмы Ашоффа-Талалаева при ревматическом миокардите, представленной на рис. 11, где определяются крупные гиперхромные (активированные) макрофаги, а также лимфоциты, располагающиеся вокруг и в очагах фибриноидного некроза.
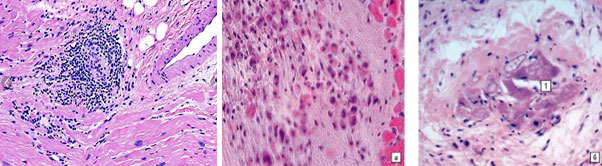
Рис. 11. Гранулёма Ашоффа-Талалаева при ревматическом миокардите. Видны крупные гиперхромные макрофаги, лимфоциты, очаги фибриноидного некроза (Х200), по материалам [14]
На Мф и ДК в очагах иммунного гранулематозного воспаления существенно возрастает экспрессия аллелей локусов МНС II класса – HLA-DR, HLA-DQ, HLA-DP, а также маркера CD205, Одновременное присутствие пролиферирующих Т-лимфоцитов формирует возможность индукции аутоиммунного ответа in situ. В качестве иллюстрации сказанного приводим снимки препаратов иммунных гранулём при болезни Крона. На рис. 12 видны четкая компактная локализация CD205+ клеток в центре иммунных гранулём. CD205 – это мембранный маркёр, экспрессирующийся на активированных Мф и ДК. В этих же местах также четко визуализируются интрагранулематозные CD3+лимфоциты (зелёный цвет) в тесном контакте с CD205+ клетками (красный цвет). Причём CD3+лимфоциты являются пролиферирующими, что документируется по экспрессии маркёра клеточной пролиферации Ki67 [114].
Очевидно, что микроокружение в иммунных гранулёмах, межклеточные контакты создают благоприятные условия для аутоиммунного ответа in situ.
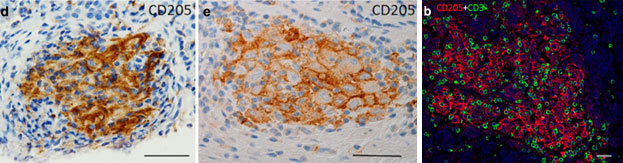
Рис. 12. Иммунные гранулёмы при болезни Крона. Иммуногистохимическая идентификация CD205+ клеток (d,e); CD3+лимфоциты (зелёный цвет) и CD205+макрофаги и дендритные клетки (красный цвет) в иммунной гранулёме, метод иммунофлуоресценции (b), по материалам [114]
Гранулёмы при ИВРЗ морфологически относят к эпителиоидным гранулёмам. Формирование таких компактных мононуклеарных инфильтратов обусловлено деятельностью активированных резидентных макрофагов и эмиграцией в очаг воспаления из посткапиллярных венул, выстланных “высокими“ эндотелиоцитами 2 типа, моноцитов, лимфоцитов, нейтрофилов [141].
Гранулёмы являются мобильной структурой, отражающей стадию воспаления и, в определённой степени, её нозологическую специфичность. Пул резидентных (тканевых) макрофагов на несколько порядков превышает их костномозговой резерв [6]. Формирование ГЗТ-гранулём является преимущественно местным процессом. Моноциты, Т- и В-лимфоциты гематогенного происхождения дополняют клеточный состав этих гранулём. Активация клеток макрофагально-моноцитарного гистогенеза в составе ГЗТ-гранулём – есть в т. ч. и повышение фагоцитарной активности этих клеток в отношении продуктов дезорганизации соединительной ткани с последующей возможностью выполнения АГ-презентирующей функции и индукцией аутоиммунного ответа.
Можно проследить и некоторую общность структурно-функциональной организации между упомянутыми выше фолликулоподобными (эктопическими) лимфоидными структурами (ELS) и ГЗТ-гранулёмами. Эта общность касается прежде всего, во-первых, идентичности клеточного состава, во-вторых, важной роли макрофагов и их производных в формировании этих патоморфологических структур, в-третьих, спектр продуцируемых провоспалительных цито- и хемокинов практически полностью совпадает, в-четвёртых, микроокружение и в том, и в другом случаях создаёт возможность индукции извращённого аутоиммунного ответа на собственные АГ-детерминанты. Если сравнить картину гранулёмы в миокарде при ревматической лихорадке, представленную слева на рис. 11 с картиной фолликулоподобной структуры в синовиальной оболочке при РА, представленной на рис. 6 и на рис. 7 слева, то очевидное сходство этих структур не вызывает сомнений. В процессах формирования ГЗТ-гранулём и прогрессировании воспалительного процесса также очевидно значение ангиогенеза in situ. В частности, показано, что пролиферация эндотелия капилляров совпадает во времени с пиком мононуклеарной инфильтрации при гранулематозном воспалении [144].
1.4. Адгезионные лиганд-рецепторные взаимодействия и эндотелиальная реакция при хроническом продуктивном воспалении
“Точкой отсчёта” формирования КВИ является сосудисто-эндотелиальная реакция в ответ на действие любого триггера, результатом которой является ангиогенгез. Ангиогенез – это биологический процесс, посредством которого образуются кровеносные сосуды. Этот процесс сопровождается развитием адгезионных межклеточных и клеточно-матриксных взаимодействий, продукцией и рецепцией цито- и хемокинов, эмиграцией клеток из кровотока и активацией резидентных клеток различного гистогенеза и функционального предназначения in situ. Очевидна тесная взаимосвязь и разнонаправленная взаиморегулируемость этих процессов, наиболее демонстративно представленная в виде провоспалительных, аддитивных, синегрических и ингибирующих эффектов цито- и хемокинов. В этих условиях создается микроокружение, благоприятствующее индукции процессов иммуногенеза.
В инициации КВИ значительная роль принадлежит активности эндотелиоцитов. Диапедез лимфоцитов, моноцитов, нейтрофилов, эозинофилов в очаг воспаления происходит преимущественно в области посткапиллярных венул, выстланных “высокими“ эндотелиоцитами 2 типа. Трансформации эндотелиоцитов в “высокий” эндотелий, в частности, способствуют продуцируемые активированными Т-лимфоцитами цитокины (IL-1α, IFN-γ, TNF-α и др.). Активированные эндотелиоциты экспрессируют спектр адгезионных молекул с различным функциональными свойствами. Лиганд-рецепторные взаимодействия между активированными эндотелиоцитами и клетками крови включают в себя десятки молекул, формируя по аналогии с иммунологическим синапсом – синапс эндотелиально-клеточный.
На активированных эндотелиоцитах экспрессируется следующий спектр адгезионных молекул, обепечивающих диапедез клеток крови в очаг воспаления, начиная с этапа прилипания и роллинга и заканчивая выходом клетки из сосудистого русла: селектины – Р-селектин (CD62P) и Е-селектин (CD62E); из иммуноглобулинового семейства – молекулы VCAM и их разновидности [VCAM-1(CD106), ELAM-1, ICAM-1(CD54), ICAM-2]; CD34 для рецепторов миелоидных клеток; муцин GlyCAM-1.
Рецепторами рециркуляции, или хоминг-рецепторами, на лимфоцитах для указанных молекул являются VLA-4 (CD49dCD29), LFA-1 (CD11a CD18), CD44. Кроме этого на лейкоцитах конститутивно экспрессированы L-селектины, рецепторы для Р- и Е-селектинов (PSGL-1). Основной интегрин лимфоцитов LFA-1, представлен и на поверхности моноцитов и макрофагов. Интегрин Мас-1 экспрессируется на Мф, а также на других миелоидных и NK-клетках. Третий интегрин этой группы – p150/р95 – маркер ДК, но он также представлен на других клетках миелоидного ряда. β1-интегрины (молекулы группы VLA) взаимодействуют с компонентами межклеточного матрикса (фибронектином, ламинином, коллагеном, фибриногеном) и мембранным рецептором VCAM-1 (CD106).
На активированном эндотелии экспрессируются:
VLA-1 (CD49a/CD29), его лиганды – коллаген I–V типов;
VLA-3 (CD49b/CD29), его лиганды – фибронектин, коллаген I–V типов, ламинин;
VLA-5 (CD49e/CD29), его лиганды – фибронектин, витронектин;
VLA-6 (CD49f/CD29), его лиганды – ламинин;
LPAM-1 (CD49d/X), его лиганды – фибронектин;
CD51/CD6, его лиганды – витронектин, фибриноген.
Также на активированном эндотелии экспрессируются рецепторы интегринов – ICAM-1 (CD54), ICAM-2 (CD102), VCAM-1 (CD106) [124, 133].
Таким образом, всё многообразие и специфичность адгезионных взаимодействий активированного эндотелия с клетками крови и межклеточным матриксом обеспечивает процесс эмиграции лейкоцитов из кровяного русла в очаг воспаления, что является важным фактором организации КВИ при ревматических заболеваниях.
Не менее важным фактором организации КВИ и межклеточных взаимодействий in situ является экспрессия на активированных эндотелиоцитах аллелей МНС II класса. Показано, что под влиянием IFN-γ на эндотелиоцитах в воспалительном очаге алелли HLA-DR экспрессируются на повышенном уровне, тем самым создавая условия для презентации антигенного материала и инициации аутоиммунного ответа [77].
Патогенез ХПВ неразрывно связан с реализацией разнонаправленной функциональной активности спектра провоспалительных цито- и хемокинов, продуцируемых как клетками воспалительного инфильтрата, так и доставляемых гематогенным и лимфогенным путём. Основными цитокинам, влияющим на функции эндотелиоцитов при ХПВ, являются IL-1α, IL-1β, IL-6, TNF-α TNF-β, IFN-α, IFN-β, IFN-γ, трансформирующий фактор роста β (TFG-β). К некоторым из них (IL-1β и TNF-α) эндотелиоциты конститутивно экспрессируют рецепторы. Под влиянием этих цитокинов происходит активация эндотелиоцитов с трансформацией в высокий эндотелий и экспрессией ряда мембранных молекул, включая Р- и Е-селектины, рецепторы L-селектинов и интегринов (ICAM-1, VCAM-1), а также секрецией провоспалительных цитокинов и хемокинов.
Важным свойством провоспалительных цитокинов, в изобилии продуцирующихся в очаге продуктивного воспаления при ревматических заболеваниях, является их прокоагулянтная активность. Известны широкие перекрестные связи между иммунной системой и системой гемостаза. При ХПВ, вирусных инфекциях эти связи сопровождаются усилением сосудисто-тромбоцитарного и коагуляционного гемостаза. Появился даже термин “иммунотромбоз” в связи с вирусом SARS-CoV-2. Результатом подобных процессов является распространённые микротромбы, имеющие существенное патогенетическое значение. IL-6 способствует продукции активированных тромбоцитов с последующей их агрегацией. TNF-α и IL-2 увеличивает продукцию ингибитора важного тромболитического фактора – плазминогена (PAI-1) с последующим усилением тромбообразования. IFN-γ усиливает продукцию тромбоцитов с тромбогенными эффектами [96].
Известна прокоагулянтная активность IL-1, обусловленная экспрессией на активированном эндотелии фактора III с последующим образованием микротромбов. IL-1 способствует экспрессии адгезионных молекул на эндотелии из группы интегринов и селектинов. Кроме этого, IL-1 стимулирует продукцию эндотелиоцитами сильного вазоконстриктора – эндотелина-1. Другой цитокин – IL-6, способствует пролиферации клеток КВИ. Цитокины из группы TNF и IFN усиливают экспрессию антигенов МНС I и II классов на клетках макрофагально-моноцитарного ряда. К патогенетически важным свойствам TNF-α нужно отнести стимуляцию неоангиогенеза и репарацию эндотелиоцитов в очаге воспаления. Сильным стимуляторами неоангиогенеза являются группа провоспалительных СХС-хемокинов (CXCL9 – CXCL16) и самый важный из них – IL-8. Кроме этого, IL-8 способствует привлечению и аттракции нейтрофилов в очаг воспаления и осуществления ими функции так называемых “нейтрофильных ловушек”, которые усиливают тромбообразование [101].
Очевидно, что адгезионные лиганд-рецепторные взаимодействия и связанные с этим процессы неоангиогенеза являются важными патогенетическими звеньями развития ХПВ и формирования КВИ. Гетерогенность взаимодействующих клеток и молекул подчёркивает многокомпонентность и взаимозависимость процессов. Исходя из представленной картины, весьма перспективны исследования в области таргетной терапии ИВРЗ, а также разработки методов оценки стадии и активности ИВРЗ.
1.5. Провоспалительные хемокины и цитокины
Хемокины представляют собой семейство небольших (8–10 кДа) хемотактических цитокинов, которые контролируют процессы миграции клеток врождённого и приобретенного иммунитета и являются ключевыми факторами формирования КВИ. В настоящее время идентифицированно более 50 хемокинов и 19 рецепторов хемокинов. Хемокины являются секретируемыми сигнальными белками и классифицируются на четыре основных группы в зависимости от местоположения остатков аминокислоты цистеина: хемокины группы XC (которые содержат один концевой цистеин), хемокины группы CC (которые имеют два соседних концевых цистеина), хемокины группы CXC (которые имеют два цистеина, разделенных одной другой аминокислотой) и хемокины группы CX3C (которые имеют два цистеина, разделенных тремя аминокислотами). Хемокиновые рецепторы представляют собой трансмембранные белки, которые связаны с цитоплазматическими G-белками и регулируют миграцию иммунных клеток. Эти рецепторы разделены на группы CCR, CXCR, XCR и CX3CR [59].
Иммобилизация хемокинов в основном веществе рыхлой неоформленной соединительной ткани (коллаген адсорбирует хемокины) и на поверхности клеток формирует градиент их концентрации, необходимый для направленной миграции клеток в очаг воспаления. При ИВРЗ высокие уровни хемокинов и их рецепторов индуцируют миграционную активность иммунных клеток в поражённые органы и ткани, включая, Мф, ДК, Т-клетки и В-клетки, Нф [106]. Этому способствует связывание провоспалительных хемокинов с базальной мембраной венулярного отдела сосудистого русла, выстланного высоким эндотелием, а также с коллагеновыми волокнами (коллаген IV типа), что также формирует градиент хемоаттрактантов и стимулирует хемотаксис клеток в очаг ХПВ [172].
Весьма существенна роль провоспалительных хемокинов как интегративных факторов между врождённым и адаптивным иммунитетом. Так активация дендритных ДК и Мф в т. ч. и продуктами дезорганизации соединительной ткани посредством PAMP – рецепторов (TLR, NOD1, NOD2) стимулирует эти клетки к продукции хемокинов групп CXCL, CCL, CCR, привлекающих клетки адаптивного иммунитета – Т- и В-лимфоциты за счёт взаимодействия с хемокиновыми рецепторами CCR7 и CXCR4 в очаге воспаления [131].
При РА в сыворотке крови, синовиальной жидкости и непосредственно в синовиальной ткани определяются повышенные уровни хемокинов группы CXC (CXCL1, CXCL2, CXCL5, CXCL8 (ИЛ-8), CXCL9, CXCL10, CXCL12, CXCL13 и CXCL16), хемокинов группы CC (CCL2, CCL3, CCL4, CCL5, CCL18, CCL19, CCL20, CCL21 и CCL25) и хемокинов группы XC (XCL1 и XCL2). Каждый из указанных хемокинов имеет свои функциональные особенности, но их всех объединяет конечные провоспалительные эффекты. Более того, уровень и состав хемокинов, в частности, хемоаттрактанта CXCL13, служит маркёром активности воспалительного процесса при РА. Основными продуцентами указанных хемокинов являются синовиальные Мф и фибробласты, фолликулярные ДК, синовиальные эндотелиальные клетки и Нф, т. е. все клетки принимающие активное участие в формировании КВИ. В реализации патофизиологических эффектов указанных хемокинов при РА принимают участие рецепторы хемокинов из группы CXCR, включая CXCR1, CXCR2, CXCR3, CXCR4, CXCR5 и CXCR6 [113].
При СКВ, также как и при РА, определяется увеличение в сыворотке крови и в почках хемокина CXCL13 и уровень этого хемокина коррелирует с активностью заболевании. Продуцентами этого хемокина являются почечные дендритные клетки. Есть данные о повышении при СКВ уровней хемокинов из группы СС и СХС. Кумуляции Т-лимфоцитов в очагах продуктивного воспаления способствуют хемокиновые рецепторы CXCR3–5, CCR1, CCR2, CCR5, CX3CR1, CXCR3 и CCR5, В-лимфоцитов – рецептор CXCR5, а рецепторы CCR1, CCR2 и CX3CR1 регулируют миграцию моноцитов [53].
У пациентов с ССД определяется повышение хемокинов группы CXC (CXCL3–11 и CXCL16) в сыворотке или плазме. Считается, что основными продуцентами этих хемокинов являются плазмацитоидные ДК, локализующиеся в т. ч. и в воспалённой коже. Интересно, что при ССД определяется увеличение рецепторов CCR2 и CX3CR1 и эта повышение коррелирует с увеличением выработки CCL2 фибробластами кожи и увеличением выработки CX3CL1 эндотелиальными клетками кожи [18,36].
При ПМ повышается уровни CXCL9 и CXCL10 хемокинов. Считается, что при этом заболевании продуцентами CXCL10 являются CD68 + макрофаги, а также CD4+ и CD8+ T-лимфоциты, тогда как при дерматомиозите продуцентами этого же хемокина являются CD4+ T-лимфоциты и CD68+ макрофаги [45].
В мышечных биоптатах больных ПМ определяется повышенная экспрессия следующих хемокинов: CCL2, CCL3, CCL4 и CX3CL1. При дерматомиозите эндотелиальные клетки являются основными продуцентами CCL2, тогда как при полимиозитах макрофаги и CD8+Т-лимфоциты могут быть основными клеточными источниками CCL2 и CX3CL1. Что касается хемокиновых рецепторов, то известно, что в мышцах пациентов с ПМ присутствует большое количество Т-клеток с хемокиновым рецептором CXCR3, моноцитов с хемокиновым рецептором CCR2 и макрофагов с хемокиновым рецептором CX3CR1 [46, 151].
Выраженной хемотаксической активностью в отношении, прежде всего, нейтрофилов, а также Т-лимфоцитов, моноцитов, эозинофилов и базофилов, обладает IL-8, принадлежащий к группе провоспалительных СХС хемокинов. Он также инициируют эмиграцию клеток из сосудов в ткань. IL-8 продуцируется активированными эндотелиоцитами макрофагами и моноцитами. Этот провоспалительный хемокин способен связываться к глюкозаминогликанами межклеточного матрикса, Благодаря этому значительная часть IL-8 иммобилизируется, что очень важно для формирования градиента его концентрации в тканях, необходимого для хемотаксиса практически всех клеток воспалительного инфильтрата. Все эффекты продуцируемых хемокинов реалируются за счёт взаимодействия с хемокиновыми рецепторами двух основных групп – CCR и CXCR. Все клетки воспалительного инфильтрата экспрессируют указанные рецепторы к хемокинам. Необходимо учитывать, что специфичность хемокиновых рецепторов характеризуется вырожденностью: с одним и тем же рецептором может взаимодействовать до 10 хемокинов
При ИВРЗ продукция провоспалительных цитокинов как в очаге воспаления, так и в системной циркуляции достигает максимальных значений. Речь идёт, прежде всего, о таких классических провоспалительных цитокинах, как IL-1α, IL-1β, IL-2, IL-8, TNF-α, TNF-β.
Из цитокинов, патогенетически важных при ИВРЗ и принимающих участие в формировании КВИ, большее внимание уделяется IFN I типа, поскольку интерпретация IFN-зависимых механизмов при ревматических заболеваниях является существенной частью при создании персонифицированных схем лечения, связанных с применением многочисленных препаратов интерферонового ряда, в т. ч. и генноинженерных [8].
К IFN I типа относятся около 17 генетически детерминированных вариантов IFN и наиболее важными из них являются IFN-α и IFN-β. Основными клетками, продуцирующими IFN-α являются плазмоцитоидные ДК, являющиеся активными участниками КВИ, а продуцентами IFN-β являются большинство ядросодержащих клеток КВИ – фибробласты, макрофаги, дендритные клетки, синовиоциты, также находящиеся в составе КВИ. Основными индукторами усиленной продукции IFN I типа являются инфекционные агенты (вирусы, бактерии), которые, взаимодействуя с мембранными TLR рецепторами и цитоплазматическими RIG рецепторами всех перечисленных клеток, активируют их и побуждают к усиленному синтезу IFN I типа. Однако не исключается роль продуктов дезорганизации основного вещества соединительной ткани в активации IFN-продуцентов.
В целом, группа интерфероновых цитокинов в контексте ИВРЗ выполняет роль координатора врождённого и адаптивного иммунитета. В настоящее время при описании патогенетических механизмов заболеваний, характеризующихся преобладанием активации механизмов врождённого иммунитета, прежде всего РАМП-рецепторов, при отсутствии обнаруживаемых признаков аутореактивности Т- и В-клеток применяют термин “аутовоспаление”. В тех же случаях, когда очевидна аутореактивность сенсибилизированных Т- и В-клеток, в т. ч. и в составе КВИ, говорят об “аутоиммунных заболеваниях”[22].
Конечно, подобное разделение весьма условно, вместе с тем оно применяется с целью определения патогенетического звена, наиболее “чувствительного” к медикаментозной терапии и интерпретации многочисленных данных о селективности иммунотропных средств и воздействий. Подчёркивается значительная роль интерфероновых цитокинов в патогенезе хронических воспалительных заболеваний. Сывороточным уровням IFN I типа отводится роль биомаркёров иммуновоспалительных заболеваний и даже вводится понятие “интерферонопатий” [21,43].
В этом отношении весьма важным являются данные, свидетельствующие о том, что ауто-АГ, образовавшиеся в результате деструктивных, воспалительных процессов в рыхлой волокнистой соединительной ткани, взаимодействуют с мембранными TLR7 и TLR9 пДК. Это взаимодействие сопровождается усиленной продукцией пДК IFN I типа, а также провоспалительных цитокинов [104].
Продукция IFN-ов I типа регулируется несколькими поверхностными рецепторами в плазмацитоидных ДК, включая TLR7 и TLR9. Эти же клетки в составе КВИ, продуцируя в больших количествах IFN I типа и IL-6, способствуют дифференцировке В-лимфоцитов в плазматические клетки – источник ауто-АТ [73,152].
Внутриклеточный синтез IFN-ов I типа регулирует фактор 5 (IRF5). В свою очередь гиперпродукция IFN-ов I типа усиливает экспрессию TLR рецепторов на клетках макрофагально-моноцитарного типа, способствуя тем самым индукции аутоиммунного ответа и аутовоспаления. Этот механизм показан, в частности, при СКВ [54,148].
Увеличение уровня IFN I типа как в системной циркуляции, так и в КВИ, способствует прогрессированию и утяжелению воспалительного процесса, включая и местный. При СКВ, РА, болезни Шегрена уровень IFN I типа в сыворотке крови существенно повышен, наряду с повышенным риском развития этих заболеваний [49,67]. Это повышение обусловлено в т. ч. и активностью вышеобозначенных клеток in situ. В мышечных биоптатах при аутоиммунных миозитах в составе КВИ обнаруживаются пДК активированные Мф и лимфоциты. Эти клетки интенсивно продуцируют IFN I типа, повышающие экспрессию аллелей MHC I класса. Также интерфероны, продуцируемые клетками врожденного и адаптивного иммунитета, вызывают повышенную продукцию нескольких ауто-АГ, специфичных для аутоиммунного миозита и дерматомиозита. К ним относятся TRIM21, MDA5 и IFIT3 [95].
Аналогичную роль при ХВЗ играет и группа цитокинов, принадлежащих к семейству IL-1. Главными продуцентами IL-1 являются клетки КВИ – макрофаги и Th1 CD4+ клетки, соответственно. IL-1β является важным медиатором как врождённого, так и приобретенного иммунитета. Свою провоспалительную активность этот цитокин реализует за счёт активации цитозольных инфламмасом [140]. Рецепторы семейства IL-1 содержат домен, гомологичный цитоплазматическим доменам всех TLR. Следовательно, воспаление, индуцированное взаимодействием соответствующих лигандов с TLR рецепторами вызывает активацию аналогичных сигнальных активационных путей рецепторов семейства IL-1 [16].
Провоспалительную активность семейство IL-1, впрочем, как и все другие провоспалительные цитокины, реализует как в locus morbi, так и в системной циркуляции, обуславливая тем самым патогенетическую связь этих цитокинов между врождённым и адаптивным иммунитетом. Эта связь была продемонстрирована при некоторых моногенных интерферонопатиях. Резкое возрастание продукции IL-1β явилось результатом мутаций в генах цитозольных рецепторов врождённого иммунитета – NLRP3 и NLRC4, TLR5 и семейства рецепторов S100. Эти явления имели место при таких заболеваниях как РА, ювенильный полиартрит, ревматическая лихорадка, подагра, кардиоваскулярные болезни, сахарный диабет 2 типа, метаболический синдром, при опухолях [34,75,107].
Таким образом, продукция и рецепция провоспалительных хемо- и цитокинов, широкий спектр адгезионных лиганд-рецепторных взаимодействий обеспечивает миграцию клеток гематогенного происхождения, а также активацию резидентных клеток в очаге воспаления. Эти процессы являются важным патогенетическим звеном формирования КВИ при ИВРЗ, обуславливающих динамику и исход патологического процесса. Таргетное использование ингибиторов провоспалительных хемо-цитокинов является одним из наиболее патогенетически обоснованных способов лечения ИВРЗ.


