Куват Темиргалиевич Момыналиев
Проектирование медицинских изделий
5.5 Этапы процесса проектирования медицинских изделий с учетом эксплуатационной пригодности (человеческого фактора)
5.5.1 Идентификация использования, пользователей, среды использования, операционных контекстов использования и обучения (создание спецификации эксплуатации)
Чтобы проектировать изделие для реального использования, важно понимать, кто пользователи, их опыт, задачи, которые они должны выполнять, и контексты, в которых они работают. Эта информация может быть собрана несколькими способами: с помощью интервью, этнографического исследования, контекстуального опроса и подобных подходов, как показано в таблице 5.1. Здесь должны быть идентифицированы и описаны все потенциальные пользователи изделия, включая случайных, таких как обслуживающий персонал.
Понимание должно включать (можно этим не ограничиваться):
– профили пользователей: описание пользователей (пол, возраст, рост, образование, опыт, слух, зрение, компьютерная грамотность, ценности, мотивация, культура, любые антропометрические и биомеханические факторы, состояние болезни);
– среду использования (например, температура, влажность, свет, шум);
– путь пользователя, показывающий цели и последовательность задач, выполняемых отдельными группами пользователей, сценарии;
– обучение, которое пользователи должны пройти перед использованием продукта (включая любые сведения о завершении обучения);
– частоту использования.
Обоснование выбора репрезентативных пользователей, условий использования и достоверности результатов испытаний должно быть оценено и задокументировано с точки зрения риска на основе собранной информации и должно соответствовать предполагаемым заявленным характеристикам, сделанным для продукта.
5.5.2 Выявление известных проблем использования
Необходимо проанализировать данные (как внутренние, так и внешние) на предмет потенциальной ошибки при использовании аналогичных и сопоставимых изделий конкурентов (путем послепродажного надзора, жалоб, см. разделы 5.6 и 5.7) и включить в оценку ГОСТ ISO 14971-2021 "Изделия медицинские. Применение менеджмента риска к медицинским изделиям"). Другие источники информации, в том числе опросы и наблюдательные исследования, и те, которые указаны в разделе 5.7, также должны использоваться для выявления проблем, которые, возможно, не связаны с причинением вреда пациенту, но негативно влияют на эффективность работы пользователей.
5.5.3 Оценка риска использования и ошибки использования
Это шаг необходим для определения высокоуровневых задач и характеристик пользовательского интерфейса, которые могут быть связаны с безопасностью. Этот анализ может быть выполнен с использованием таких методов, как анализ задач, экспертный анализ, контекстуальное исследование и эвристический анализ, а также документирование оценки риска, связанного с использованием и ошибками использования изделия (см. ГОСТ ISO 14971- 2021). Предсказуемые ошибки использования, связанные с каждым шагом или характеристикой пользовательского интерфейса, должны быть задокументированы.
Задачи и связанные с ними ошибки использования должны оцениваться по степени тяжести вреда. Это позволит расставить приоритеты в разработке, чтобы сосредоточиться на областях пользовательского интерфейса, которые могут повлиять на безопасное и эффективное использование и, следовательно, снизить риски при применении. Обоснование приоритизации задач должно быть задокументировано.
Опасности, традиционно рассматриваемые при анализе рисков, включают:
– Физические опасности (например, острые углы или края)
– Механические опасности (кинетическая или потенциальная энергия движущегося объекта)
– Термические опасности (высокотемпературные компоненты)
– Электрические опасности (электрический ток, электромагнитные помехи (EMI))
– Химическая опасность (токсичные химикаты)
– Радиационные опасности (ионизирующие и неионизирующие)
– Биологические опасности (аллергены, бионесовместимые агенты и инфекционные агенты)
Эти опасности обычно связаны со случаями отказа изделия или его компонента, которые не зависят от того, как пользователь взаимодействует с ним. Заметным исключением являются инфекционные агенты (микробы/патогены), которые могут попасть в изделие в результате перекрестного заражения, вызванного ошибкой при использовании.
Опасности медицинских изделий, связанные с взаимодействием пользователя с ними, также должны быть включены в управление рисками. Они называются опасностями, связанными с использованием (рисунок 5.3). Эти опасности могут возникать из-за аспектов дизайна пользовательского интерфейса, из-за которых пользователь не может адекватно или правильно воспринимать, читать, интерпретировать, понимать или действовать в соответствии с информацией, поступающей от изделия. Некоторые опасности, связанные с использованием, более серьезны, чем другие, в зависимости от тяжести потенциального вреда пользователю или пациенту, столкнувшемуся с опасностью.
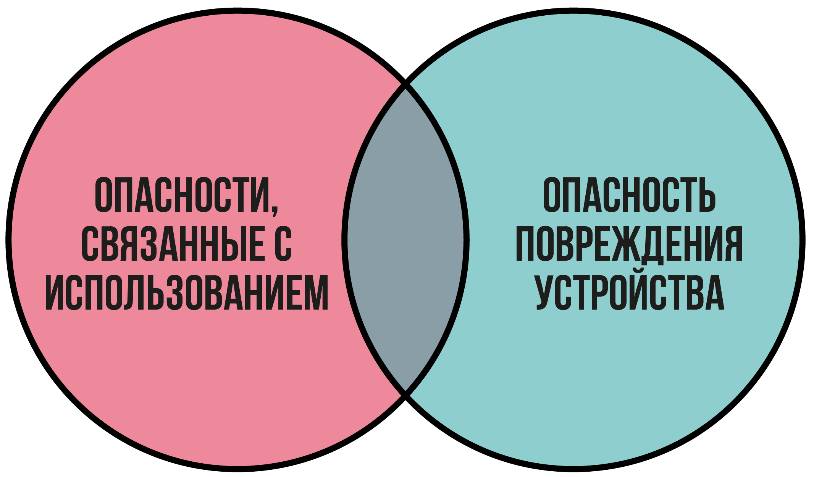
Рисунок 5.3 – Опасности, связанные с использованием или с отказом изделия и перекрывающиеся опасности, связанные как с его использованием, так и с отказом
Опасности, связанные с использованием, связаны с одной или несколькими из следующих ситуаций:
– Использование изделия требует физических, перцептивных или когнитивных способностей, превышающих возможности пользователя.
– Использование изделия не соответствует ожиданиям или интуитивным представлениям пользователя о его работе.
– Среда использования влияет на работу изделия, и этот эффект не осознается или не понимается пользователем.
– Конкретная среда использования ухудшает физические, перцептивные или когнитивные способности пользователя при использовании изделия.
– Изделия используются способами, которые производитель мог предвидеть, но не предусмотрел.
– Изделия используются ожидаемым, но нецелесообразным образом (например, из- за несоответствующих привычек пользователя) и для которых можно было бы применить меры по устранению или снижению риска, но они не были применены.
5.5.4 Разработка спецификации пользовательского интерфейса
Должна быть разработана спецификация пользовательского интерфейса, описывающая характеристики дизайна изделия для уменьшения потенциальных ошибок использования. К ним относятся такие характеристики пользовательского интерфейса, как маркировка, форма, цвет, значки, сигналы тревоги и кнопки. Также должен быть написан план того, как будет разрабатываться дизайн посредством оценки. Этот шаг может включать описание аспекта пользовательского интерфейса, который будет оцениваться, кто будет тестироваться и среда, в которой будет использоваться изделие.
5.5.5 Оценивания пользовательского интерфейса
Задачи, подлежащие тестированию при любой оценке, должны быть задокументированы. Это позволяет гарантировать, что все аспекты пользовательского интерфейса, которые могут повлиять на безопасность пользователя или пациента, имеют приоритет. Масштаб оценки должен быть определен на этом этапе и может включать:
– Все задачи/сценарии использования изделия, связанные с опасностями.
– Подмножество сценариев использования, связанных с опасностью, в зависимости от серьезности вреда (критические задачи).
Во время разработки любое изделие должно быть подвергнуто формирующей оценке, чтобы определить, насколько хорошо оно отвечает потребностям пользователя, эффективны ли меры по снижению риска, связанного с использованием, а также обнаружить ранее неизвестные ошибки. Ближе к концу процесса разработки изделия, как правило, необходимо провести итоговую оценку, чтобы продемонстрировать, что изделие может использоваться предполагаемыми пользователями без серьезных ошибок или проблем при эксплуатации, для предполагаемого использования и в ожидаемых условиях использования (также известных как человеческий фактор). Обычно бывает достаточно провести итоговое тестирование в смоделированной среде.
При планировании всех форм пользовательского тестирования важно учитывать этику и риск причинения вреда. Пример этической дилеммы при оценке конкретной медицинской технологии: «должны ли мы проводить это исследование». Участники должны по возможности давать информированное согласие на участие. Следует придерживаться принципа «Не навреди и, если возможно, приноси пользу». Обычно план включает в себя выявление рисков физического или психологического вреда, затрат (времени, расходов) для участников, а также потенциальных выгод для участников, как немедленных, так и долгосрочных. Прежде чем приступить к оценке, нужно учитывать, что производитель несет ответственность за то, что предлагаемые им исследования, соответствуют надлежащему уровню этических норм.
5.5.5.1 Формирующее оценивание (Итеративное тестирование во время разработки продукта)
Формирующее оценивание обычно выполняется итеративно на протяжении всех процессов проектирования и разработки изделия, с целью обеспечения руководства разработкой пользовательского интерфейса. Этот шаг используется для выявления ошибок использования изделия, которые могут привести к неприемлемому риску. Итеративное тестирование должно проводиться по всем аспектам проекта.
Эти исследования следует проводить на участниках, которые имеют соответствующие характеристики предполагаемых пользователей. Обоснование количества пользователей, участвующих в тестировании, должно быть задокументировано, обоснование должно учитывать разнообразие пользователей и количество поддерживаемых задач. Ошибки использования, выявленные в исследованиях, должны быть проверены и добавлены к оценке риска использования на предмет их серьезности, а также потенциального причинения вреда и определения их приемлемости.
Проверка инструкций по применению и сопроводительной документации/информации инструкции и сопроводительная документация являются важной частью пользовательского интерфейса, поскольку они сообщают важную информацию о безопасности и о том, как использовать изделие по назначению. Содержание и формат руководства должны быть согласованы с предполагаемыми пользователями. Формат тестирования будет включать в себя обеспечение того, чтобы пользователи могли следовать соответствующим инструкциям для правильного применения продукта и понимания информации, предоставленной для их безопасности. Исследование должно проводиться в том же формате, что и итоговый тест, и на материалах, репрезентативных для окончательного текста и макета.
Исследования и улучшения разработки следует проводить до тех пор, пока не будет уверенности в том, что дизайн безопасен и эффективен (что неприемлемый риск был снижен), чтобы перейти к итоговой оценке. Эффективная оценка приведет к хорошей эффективности в последующем пользовательском итоговом тестировании, сводя к минимуму проблемы проектирования на поздних стадиях разработки.
5.5.5.2 Итоговое оценивание
После завершения разработки и минимизации рисков, выявленных в ходе итеративного тестирования, следует приступить к итоговому исследованию. Это проверка проекта для тех задач, с выявленной потенциальной ошибкой использования, которая может повлиять на безопасность и эффективность изделия и иметь связанный с ним контроль рисков пользовательского интерфейса, включая информацию об изделии для обеспечения безопасности. Это тестирование должно проводиться на образце запускаемого изделия.
Исследование должно:
– Включать представителей всех выявленных групп пользователей (согласно Faulkner 20036, 15 участников из каждой группы идентифицируют в среднем 97 % всех ошибок использования).
– Включать все задачи / характеристики с выявленной потенциальной ошибкой использования, которая может повлиять на безопасность и эффективность изделия.
– Включать задачи, необходимые для работы изделия.
– Выполняться в реалистичной смоделированной среде или в условиях реальной среды, если моделирование не может обеспечить реалистичную среду, на готовом изделии (или изделии, репрезентативном для готового изделия).
– Не включать подсказки или просьбы просмотреть руководство во время исследования.
– Способствовать оценке выполнения задач и сбору субъективных данных о безопасности и простоте использования изделия.
При разработке и тестировании следует учитывать навыки и знания пользователей, включая характер и содержание требуемой подготовки; когда и как будет проводиться это обучение и являются ли предположения, сделанные в отношении проведения обучения, разумными и эффективными. Например, медсестры, работающие в незнакомой обстановке, могут быть экспертами в определенной диагностике или терапии, но иметь ограниченный доступ к обучению работе с незнакомым изделием. Необходимо четко сформулировать и обосновать свои ожидания / требования к обучению, в том числе продемонстрировать, что требования являются разумными для предполагаемых условий использования.
После итогового оценивания все выявленные ошибки использования должны быть рассмотрены на предмет первопричины и оценены на предмет остаточного риска. Также следует учитывать закрытые вызовы, трудности, связанные с использованием, и субъективные отзывы. Ошибки использования, возникающие в задачах, которые были определены как критические (связанные с безопасностью), должны быть тщательно рассмотрены на предмет их приемлемости. Эти ошибки использования, приводящие к неприемлемому риску, потребуют дальнейших действий по управлению рисками использования изделия и дальнейшего тестирования. удобства его использования, чтобы подтвердить, что проблемы устранены.
Любые новые обнаруженные ошибки должны быть добавлены к оценке риска использования изделия, а ошибка использования и остаточный риск оцениваются на предмет приемлемости.
5.5.6 Сводный отчет о человеческом факторе
Сводный отчет может быть подготовлен, чтобы сообщить о предпринятых шагах для снижения риска для пользователя при использовании медицинского изделия.
Обычно он включает следующие детали (но не ограничивается ими):
– предполагаемые пользователи изделия, использование, среда и обучение;
– описание пользовательского интерфейса изделия;
– сводка известных проблем использования (рассматриваемое изделие и другие похожие изделия на рынке);
– выбор задач пользователя и приоритизация (на основе файла управления рисками);
– резюме формирующих оценок;
– результаты итогового тестирования (включая ручную проверку) эксплуатационной пригодности;
– статус выгоды-риска изделия из файла управления рисками;
– выводы.
5.6 Пострегистрационный надзор
Добросовестные производители медицинских изделий имеют систематическую процедуру анализа опыта, полученного от использования их изделий на постпродажном этапе, и возможность применять соответствующие средства для любых необходимых корректирующих действий. Его часто называют пострегистрационным надзором (мониторингом). Требуемая упреждающая ПКМ чрезвычайно важна для обеспечения того, чтобы все соответствующие отзывы были рассмотрены и при необходимости приняты меры для улучшения существующих и будущих конструкций медицинских изделий, где это необходимо (т. е. до выхода на рынок).
В рамках этих обязательств производители медицинских изделий обязаны информировать о неблагоприятных событиях и корректирующих действиях по обеспечению безопасности использования изделий.
В России приказом Минздрава России от 19.10.2020 № 1113н утвержден Порядок сообщения субъектами обращения медицинских изделий обо всех случаях выявления побочных действий, не указанных в инструкции по применению или руководстве по эксплуатации медицинского изделия, о нежелательных реакциях при его применении, об особенностях взаимодействия медицинских изделий между собой, о фактах и об обстоятельствах, создающих угрозу жизни и здоровью граждан и медицинских работников при применении и эксплуатации медицинских изделий. Этот Порядок вступил в силу 01.01.2021 и впервые в российской практике предусмотрел клинический мониторинг медицинских изделий.
В ЕАЭС утверждено Решение Коллегии ЕЭК от 22 декабря 2015 г. N 174 «Об утверждении Правил проведения мониторинга безопасности, качества и эффективности медицинских изделий». Основой мониторинга безопасности является анализ сообщений о неблагоприятных событиях (инцидентах) на всех этапах обращения МИ, включая пострегистрационный контроль. Производитель (или его уполномоченный представитель) обязан оперативно реагировать на сведения о выявленных нежелательных реакциях, предоставляя в уполномоченный орган первоначальный, последующий (при необходимости) и заключительный отчеты о корректирующих действиях.
Производители должны активно и систематически запрашивать мнения пользователей, а также следить за тем, чтобы они знали о любых проблемах, связанных с взаимодействием медицинских изделий между собой. Этот обзор должен включать данные о жалобах на потенциальную ошибку использования собственных и (при наличии) аналогичных изделий и сопоставимых изделий конкурентов. Должны быть рассмотрены общедоступные данные о нежелательных явлениях и отзывах продукции. Такие данные можно найти в базе данных Федеральной службы по надзору в сфере здравоохранения (Росздравнадзора), FDA Manufac- turer and User Facility Device Experience (MAUDE), уведомлениях ЕС о безопасности на местах на веб-сайтах компетентных органов, CDRH FDA по отзывам медицинских изделий и т.п.
Другие соответствующие потенциальные источники данных должны быть рассмотрены там, где они доступны.
Они могут включать:
– статьи в журналах;
– результаты общедоступных клинических исследований;
– отзывы о послепродажных клинических исследованиях;
– реестры изделий;
– исследования пользователей и наблюдательные исследования пользователей, используемые для выявления проблем более низкого уровня, которые, возможно, не были связаны с причинением вреда пациенту, но тем не менее негативно влияют на пользовательский опыт и эффективность;
– статистика госпитализации;
– социальные медийные источники.
Этот постоянный обзор данных должен включать обновление оценки риска изделия, связанного с использованием и ошибками использования (см. ГОСТ ISO 14971). Оценка регулируется управлением рисками, проектированием удобства использования, верификацией изделия, а также процессами корректирующих и предупреждающих действий.
5.7 Жизненный цикл изделия и постоянное совершенствование
Проектирование удобства использования должно быть включено в дизайн изделия от концепции идеи до окончательной валидации изделия и послепродажного надзора как часть оценки пользы и риска для всех медицинских изделий и их комбинаций, используемых с лекарственными препаратами. Принимая во внимание широкий спектр медицинских изделий и изделий, комбинированных с лекарственными препаратами, необходим гибкий подход к требованиям в зависимости от типа изделия, предполагаемого использования и известных погрешностей использования аналогичных изделий. Однако принятый подход должен быть основан на оценке риска, обоснован и должным образом задокументирован на протяжении всего жизненного цикла изделия.
Принципы, изложенные выше, должны быть приняты во внимание при разработке новых медицинских изделий. Ранние итеративные исследования могут быть полезны на этапе клинического исследования при переходе от лабораторного стола к испытанию изделия на добровольцах, хотя может быть дано обоснование для проведения клинических испытаний на более позднем этапе с предварительными прототипами, близкими к окончательному варианту. Когда использование ограничено числом высококвалифицированного персонала, рисками управляют более жестко, а пользовательский интерфейс может быть рудиментарным, поэтому на данном этапе нет необходимости проводить формирующее оценивание человеческого фактора.
Однако если в клинических испытаниях участвуют минимально обученные пользователи или неспециалисты или вероятность ошибки использования, приводящей к причинению вреда, высока, проектирование удобства использования требует большего внимания на более ранней стадии разработки изделия.
Общепризнано, что во многих случаях пользовательский интерфейс будет постоянно улучшаться на протяжении всего жизненного цикла изделия, как на этапе начальной разработки, так и на этапе постмаркетинга. Будет важно обсудить входные факторы дизайна изделия на всех этапах взаимодействия с регулирующими органами с обоснованием принятого подхода. Итеративные исследования часто проводит в небольшом масштабе, начиная с самых ранних стадий разработки (ранний прототип), чтобы обеспечить установление надлежащих приоритетов дизайна для пользователей. Насколько это возможно, окончательная или итоговая валидация должна проводиться на полностью репрезентативном изделии, хотя после клинических испытаний могут потребоваться дальнейшие изменения его дизайна.
Важно, что управление изменением изделия происходит на протяжении всего жизненного цикла изделия будь то благодаря обратной связи после маркетингового анализа, достижениям в области технологий или проблем с поставкой компонентов. Любые изменения в изделии должны быть оценены, необходимость дополнительных исследований удобства использования должна быть рассмотрена в отношении связанных рисков, а принятый подход должен быть обоснован в техническом файле.
РЕЗЮМЕ
В медицинской практике для обследования и лечения пациентов все чаще используются медицинские изделия. При этом ошибки применения, вызванные недостаточной эксплуатационной пригодностью медицинского изделия, становятся все более серьезной причиной для беспокойства. Многие медицинские изделия, разработанные без использования процессов проектирования с учетом эксплуатационной пригодности (человеческого фактора), являются интуитивно непонятными, трудными в освоении и сложными в применении.
По мере развития здравоохранения все менее квалифицированные пользователи, включая и самих пациентов, используют медицинские изделия, которые становятся все более сложными. Проектирование пользовательского интерфейса с должным уровнем эксплуатационной пригодности требует иного процесса и уровня квалификации, чем техническая реализация пользовательского интерфейса.
Процессы проектирования с учетом эксплуатационной пригодности предназначены для идентификации и минимизации ошибок применения, что в свою очередь снижает связанные с использованием изделия риски. Некоторые, хотя и не все, виды некорректного использования поддаются управлению со стороны изготовителя. Процессы проектирования с учетом эксплуатационной пригодности связаны с процессами менеджмента риска.
В этой главе мы увидели, что проектирование удобства использования – это повторяющийся процесс, включающий проектирование, тестирование и проверку этапов проектирования, а также оно требует внимания к постпродажной фазе, поскольку во время использования изделия в клинической практике могут появиться доказательства того, что конструкция требует дальнейшего улучшения.

1. Почему необходимо учитывать человеческий фактор при проектировании медицинских изделий?
2. Укажите основные опасности, которые традиционно рассматриваются при анализе рисков использования медицинского изделия.
3. Перечислите основные отличия формирующей оценки от итоговой оценки.
4. Какие факторы необходимо учитывать при разработке спецификации эксплуатации медицинского изделия.
5. Чем нормальная эксплуатация/применение медицинского изделия отличается от предусмотренного применения/назначения медицинского изделия.


1. IEC 62366-1:2015 Медицинские изделия, часть 1: Применение инженерии удобства использования к медицинским изделиям (В России принят ГОСТ Р МЭК 62366-1-2021 «Изделия медицинские. Часть 1. Проектирование медицинских изделий с учетом эксплуатационной пригодности»).
2. МЭК/ТР 62366-2:2016. Медицинские изделия, Часть 2: Руководство по применению инженерии удобства использования к медицинским изделиям.
3. EN 60601-1-6:2010 Медицинское электрическое оборудование, часть 1-6: Общие требования к базовой безопасности и основным характеристикам. Стандарт обеспечения. Удобство использования (В России принят ГОСТ Р МЭК 60601-1-6-2014 "Изделия медицинские электрические. Часть 1-6. Общие требования безопасности с учетом основных функциональных характеристик. Дополнительный стандарт. Эксплуатационная пригодность").
4. ГОСТ Р МЭК 60601-1-2010 «Изделия медицинские электрические. Часть 1. Общие требования безопасности с учетом основных функциональных характеристик»
5. ГОСТ IEC 60601-1-8-2011 «Изделия медицинские электрические. Часть 1-8. Общие требования безопасности. Общие требования, испытания и руководящие указания по применению систем сигнализации медицинских электрических изделий и медицинских электрических систем».
6. IEC 60601-1-11:2010 "Изделия медицинские электрические. Часть 1-11. Общие требования безопасности с учетом основных функциональных характеристик. Дополнительный стандарт. Требования к медицинскому оборудованию и системам, используемым для ухода за больными в домашней среде.



