
Аурика Луковкина
Атеросклероз
Роль психоэмоционального напряжения в развитии атеросклероза
Значение этого фактора риска в возникновении атеросклеротического процесса многие ученые и исследователи оценивают как наиважнейший, ставят его на первое место. Как достоверный фактор, влияющий на атерогенез, – практически все. А. Л. Мясников в пользу значения нервного фактора в этиологии атеросклероза выдвигает следующие данные.
Он пишет: «Во-первых, как видно из обзора эпидемиологии атеросклероза, род работы людей, связанный с нервноэмоциональным напряжением, несомненно, способствует развитию атеросклероза. Во-вторых, изучение историй болезни лиц, страдающих различными формами атеросклероза (особенно коронарного) ясно указывает на значение психических и эмоциональных напряжений в его этиологии.
Так, например, мы рассмотрели анамнез 200 больных мужчин в возрасте 40–60 лет и установили, что в анамнезе (за год и больше до первого острого проявления болезни) резкие психоэмоциональные нагрузки были отмечены в 69 % случаев. В другой категории данных, касавшихся ближайшего на протяжении последнего полугода острого заболевания грудной жабой, инфарктом миокарда на почве атеросклероза, психоэмоциональные травмы и нервные перенапряжения были еще более частыми и отмечались в 80 % случаев, то есть у 8 из каждого 10 больных.
Именно на основании тщательного изучения историй болезни лиц, страдающих атеросклерозом, опытные врачи прошлых лет высказывались в пользу его нервного происхождения.
В-третьих, в пользу нейрогенной теории атеросклероза можно привести материалы, касающиеся содержания холестерина и других липидов крови. Можно сказать, что при всякого рода нервных напряжениях, содержание в крови холестерина возрастает. Весьма поучительны наблюдения, в которых изменения уровня холестеринемии отмечались у людей в прямой связи с возбуждением или успокоением их центральной нервной системы посредством соответствующих лекарств. Так, под влиянием введения возбуждающих нервную систему средств (фенамина и кофеина) содержание холестерина в крови повышается, а при введении средств, усиливающих процессы торможения (амиталнитрия и хлоралгидрата) понижается, причем снижение тем сильнее, чем выше был исходный уровень холестерина» (рис. 3).
Очень глубоко и детально разработал вопрос об эмоциональном напряжении как профилирующем, этиологическом факторе в развитии атеросклероза П. С. Хомуло. Он пишет: «В эксперименте на животных и исследованиях на человеке нами было показано влияние эмоционального и пихоэмоционального напряжения на физиологию желез внутренней секреции, симпатико-адреналовую систему, обмен холестерина и липопротеидов, состояние сосудистой стенки и развитие атеросклероза.
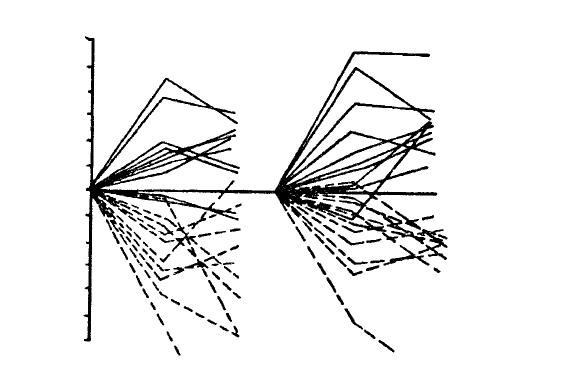
Рис. 3. Влияние нейротропных средств на содержание холестерина в крови у больных гипертонией и атеросклерозом. Кофеин – левые верхние кривые; фенамин – правые верхние; амил!натрий – левые нижние; хлоралгидрат – правые нижние кривые
Экспериментальный атеросклероз, сходных по морфологическим признакам с атеросклерозом у человека, мы получили с помощью различных моделей отрицательных эмоциональных напряжений у собак, кроликов и крыс без введения холестерина или других липидов в рацион.
Основные закономерности в развитии изменений в деятельности симпатико-адреналовой и эндокринной систем, обмена веществ, функции сосудистой стенки при эмоциональном напряжении у животных оказались сходными с таковыми при психоэмоциональном напряжении у людей. Это позволило провести аналогию между ролью эмоциональных напряжений в этиологии атеросклероза у животных и у человека.
В эксперименте были установлены основные патогенетические механизмы нейрогенного атеросклероза: гиперхолестеринемия и гиперлипопротеинемия, развивающиеся на базе эмоционально обусловленной мобилизационной гиперлипидемии; активация симпатико-адреналовой системы, повышения уровня биологических активных аминов при длительном эмоциональном напряжении на фоне подавления глюкокортикоидной функции коры надпочечников и как следствие – повышение проницаемости артерий в условиях гиперлипопротеидемии; гиперлипопротеидемия, усиленный эндоцитоз эндотелиальных клеток и повышенная проницаемость артерий, приводящие к накоплению липидов и особенно холестерина в стенке артерий и развитию атеросклероза. Основные патогенетические механизмы развития нетрогенного атеросклероза у животных и у человека имеют, по-видимому, много принципиально сходных черт.
На основании собственных данных и анализа исследований других лабораторий по проблеме сделано заключение, что рост заболеваемости атеросклерозом в большей мере обусловлен повышением психоэмоционального напряжения у людей.
Чтобы лучше понять действие эмоциональных факторов на развитие атеросклероза надо вспомнить, что чрезмерное (или просто часто повторяющиеся) психоэмоциональные травмы действуют подобно стрессу, учение о котором подробно разработал канадский патолог Селье. Напомним основные положения этого учения.
Стресс – это неспецифическая реакция организма, развивающаяся под влиянием различных интенсивных или не знакомых организму воздействий. Селье назвал его общим адаптационным синдромом, который сформировался в процессе эволюции именно как звено адаптации организма к широкому спектру факторов внешней и внутренней среды.
Механизм стресса состоит в том, что ответ на стрессорные ситуации внешней среды возбуждение адренергических центров головного мозга, детерминирующих стресс, вызывает значительное увеличение рилизинг – факторов, гормонов и высвобождения нейромедиаторов. Вначале гипотпламус активирует секрецию гормонов гипофиза, в дальнейшем возрастает выход кортикостероидов из надпочечников, а также катехоламинов из адренергических терминалей и надпочечников. Адаптивный эффект состоит в мобилизации энергетических и структурных ресурсов организма, что выражается увеличением в крови концентрации глюкозы, жирных кислот, нуклеидов, аминокислот, а также мобилизацией функции дыхания и кровообращения. Все эти изменения, подготавливающие организм к интенсивной мышечной деятельности (например, сражение, или быстрый бег), играли огромную роль в борьбе за выживание на заре существования человечества. Понятно, что повышение в крови глюкозы и жирных кислот позволяли обеспечить необходимую деятельность мышц и сердечно-сосудистой системы, участвующих в этих нагрузках. Весь процесс происходил параллельно выраженной эмоциональной реакции организма на ситуацию.
Прошли века, и современные люди значительно слабее и реже используют свою мышечную активность в повседневной жизни, но в то же время психоэмоциональные перегрузки многократно возросли. Но, учитывая, что закрепленный в ходе эволюции механизм стресса практически не изменился, в наш век можно говорить о незавершенной эмоциональной реакции, то есть психоэмоциональные конфликты остаются без заключительного финала (физических действий), что способствует накоплению неиспользованных, возросших во время стресса, веществ, способствующих запуску атеросклеротического процесса (липопротеиды, катехоламины, ангиотензин, ренин, вазопрессин и др.)
Из всего вышесказанного становится понятным, что люди, занимающиеся спортом или имеющие профессию, связанную с физической нагрузкой, значительно реже заболевают атеросклерозом или болезнями, связанными с его осложнениями (стенокардия, инфаркт миокарда, инсульт) даже при той же степени эмоциональных нагрузок, чем, например у лиц, преимущественно умственного труда или малоподвижного образа жизни. В крови людей, ведущих активный образ жизни, повышается уровень липопротеидов высокой плотности, что защищает их от развития атерослероза.
Интересно также отметить, что везде нужна своеобразная «золотая середина», так как исследования показали, что чрезмерные физические перегрузки приводят, напротив, к таким сдвигам в липопротеидном обмене, который способствуют атерогенным процессам в организме. То есть знаменитый лозунг «Бегом от инфаркта» должен быть подвергнут определенной коррекции, и физические нагрузки, а также занятия спортом в среднем и преклонном возрасте желательно правильно дозировать.
Хотелось бы сказать, что психоэмоциональный фактор имеет значение для развития атеросклероза, в основном, при частом и длительном действии, когда истощаются защитные механизмы, действующие, напротив, как противоатерогенный фактор при кратковременных отрицательных эмоциях (которые, видимо, стимулируют психику человека к поиску выхода из данного стресса).
Таким образом, прогрессирующее нарастание развития атеросклероза во всем мире, эпидемические масштабы его с биологической точки зрения есть нарушение естественных потребностей человека, как биологического вида, плата за неразумное использование возможностей современной жизни, нарушение естественных законов природы. Повышенные темпы современной жизни и работы, неправильный образ жизни, невротизация и перегрузки психики современного человека (с неадекватной реакцией на них) – вот факторы, способствующие росту атеросклероза в XX веке».
Механизм развития атеросклероза
Участие липопротеидов в атерогенезе
В 1912 г. Н. Н. Аничковым была предложена теория развития атеросклероза, основным патогенетическим звеном которой считались нарушения липидного обмена, в первую очередь холестерина. В дальнейшем, развитие этой концепции шло следующим путем (по А. Н. Климову):
1) в 20-х—40-х годах – увеличение холестерина в плазме крови усиливает опасность развития атеросклероза;
2) в 40-х—50-х годах: липопротеиды как переносчики холестерина являются ответственными за развитие атеросклероза;
3) в 60-х—70-х годах: липопротеиды неоднородны по своему составу; липопротеиды низкой плотности (ЛПНП) и липопротеиды очень низкой плотности (ЛПОНП) – являются атерогенными, а липопротеиды высокой плотности (ЛПВП) – антиатеро-атерогенными, защищающими организм от возникновения атеросклероза;
4) в 80-х—90-х годах: в основном, модифицированные ЛПНП и ЛПОНП, а также атерогенная независимая фракция ЛП(а) – в первую очередь ответственны за развитие атеросклероза.
Для того, чтобы хорошо разобраться в участии липопротеидов (ЛП) в механизме развития атеросклеротического процесса, вспомним некоторые аспекты жирового обмена в организме человека.
Понятие «жировой обмен» в последнее время часто заменяют на аналогичное – «липидный обмен», так как входящие в состав органов и тканей нейтральные жиры и жироподобные соединения объединяются под общим названием липиды.
Липиды это класс жиров и жироподобных веществ (липоиды), различающихся по своему химическому составу, структуре и выполняемым в организме функциям, но сходных по физико-химических свойствам (таким, как нерастворимость в воде, но растворимость в так называемых жировых растворителях – эфире, бензоле, хлороформе и др.). В организме человека она является важнейшим компонентом энергетического обмена.
Липиды бывают простые и сложные. К простым относятся: триглицериды (ТГ), воски, стерины; среди них наиважнейший – холестерин – (ХС), жирные кислоты (ЖК). К сложным липидам относят вещества, содержащие не только остатки жирных кислот, альдегидов или спиртов жирного ряда, но и остатки фосфорной кислоты, моно– или олигосахаров. К сложным липидам относят фосфолипиды и гликолипиды, из которых первые имеют наибольшее значение в процессах, относящихся к атерогенезу.
Триглицериды – нейтральные жиры, главная составная часть животных жиров и растительных масел, присутствующая во всех тканях организма, в питании человека является одним из основных пищевых веществ. Могут выполнять функцию «депо» – образуя запасы в подкожно-жировой клетчатке, являются главным энергетическим резервом организма.
Свойства ТГ определяются природой остатков жирных кислот в их молекуле. Жиры, содержащие значительное количество насыщенных ЖК (пальмитиновой, стеариновой, лауриновой, капроновой, каприловой, бегоновой и др.) имеют более высокую температуру плавления и у них твердая консистенция. Жиры, в состав которых входит много моно– и полиненасыщенных ЖК (арахидоновая, тимнодоновая, олеиновая и т. д.), называются маслами и при обычной температуре находятся в жидком состоянии. В сутки взрослый человек потребляет от 60 до 100 г жиров животного и растительного происхождения. Потребность в них у человека зависит от многих факторов: возраста, привычки питания, характера трудовой деятельности, климатических условий и др. Избыточное потребление животных жиров чревато нарушением жирового обмена (т. е. отложение избыточного жира в жировой ткани, что наблюдается, например, при ожирении).
ТГ, поступившие в организм с пищей, подвергаются расщеплению в тонком кишечнике (в основном, при действии ферментов поджелудочной железы, выделяющихся с панкреатическим соком).
Продукты расщепления ТГ, образовавшиеся в кишечнике, используются для ресинтеза тех жиров, которые более специфичны для человеческого организма.
Однако давно установлено, что при длительном употреблении какого-либо определенного жира, состав жировой ткани, а иногда – плазмы крови, становится идентичным тому составу жиров, который поступает извне.
При надобности ТГ синтезируются в самом организме во многих органах и тканях, хотя наиболее важную роль в этом отношении играют печень, стенка кишечника и клетки жировой ткани.
Заметим, что жировая ткань как депо энергии в организме, имеет большое значение. Ведь при сгорании 1 г нейтрального жира, выделяется 9,5 ккал (а выход энергии и углеводов, второго по значимости энергетического резерва, только 4,2 ккал/г). Установлено, что жировых запасов среднего человека достаточно для обеспечения энергией в течение примерно 40 дней.
Жирные кислоты бывают свободные (неэстерифицированные – НЭЖК) и эфирносвязанные (эстерифицированные – ЭЖК). В организме человека свободные и входящие в состав липидов ЖК выполняют энергетическую и пластическую функцию. Соотношение свободных и связанных ЖК: 5 % и 95 %, из последних эстерифицированные ЖК находятся в наиболее значимых липидах в следующих пропорциях: в ТГ примерно 45 %; в эфирах ХС примерно 15 %; в ФЛ примерно 35 %. Выделяют физиологически наиболее важные ЖК, имеющие практическое значение в организме, – их около 20.
Жирные кислоты бывают насыщенные (примерно 25 %) и ненасыщенные (примерно 75 %). Установлено, что если в рацион человека входит значительное количество жиров, содержащих много насыщенных ЖК, это способствует развитию гиперхолестеринемии; включение же в рацион растительных масел, богатых ненасыщенными ЖК, способствует снижению содержания холестерина в крови. Известно, что ткани человека и некоторых животных потеряли способность синтезировать ряд полиненасыщенных кислот. К таким кислотам относятся линолевая, линоленовая и арахидоновая кислоты; они получили название незаменимых (эссенциальных) ЖК или условно – витамин F.
Как правило, люди не испытывают недостатка в незаменимых ЖК, так как они в значительных количествах содержатся во многих пищевых продуктах растительного происхождения, а также в рыбе и птице (в мясных продуктах их содержание значительно ниже).
Особое место среди полиненасыщенных ЖК занимает так называемая тинодоновая кислота; ею богат жир морских животных. Исследовано, что низкая распространенность ишемической болезни сердца, замедленная свертываемость крови эскимосов связана с их традиционной диетой, содержащей продукты, богатые тинодоновой кислотой (сардина, лосось, сельдь и др.).
При необходимости ЖК синтезируются в организме во многих органах и тканях: в печени, стенке кишечника, легочной, жировой тканях, костном мозге, лактирующей молочной железе, и в сосудистой стенке. Биосинтез ЖК в тканях организма регулируется по принципу механизма обратной связи, то есть накопление ЖК оказывает тормозящее влияние на их биосинтез.
Увеличение концентрации НЭЖК в крови может быть обусловлено приемом жирной пищи, факторами, стимулирующими липолиз – гепарином, адреналином и др. Повышенное содержание НЭЖК отмечается при атеросклерозе после инфаркта миокарда, а также при сахарном диабете, нефрозах, голодании, стрессах. Пониженное содержание НЭЖК отмечается при гипогиерозе, продолжительном лечении глюкокортикоидами, после инъекции инсулина.
Холестерин. Важнейший в биологическом отношении липид, представитель класса стеринов. В организме человека выполняет разнообразные физиологические функции; прежде всего, из холестерина образуются желчные кислоты, витамин Д3, половые гормоны и кортикостероиды.
В зависимости от питания в организм человека ежедневно поступает примерно от 300 до 500 мг холестерина, который может содержаться в пище в свободном (нестерифицированном) и связанном (с жирными кислотами) состоянии. Этот эстерифицированный холестерин расщепляется в тонком кишечнике на холестерин и жирные кислоты, после чего происходит всасывание свободного холестерина для нужд организма, в том числе и образования холестеринсодержащих липопротеидов.
Учитывая, что в самой желчи, поступающей в тонкую кишку за сутки, содержится еще примерно 1500 мг холестерина, то в общей сумме количество холестерина, подвергающегося ресинтезу, значительно увеличивается.
Известно, что каждая клетка в организме всех млекопитающих содержит холестерин и нуждается в нем для поддержания пространственной конфигурации (так называемая холестериновая функция клеточного «скелета»).
Очень важную роль играет неэстерифицированный холестерин как компонент в составе клеточных мембран, где он вместе с фосфолипидами обеспечивает избирательную проницаемость клеточной мембраны для веществ, поступающих в клетку и выходящих из нее. (По последним данным, ХС в мембранах клеток имеет также отношение к стабильности ее в ответ на воздействие температур).
В теле взрослого человека содержится около 140 г холестерина; хотя распределен он в органах и тканях неравномерно. Больше всего его содержится в корковом веществе надпочечников; затем – в головном мозге и нервной ткани; значительно ниже – в сосудах, печени, почках, селезенке, костном мозге; меньше всего – в скелетных мышцах и соединительной ткани.
Синтез холестерина в организме человека осуществляется в любой клетке практически всех органов и тканей. Однако чаще всего это происходит в печени и тонком кишечнике (в меньшей степени).
Известно, что под влиянием некоторых факторов, таких, как действие радиации, повышенная концентрация тиреоидных гормонов и инсулина – происходит усиление синтеза холестерина; а при тиреоэктомии, повышении концентрации глюкокотикоидов или глюкагона – угнетение его синтеза. Голодание также блокирует синтез данного липида.
Известно, что в плазме крови человека и животных весь холестерин находится в виде комплексов с белками – в так называемых липопротеидах (о них более подробно будет изложено далее), с помощью которых и осуществляется его транспорт. Более всего холестерина в плазме крови находится в составе липопротеидов низкой плотности (ЛПН), это примерно от 67 до 70 %; около 10 % – в составе липопротеидов очень низкой плотности (ЛПОНП); и 20–24 % – в составе липопротеидов высокой плотности (ЛПВП).
Замечено, что сходное распределение отмечено у тех животных, которые склонны к развитию атеросклероза (это обезьяны, свиньи, кролики, морские свинки, голуби, куры и т. д.). Напротив, у животных, развитие атеросклероза для которых не характерно (собаки, кошки, суслики, норки, песцы, лошади, дельфины и др.) большая часть холестерина плазмы находится в составе ЛПВП, обладающих антиатерогенным действием.
Именно поэтому, в клиническую практику введено правило расчета коэффициента, отражающего отношение атерогенных липопротеидов к антиатерогенным.
Так называемый холестериновый коэффициент атерогенности (k) рассчитывается по следующей формуле:
k общий = (XC общий – XC * ЛПВП) / XC * ЛПВП,
где ХСобщий – концентрация общего холестерина; ХС X ЛПВП – концентрация липопротеидов высокой плотности.
Это отношение является идеальным у новорожденных (не более единицы); у лиц 20–30 лет его величина колеблется от 2 до 2,9; у здоровых лиц старше 30 лет она находится в пределах 3–3,5 (причем у женщин, как правило, ниже, чем у мужчин); у лиц с ишемической болезнью сердца – от 4 до 5,0–6,0 единиц и выше.
Этот коэффициент, как показатель, в настоящее время, является более чувствительным фактором развития атеросклероза, чем холестерин – лецитиновый показатель (отношение концентрации холестерина к концентрации лецитина в плазме крови), который широко применялся в клинике ранее.
Расщепление избыточного холестерина в организме происходит с образованием различных продуктов, физиологически важных для деятельности многих функциональных систем. Прежде всего это катаболизм холестерина в печени с образованием желчных кислот; в надпочечниках – с образованием кортикостероидных гормонов, в тестикулярной ткани и яичниках – с образованием стероидных половых гормонов.
Наибольший процент приходится на окисление холестерина до желчных кислот, которые могут по мере надобности вновь всасываться в тонком кишечнике (при выделении их поджелудочной железой в процессе переваривания пищи), а могут удаляться через толстый кишечник с фекалиями (таким образом из организма человека ежедневно подлежит удалению от 0,5 до 1 грамма холестерина).
Фосфолипиды. Относятся к классу сложных липидов; они являются соединениями сложных эфиров многоатомных спиртов глицерина с высшими жирными кислотами, а также фосфорной кислотой – с присоединенным к ней азотистым основанием.
С пищей в организм человека поступает 1–2 г фосфолипидов в сутки; еще примерно 10–12 г изливается в тонкий кишечник c желчью, где все они подвергаются расщеплению и всасыванию.
Фосфолипиды так же, как и холестерин, найдены во всех клетках любых органов и тканей организма. Часто эти 2 липида называют комплементарными, так как фосфолипиды – такой же необходимый компонент в структуре мембраны, как и холестерин. Больше всего фосфолипидов находится в тканях головного мозга и нервов; в 2 раза меньше – в печени; еще меньше – в почках и сердце.
Известно, что их функциональные обязанности многогранны. Фосфолипиды участвуют в иммунологических процессах, в реакциях, связанных с системой свертывания крови; в пролиферации и регенерации клеток, в проведении импульсов по нервным волокнам и многих других процессах, которые интенсивно изучаются в последние годы.
С точки зрения липидного обмена, им принадлежит огромное значение в формировании липопротеидов (особенно липопротеидов высокой плотности, где их содержание максимально).
Синтез фосфолипидов, как и холестерина, происходит практически во всех тех же органах, но наиболее интенсивно – в печени и клетках кишечника.
Максимальное количество фосфолипидов приходится на фосфатидилхолин (лецитин), азотсодержащее основание которого – холин.
Известно, что, если длительно не покрывается пищевая потребность в холине, то вместо синтеза фосфолипидов происходит сдвиг в сторону синтеза липопротеидов, содержащих большой процент таких липидов, как триглицериды и холестерин, которые способствуют жировой инфильтрации печени.
Таким образом, механизм действия лекарственных препаратов: холина, хлорида и метионина (последний в процессе переметилирования синтезирует холин) основан на увеличении фракции фосфолипидов, которые в составе липопротеидов высокой плотности предотвращают развитие атеросклероза.
Катаболизм ФЛ происходит во многих тканях организма под действием специальных ферментов (фосфолипаз).
Содержание основных липидов в плазме человека:
ТГ = 0,5–2,3 ммоль/л;
ХС общ = 3,9–6,5 ммоль/л;
НЭЖК = 0,4–0,8 ммоль/л;
ЭЖК = 7,1 – 15,9 ммоль/л;
ФЛ = 1,4–3,7 ммоль/л.
Все эти основные липиды в плазме крови человека находятся в комплексе с белками, образуя сложные соединения – липопротеиды (ЛП).
ЛП входят в состав всех живых организмов, выполняют функцию транспорта и запасания липидов, являются необходимой составляющей различных структур клетки; содержание ЛП в крови служит важным диагностическим тестом при ряде заболеваний (в первую очередь, при атеросклерозе).
ЛП делят на свободные (те, что находятся в плазме крови) и структурные (это ЛП, находящиеся в мембранах клеток, ми– елиновой оболочке нервов и т. д.).
Рассмотрим более подробно ЛП плазмы крови. По классификации, использующей гидратированную плотность ЛП, их делят на 4 класса:
1) хиломикроны (ХМ);
2) липопротеиды очень низкой плотности (ЛПОНП);
3) липопротеиды низкой плотности (ЛПНП);
4) липопротеиды высокой плотности (ЛПВП).
По электрофоретической подвижности выделяют пре-b– липопротеиды (что соответствует ЛПОНП); b-липопротеиды (соответствует ЛПНП), l-липопротеиды – (соответствует ЛПВП).
Мы в дальнейшем будем пользоваться, в основном, первой классификацией. Рассмотрим каждый класс отдельно.







