А. Л. Вёрткин
Гастропротекция. Руководство для практических врачей
Гастропротекция: что мы знаем сегодня
Итак, главная цель гастропротекции – предотвращение угрожающих жизни осложнений вследствие повреждения слизистой оболочки желудка, ДПК и пищевода: ЖКК, перфорации, развития в исходе повреждения рубцовых деформаций и непроходимости и в отдаленной перспективе – малигнизации.
Методы гастропротекции:
✓ уменьшение повреждающего действия основного эндогенного фактора агрессии для слизистой оболочки желудка, ДПК и пищевода – соляной кислоты (HCl) у пациентов с высоким риском развития кислотозависимых заболеваний;
✓ восстановление нарушенных механизмов физиологической самозащиты и регенерации гастродуоденальной слизистой или их стимуляция;
✓ физическая защита слизистой оболочки верхних отделов ЖКТ от повреждающего действия экзогенных и/или эндогенных факторов физической и химической агрессии.
Структурные и функциональные основы физиологической гастропротекции
Железы слизистой оболочки желудка в сутки секретируют 1–2,5 литра желудочного сока. Железы располагаются в глубине желудочных ямок (рис. 2). Количество желез в желудке достигает 15 млн. В зависимости от расположения железы подразделяют на кардиальные, собственные (фундальные), пилорические и железы дна желудка (рис. 3).
Кардиальные железы в основном содержат слизистые клетки, которые вырабатывают муцин, бикарбонаты и хлориды калия и натрия.
Собственные (фундальные) железы, самые многочисленные, расположены в теле и дне желудка. Состоят из 5 типов клеток: главных, париетальных (обкладочных), шеечных, добавочных слизистых и эндокринных клеток. Главные клетки секретируют пепсиноген, который в просвете желудка под влиянием соляной кислоты превращается в активный пепсин – главный фермент для переваривания белка. Париетальные (обкладочные) клетки секретируют HCl и внутренний антианемический фактор (фактор Кастла), необходимый для всасывания витамина В12 в кишечнике (рис. 4). Синтез и секрецию фактора Кастла, как и секрецию HCl, в желудке стимулируют гистамин, гастрин, а системно – стимуляция активности блуждающего нерва (ацетилхолин). Слизистые шеечные клетки являются предшественниками эпителиоцитов желудка. Вырабатывают муцин, который предохраняет их от повреждения. Добавочные (слизистые) клетки секретируют муцин и гидрокарбонат. Эндокринные клетки относятся к диффузной эндокринной системе (ДЭС или APUD-система), которая в своем гастроэнтеропанкреатическом отделе вырабатывает гормоны, регулирующие секрецию и моторику пищеварительного тракта.
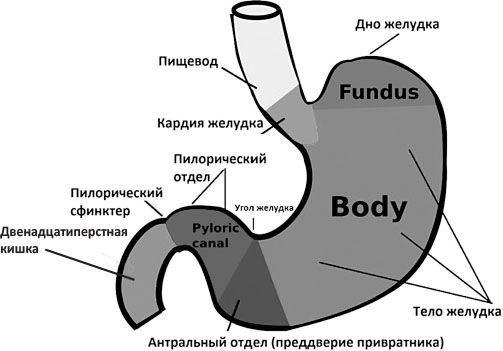
Рисунок 1. Функциональная анатомия желудка.
Пилорические железы также в основном содержат эндокринные и слизистые клетки.
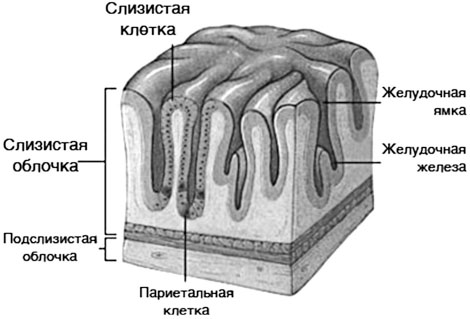
Рисунок 2. Строение слизистой оболочки желудка.
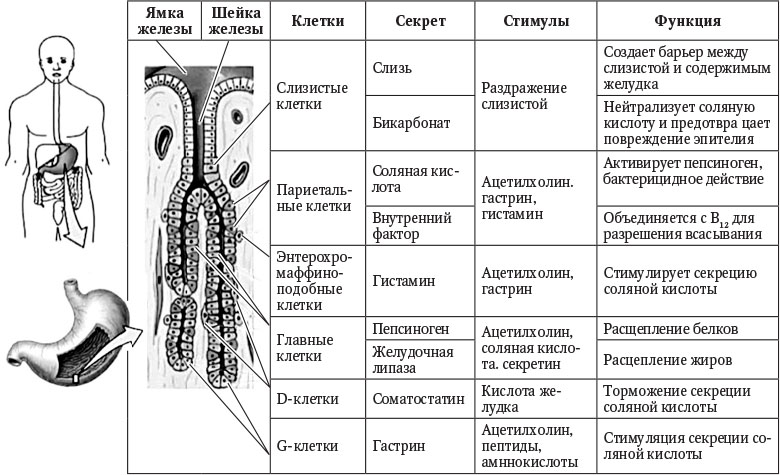
Рисунок 3. Структура и клеточный состав желез желудка.
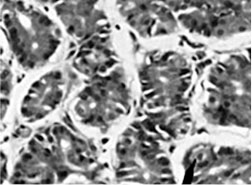
Рисунок 4. Париетальные клетки человека (гематоксилин-эозин, х200).
Эндокринные клетки слизистой оболочки желудка секретируют гастроинтестинальные пептиды и гормоны.
✓ ECL клетки расположены в теле желудка и секретируют гистамин, который стимулирует секрецию HCl;
✓ D-клетки расположены в теле и пилорическом отделе, секретируют соматостатин, стимулирующий секрецию желудочного ингибиторного пептида и угнетающий секрецию гистамина и НCl;
✓ EC-клетки расположены в теле и пилорическом отделе, секретируют серотонин, мотилин, вещество Р, активирующие моторику ЖКТ;
✓ G-клетки расположены в пилорическом отделе, секретируют гастрин, активирующий секрецию HCl и пепсиногена (см. рис. 3).
Соляная кислота определяет кислую реакцию желудочного сока
Соляная кислота (HCl) синтезируется в париетальных клетках желез тела желудка внутри специфических структур – туболовезикул, где ее концентрация очень высокая. В просвет железы HCl проникает против градиента концентрации 1:1000000 путем активного транспорта через апикальные мембраны париетальных клеток (секреторная поверхность клетки), в которых находятся специальные канальцы при участии специфического белка. Процесс выхода ионов водорода в канальцы является энергозависимым и происходит при участии фермента-переносчика Н+/К+-АТФазы (протоновый насос), которая обеспечивает перенос Н+из цитоплазмы в канальцы париетальной клетки. В секреции также задействованы: переносчик ионов K+/Cl– по типу симпорта, переносчик ионов НСО3-/Cl– по типу антипорта и фермент карбоангидраза, обеспечивающий синтез Н2СО3 из углекислого газа и воды (рис. 5).

Рисунок 5. Секреция соляной кислоты париетальной клеткой желудка. Основные транспортные системы, роль H+/K+-АТФазы (1).
Синтез и секрецию HCl в париетальных клетках стимулируют ацетилхолин, гастрин и гистамин, которые активируют свои специфические рецепторы (М3, G и Н2) на мембране клеток и непосредственно на тубуловезикулах, содержащих Н+/К+-АТФазы. Ингибируют синтез и секрецию HCl простагландины и соматостатин. Несмотря на постоянное функционирование нескольких путей и уровней регуляции, секреция HCl четко интегрируется в соответствии с необходимыми для оптимального пищеварения уровнями кислотности, который определяют хеморецепторы желудка и который зависит 1) от состава пищи и 2) от способности желез желудка к ощелачиванию.
Кислотность в каждом из отделов желудка различается и соответствует его физиологической функции. В теле желудка, где находятся париетальные клетки и секретируется HCl, кислотность в просвете желудка наиболее высокая. Базальная секреция желудка максимальна вечером (в 23 часа) и минимальна утром (от 5 до 11 часов). Это свидетельствует о ее зависимости от тонуса блуждающего нерва, а также связано с секрецией мелатонина, синтезирумого как в шишковидной железе, так и в клетках ДЭС. Базальную секрецию стимулируют: гистамин, ацетилхолин, гастрин, кальций, энкефалины; подавляют: соматостатин, кальцитонин, глюкагон, дофамин, вазоактивный пептид, норадреналин, простагландины; регулирует: панкреатический полипептид.

Основные функции HCl:
✓ активирует пепсиногены и превращает их в пепсины;
✓ создает кислую среду, необходимую для действия ферментов желудочного сока;
✓ способствует денатурации и набуханию белков в желудке, что облегчает их последующее расщепление пепсинами;
✓ гидролизирует небелковые компоненты пищи;
✓ обеспечивает антибактериальное действие желудочного сока;
✓ возбуждает панкреатическую секрецию.

Нормальная кислотность в теле желудка натощак или в отсутствии любой другой стимуляции (при базальной секреции HCl): 1,5–2,0 ед. pH. При рН<1,5 единиц говорят о гиперацидности, при рН= 2,1–5,9 ед. – о гипоацидности, при рН>6,0 ед. – об анацидности желудка. Несмотря на то что на базальную секрецию HCl влияют многие факторы, ее величина в желудке у здорового человека при обычных условиях практически постоянна и не превышает 5–7 ммоль в час. Однако и у здоровых людей базальная секреция может увеличиваться при остром и хроническом стрессе, у курильщиков, при нарушениях сна, на фоне злоупотребления кофе и крепким чаем, а также при приеме лекарств, содержащих ксантины (теофиллин). Базальная секреция уменьшается после ваготомии, при приеме антихолинергических лекарственных средств, Н2-блокаторов и ингибиторов протонной помпы (ИПП).
При поступлении пищи количество свободной HCl в содержимом желудка на некоторое время уменьшается до 2,5–3 ед. рН, однако в течение от 10 мин до 1,5 ч происходит активация секреции – дебит HCl нарастает до величин, иногда превышающих базальные уровни. Стимуляция секреции HCl начинается еще до попадания пищи в желудок. Первую фазу секреции (так называемую цефалическую) запускают запах, вид и вкус пищи, воздействие которых передается от центральной нервной системы по вагусным афферентным путям. Наиболее значительная фаза секреции – желудочная, начинается после попадания пищи в желудок. Растяжение желудка запускает выделение гастрина из G-клеток, расположенных в пилорическом отделе желудка. Гастрин, воздействуя на париетальные клетки напрямую или через активацию ECL-клеток с высвобождением гистамина, стимулирует продукцию HCl. Фаза стимулированной секреции длится в течение всего цикла пищеварения в желудке, а также и после эвакуации первых порций химуса в ДПК. Стимулированная секреция одновременно активирует секрецию основного блокатора секреции HCl – соматостатина D-клетками пилорического отдела желудка.

✓ Нормальная кислотность в пищеводе: pH = 6,0–7,0.
✓ Кислотность на поверхности эпителиального слоя, обращенного в просвет желудка: pH = 1,5–2,0.
✓ Кислотность в глубине эпителиального слоя желудка: около pH = 7,0.
✓ Нормальная кислотность в антральном отделе желудка: pH = 1,3–7,4.
✓ Нормальная кислотность в луковице двенадцатиперстной кишки: pH = 5,6–7,9.
✓ Кислотность сока тонкой кишки: 7,2–7,5 рН; при усилении секреции достигает pH = 8,6.
✓ Кислотность сока толстой кишки: pH = 8,5–9,0.

В антральном отделе желудка кислотность может колебаться в пределах 1,3–7,4 ед. рН. Однако в медицинской практике принято оценивать не кислотность, а компенсацию ощелачивания в антральном отделе. При рН>4 ед. кислотонейтрализующая функция антрального отдела считается нормальной или компенсированной. При рН>1,5–3,9 ед. – субкомпенсированной, при рН<1,5 единиц – декомпенсированной. В пилорическом отделе, как и в ДПК, среда секрета должна быть близка к нейтральной или слабощелочной с рН>5 единиц. При рН в просвете ДПК < 3,5 единицы (ацидификация ДПК) при недостаточной секреции гидрокарбоната в антральном и пилорическом отделах желудка, ДПК и поджелудочной железе развивается кислотная деструкция панкреатических ферментов с нарушением полостного пищеварения и появления симптомов диспепсии различной тяжести.
Таким образом, кислотность в просвете желудка варьирует посредством баланса между секрецией HCl (включение большего/меньшего количества париетальных клеток и нейтрализацией HCl бикарбонатом желудочного сока, секреция которого во всех структурах прямо зависит от кровообращения в артериолах и физиологического уровня простагландина Е2 в слизистой. Чем быстрее секреция HCl, тем меньше она нейтрализуется и тем выше кислотность в просвете желудка. Однако какой бы ни была кислотность в просвете желудка и ДПК, на поверхности клеток эпителия, под слоем муцина среда всегда щелочная, поскольку эпителиоциты слизистой желудка также постоянно секретируют бикарбонат. Эндогенные стимуляторы секреции бикарбоната – сама HCl, соматостатин, активация блуждающего нерва или введение холиномиметиков. Ингибиторы секреции бикарбоната: активация симпатического отдела вегетативной нервной системы – агонисты (стимуляторы) а-адренорецепторов, этанол, желчные соли, терапия нестероидными противовоспалительными препаратами (НПВП). Таким образом, секреция бикарбоната эпителием желудка и железами желудка, ДПК и поджелудочной железой является важнейшим фактором физиологической гастропротекции и обеспечения эффективного полостного пищеварения в тонкой кишке.