
Татьяна Александровна Лобаева
Основы биохимии. Учебно-тренировочные задания для студентов медицинских специальностей
Витамины
Витамины – эссенциальные (жизненно важные) факторы питания человека и животных, необходимые для протекания разнообразных химических процессов в организме. Витамины участвуют в обмене веществ как в качестве коферментов – непосредственных участников ферментативных реакций (витамины группы B, витамин РР), так и в виде регуляторов отдельных процессов (витамины С, А, Е, К, D).
Провитамины – вещества, поступающие с пищей или синтезируемые в организме и являющиеся источником витаминов; например, из 7-дегидрохолестерола под влиянием ультрафиолетовых лучей образуется витамин D3.
Классификация витаминов:
• Жирорастворимые витамины: А (ретинол), D (кальциферол), E (токоферол), K (нафтохинон), F (полиненасыщенные жирные кислоты).
• Водорастворимые витамины: B1 (тиамин), B2 (рибофлавин), B3 =РР (никотинамид), B5 (пантотеновая кислота), B6 (пиридоксин), B9= ВC (фолиевая кислота), B12 (цианкобаламин), H (биотин), C (аскорбиновая кислота).
• Витаминоподобные вещества: жирорастворимые – Q (убихинон), водорастворимые – B4 (холин), P (биофлавоноиды), BT (карнитин), B8 (инозит), U (S-метилметионин), N (липоевая кислота), B13 (оротовая кислота), B15 (пангамовая кислота).
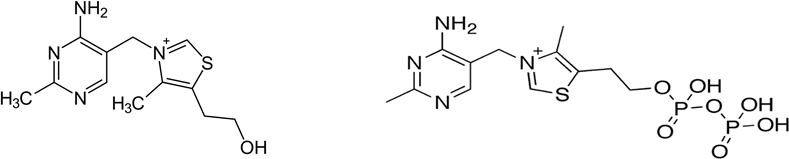
Рис. 6. Тиамин и его кофермент тиаминпирофосфат, синоним тиаминдифосфат (ТПФ, ТДФ)
Основным источником витаминов являются пищевые продукты растительного и животного происхождения, и лишь некоторые из них (фолиевая кислота, биотин, витамин К) способны синтезироваться микрофлорой кишечника. При недостатке в организме того или иного витамина или нарушении его обмена (всасывания в кишечнике, транспорта кровью, превращения в кофермент) возникают состояния, называемые гиповитаминозами. Жирорастворимые витамины при увеличении дозы накапливаются и могут вызывать гипервитаминозы с рядом общих симптомов (потеря аппетита, расстройство ЖКТ, сильные головные боли, повышенная возбудимость нервной системы, выпадение волос, шелушение кожи) и со специфическими признаками. Яркая картина гипервитаминозов отмечается только для витаминов А и D.
Определение витаминов в продуктах питания, микробиологических средах, а также стандартизация препаратов витаминов представляют большой практический интерес.
План описания витамина:
• Химическое название, буквенное обозначение, классификационная характеристика (водорастворимый, жирорастворимый)
• Химическое строение (химическая формула витамина, составные части (подписать), активная форма витамина/ кофермент с формулами)
• Источники (в каких продуктах питания содержится)
• Суточная потребность
• Особенности метаболизма (всасывание, распределение, превращение)
• Биохимические функции (биологическая роль, механизм действия)
• *названия ферментов, примеры биохимических реакций (не менее 2 реакций!)
• Антивитамины (если они выявлены): названия и формулы
• Название и проявления гиповитаминоза и авитаминоза
*Гипервитаминозы (для вит D)
Основные термины раздела:
Витамины – незаменимые низкомолекулярные факторы питания органического происхождения, присутствующие в пище и участвующие в биохимических реакциях в качестве коферментов или регуляторов.
Витаминоподобные вещества – группа условно незаменимых факторов питания, участвующих в отдельных биохимических и физиологических процессах, при их недостаточном поступлении с пищей не наблюдается развития патологических изменений.
Провитамины – вещества, поступающие с пищей или синтезируемые в организме и являющиеся источником витаминов; например, из 7-дегидрохолестерола под влиянием ультрафиолетовых лучей образуется витамин D3.
Гормоны
Гормоны – биологически активные вещества, синтезируемые в незначительных количествах эндокринными железами и клетками диффузно-эндокринной системы. Гормоны осуществляют гуморальную регуляцию обмена веществ и имеют различную химическую структуру. Уникальность гормональной регуляции обусловлена соподчинённостью работы желёз внутренней секреции, ауторегуляцией выработки гормонов и агонизмом-антагонизмом их действия относительно друг друга. Существует строгая иерархия или соподчиненность гормонов Поддержание уровня гормонов в организме в большинстве случаев обеспечивает механизм отрицательной обратной связи (см. рисунок).
Согласно классификации по химическому строению различают 4 группы гормонов:
1. Гормоны – производные аминокислот
адреналин, норадреналин, тироксин, трийодтиронин.
2. Пептидные гормоны
адренокортикотропный гормон (АКТГ), соматотропный гормон, тиреотропный гормон (ТТГ), лактотропный гормон (пролактин), лютеинизирующий гормон, фолликулостимулирующий гормон, меланоцитстимулирующий гормон, антидиуретический гормон (АДГ, вазопрессин), окситоцин, кальцитонин, паратгормон, инсулин, глюкагон.
3. Стероидные гормоны
кортизол, альдостерон, эстрадиол, прогестерон, тестостерон, кальцитриол.
4. Эйкозаноиды
простагландины, лейкотриены, тромбоксаны
Для проявления биологической активности гормона, обязательным условием является его взаимодействие с рецепторами. Существуют два основных механизма действия гормонов на уровне клетки: реализация эффекта через рецептор, расположенный на мембране и реализация эффекта через рецептор, расположенный внутри клетки.
Для реализации мембранного механизма важнейшую роль в клетке приобретают вторичные посредники (мессенджеры) – это внутриклеточные низкомолекулярные молекулы, регулирующие скорость метаболических процессов в клетке и образующиеся в ответ на связывание гормона с мембранным рецептором (ионы Са2+, 3,5 – цАМФ, 3,5 – цГМФ, инозитол-1,4,5-трифосфат, монооксид азота (NО)).
На практике, всегда следует учитывать возможные результаты взаимодействия совместной работы гормонов.
Синергизм – однонаправленное действие двух или нескольких гормонов. Например, адреналин и глюкагон активируют распад гликогена печени до глюкозы и вызывают увеличение уровня сахара в крови.
Антагонизм всегда относителен. Например, инсулин и адреналин оказывают противоположные действия на содержание глюкозы в крови. Инсулин вызывает гипогликемию, адреналин – гипергликемию. Биологическое же значение этих эффектов сводится к одному – улучшению углеводного питания тканей.
В медицинской практике гормональные препараты используют для лечения заболеваний желез внутренней секреции. Так, например, инсулин применяют для лечения диабета.
План описания гормона:
• Химическое название, классификационная характеристика (липофильный, гидрофильный и др.)
• Химическое строение (химическая формула, составные части (подписать))
* для пептидных гормонов указывается – пептидный (количество аминокислотных звеньев)
• Особенности синтеза и секреции и биотрансформации (место синтеза, схема синтеза, регуляция синтеза и секреции, инактивация и выведение гормона)
• Биохимические функции
(а) механизм действия (схема или рисунок),
б) мишени и эффекты)
• Описание гипофункции и гиперфункции эндокринной железы, синтезирующей данный гормон (названия заболеваний, основные симптомы)
Основные термины раздела:
Гормон(ы) – группа биологически активных веществ различной химической природы, секретируемых в кровь эндокринными железами в крайне малых количествах и оказывающих регулирующее действие на метаболические процессы в клетках вне места образования; недостаточное или избыточное выделение гормонов сопровождается развитием эндокринных заболеваний.
Нейромедиатор (нейротрансмиттер) – химический посредник, освобождающийся из пресинаптического нервного окончания и передающий нервный импульс в синапсе постсинаптичсскому окончанию, мышечному волокну или железе, которые эти нервы иннервируют.
Нейромедиаторы центральной нервной системы
• ацетилхолин,
• норадреналин,
• дофамин,
• серотонин,
• Ɣ-аминомасляная кислота (ГАМК)
Нейромедиаторы периферической нервной системы
• ацетилхолин
• норадреналин
Рецептор – высокомолекулярное вещество, специфически связывающееся с конкретным лигандом, например, гормоном. В качестве рецепторов, как правило, выступают гликопротеины, имеющие доменную структуру. Выделяют два класса рецепторов – мембранные и ядерные.
1.2. Формулы биоорганических соединений и их метаболитов
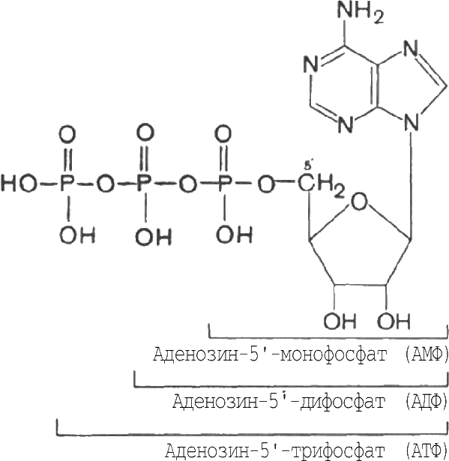
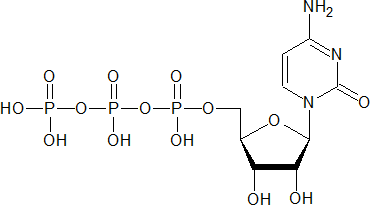
Аденозинтрифосфат (АТФ, аденозинтрифосфорная кислота) – нуклеозидтрифосфат содержащий аденин, рибозу и три остатка фосфорной кислоты.
α-Аланин (α-аминопропионовая кислота) – протеиногенная заменимая аминокислота.
CH3CH(NH2)COOH
β-Аланин (β-аминопропионовая кислота) – непротеиногенная аминокислота, входящая в состав пантотеновой кислоты и некоторых природных дипептидов (карнозина и ансерина).
Н2NCH2CH2COOH
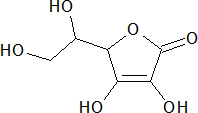
Аскорбиновая кислота (витамин С) – водорастворимый витамин, участвующий в окислительно-восстановительных реакциях (витамин-антиоксидант), кофактор ферментов лизил- и пролилгидроксилаз; при недостатке витамина С в организме развивается цинга.
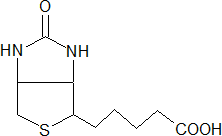
Биотин (витамин Н) – водорастворимый витамин, который в активной форме (биоцитин) способен акцептировать и отдавать углекислый газ и таким образом участвовать в реакциях карбоксилирования при синтезе высших жирных кислот, оксалоацетата и др.
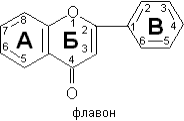
Биофлавоноиды (витамин Р) – органические вещества, производные хромана или флавана, способные уменьшать проницаемость кровеносных сосудов (представлены катехинами, флаванонами, флавонами).
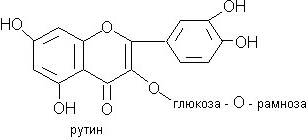
Глицин (аминоуксусная кислота) – заменимая аминокислота, входящая в состав многих фибриллярных белков (коллагена, эластина и др.), активных центров ряда ферментов и участвующая в биосинтезе глутатиона, креатина, гема, пуриновых оснований, а также в реакциях конъюгации.
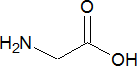
Глутамин – моноамид глутаминовой кислоты, образующийся в тканях мозга, энтероцитах и других клетках при связывании аммиака с глутаминовой кислотой; участвует в биосинтезе пуриновых и пиримидиновых нуклеотидов, аминосахаров.
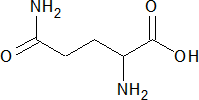
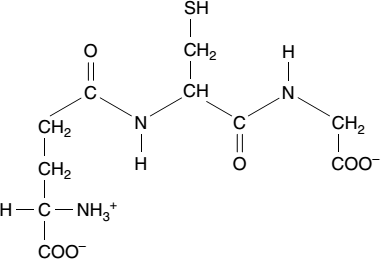
Глутатион – трипептид, состоящий из остатков цистеина, глицина и глутаминовой кислоты и участвующий в окислительно-восстановительных реакциях (аминокислотные остатки Глу и Цис связаны γ-пептидной связью).
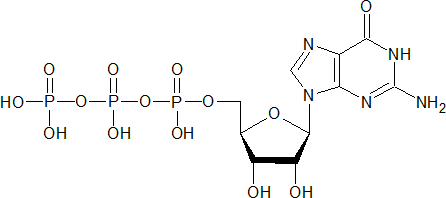
Гуанозинтрифосфат (ГТФ) – нуклеотид, в состав которого входит гуанозин, связанный с тремя молекулами фосфорной кислоты; в реакциях фосфорилирования является донором фосфата; предшественник циклического гуанозинмонофосфата (цГМФ), материал для синтеза нуклеиновых кислот.
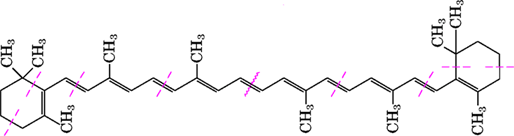
Каротин (β-каротин) – изопреноид, оранжево-желтый пигмент растительного происхождения, растворимый в жирах (молекула β-каротина в организме путем окислительного расщепления превращается в две молекулы ретиналя – витамина A).
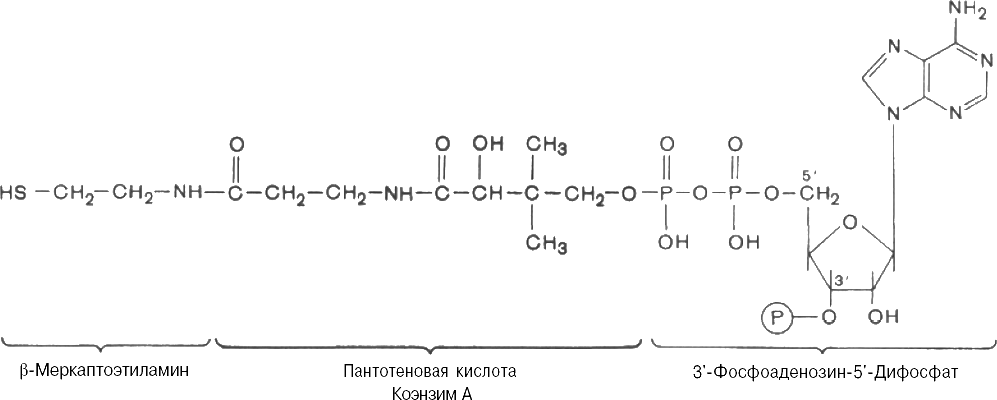
Кофермент А (коэнзим A, HS-KoA) – кофермент нуклеотидной природы, соединение, состоящее из 3'-аденозин-5' – дифосфата, пантотеновой кислоты и β-меркаптоэтиламина; участвует в активации ацильных радикалов.
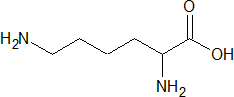
Лизин – незаменимая для организма человека аминокислота с положительно заряженным радикалом, содержащаяся почти во всех белках.
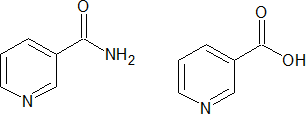
Ниацин (витамин РР) – группа органических соединений, относящихся к водорастворимым витаминам, включающая никотиновую кислоту и амид никотиновой кислоты; в организме человека никотинамид превращается в никотинамидные коферменты (НАД и НАДФ); недостаточное поступление с пищей ниацина приводит к развитию пеллагры, характеризующейся диареей, специфическим дерматитом и слабоумием.
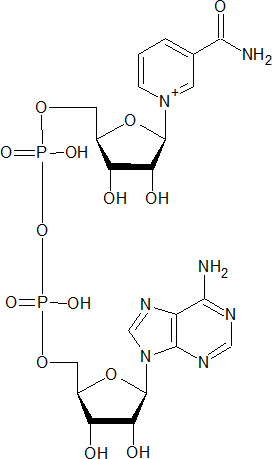
Никотинамидадениндинуклеотид (НАД+) – кофермент дегидрогеназ (оксидоредуктаз), состоящий из никотинамидного и аденилового нуклеозидов, связанных через остатки фосфорной кислоты; окисленная форма НАД+ способна восстанавливаться до НАДН(H+).
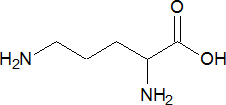
Орнитин – непротеиногенная диаминомонокарбоновая аминокислота, промежуточный продукт цикла мочевинообразования.
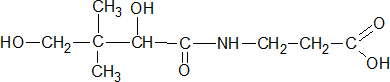
Пантотеновая кислота – водорастворимый витамин группы В, структурный компонент кофермента А и 4 -фосфопантетеина; при недостатке пантотеновой кислоты в организме развиваются дерматиты, депигментация и выпадение волос.
Пиридоксальфосфат (пиридоксаль-5-фосфат) – биологически активная форма пиридоксина (витамина В6), в составе ферментов участвует в реакциях обмена аминокислот (трансаминирование, декарбоксилирование).
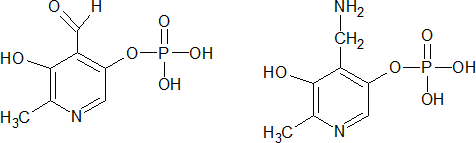
Пиридоксин (витамин В6) – водорастворимый витамин группы В, превращающийся в организме путем фосфорилирования в коферментные формы – пиридоксальфосфат и пиридоксаминфосфат; при недостатке пиридоксина наблюдаются себорейный дерматит, эпилептиформные судороги, глоссит, конъюнктивит.
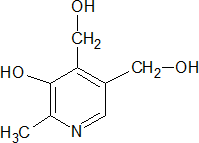
Пролин – заменимая аминокислота входит в состав большинства белков; особенно богаты пролином белки коллаген, эластин.
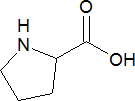
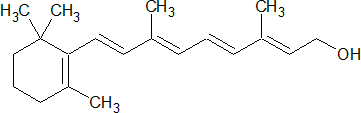
Ретиналь – изопреноид, альдегидная форма витамина А1, присутствует в белке родопсине в виде цис-ретиналя, который в процессе светоощущения изомеризуется в транс-ретиналь; дефицит ретиналя обусловливает нарушение темновой адаптации.
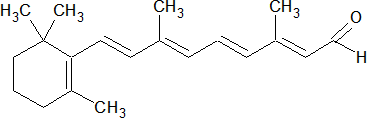
Ретиноевая кислота – изопреноид, биологически активная группа витамина А1, содержащая карбонильную группу; влияет на процессы транскрипции в клетках эпителиальных тканей.
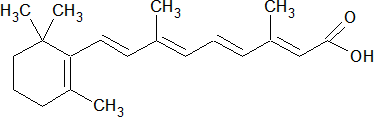
Ретинол (витамин А) – изопреноид, жирорастворимый витамин, являющийся циклическим непредельным одноатомным спиртом, образуется в организме человека из поступающих с пищей каротиноидов; недостаток ретинола в приводит к гемералопии, ксерофтальмии и др.
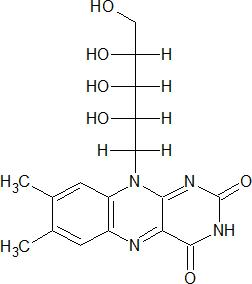
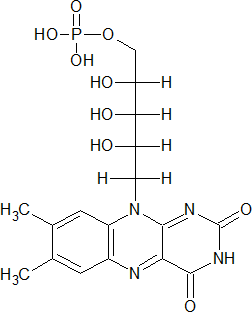
Рибофлавин (витамин В2) – водорастворимый витамин, входящий в состав флавопротеинов; в организме человека превращается в коферменты: флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД), участвующие в редокс-процессах; при недостаточном поступлении в организм рибофлавина развиваются катаракта, глоссит, хейлит, заеды и др.
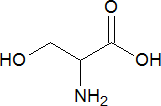
Серин – заменимая протеиногенная гидроксилсодержащая аминокислота, присутствует в составе активных центров многих ферментов, участвует в биосинтезе глицина, метионина, цистеина, боковой цепи триптофана, а также сфинголипидов и этаноламина.
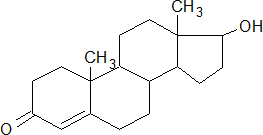
Тестостерон – производное холестерина, мужской половой гормон стероидной природы; синтезируется в яичках, плаценте и надпочечниках; влияет на развитие вторичных половых признаков по мужскому типу, регулирует сперматогенез и половое поведение, оказывает анаболическое действие.
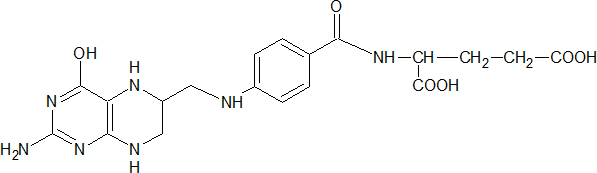
Тетрагидрофолиевая кислота (ТГФК) – активная форма фолиевой кислоты, образующаяся в реакции восстановления птеридинового кольца; производные ТГФК участвуют в реакциях переноса одноуглеродных групп.
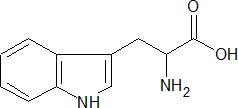
Тиамин (витамин В1) – водорастворимый витамин, составная часть кофермента тиаминдифосфата; недостаточное поступление в организм тиамина сопровождается поражением нервной и мышечной систем, желудочно-кишечного тракта (заболевание бери-бери).
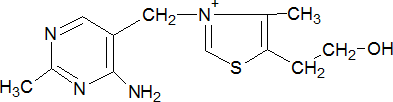
Тиаминдифосфат (тиаминпирофосфат, ТДФ, ТПФ) – фосфорилированная форма витамина тиамина; кофермент ряда ферментов, катализирующих реакции окислительного декарбоксилирования α-кетокислот и переноса двууглеродного фрагмента от молекул моносахаридов – кетоз на другие молекулы – альдозы.
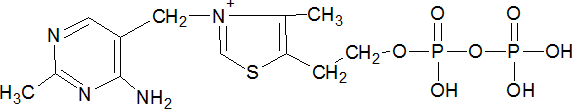
Тирозин – ароматическая условно незаменимая аминокислота, образуется из фенилаланина путем гидроксилирования; из тирозина образуются катехоламины (адреналин, норадреналин), меланины, йодсодержащие гормоны щитовидной железы (тироксин, трийодтиронин).
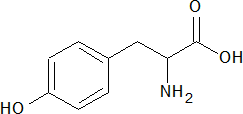
Треонин – гидроксилсодержащая алифатическая незаменимая для человека аминокислота, входит в состав многих белков.
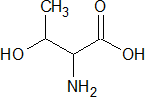
Триптофан – гетероциклическая незаменимая для человека аминокислота, производное индола; входит в состав многих белков; из триптофана образуются серотонин, мелатонин, частично, НАД+
Убихинон (кофермент Q) – изопреноид, жирорастворимое вещество с антиоксидантной функцией; в дыхательной цепи убихинон присоединяет электроны с I и II комплексов и передает их на цитохромы III комплекса.
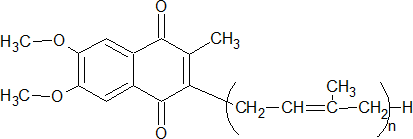
Уридиндифосфат (уридиндифосфорная кислота, УДФ) – соединение уридина с двумя остатками фосфорной кислоты; составная часть коферментов, участвующих в переносе остатков моносахаридов или их производных.
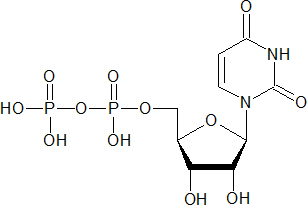
Филлохинон (витамин К, антигеморрагический) – производное нафтохинона, кофактор фермента глутамилкарбоксилазы, участвующего в синтезе остатков γ-карбоксиглутаминовой кислоты в кальцийсвязывающих белках; при недостатке витамина К возникают самопроизвольные кровотечения.
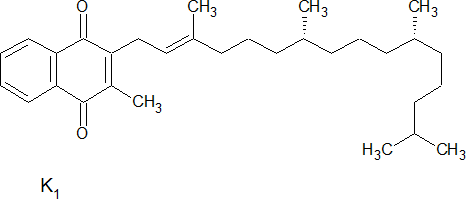
Флавинадениндинуклеотид (ФАД) – производное рибофлавина (витамина В2), состоящее из двух нуклеотидов – аденозинмонофосфата и флавинмононуклеотида; кофермент оксидоредуктаз, способный обратимо связывать два атома водорода.
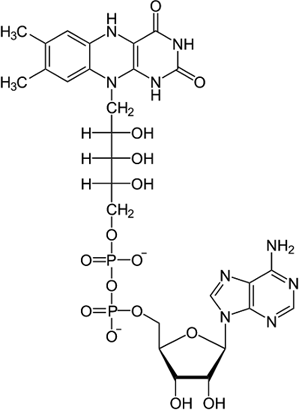
Флавинмононуклеотид (ФМН) – производное рибофлавина (витамин В2), в котором остаток рибитола этерифицирован фосфорной кислотой; простетическая группа белков флавопротеинов, составляющая часть флавинадениндинуклеотида.
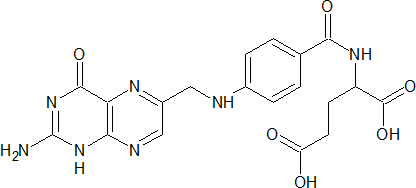
Фолиевая кислота (птероилглутаминовая кислота, витамин В9, витамин Вс) – водорастворимый витамин, содержащий птеридин, остаток парааминобензойной кислоты (ПАБК) и L-глутаминовой кислоты (Глу); при восстановлении образует гидрированную форму – кофермент тетрагидрофолиевую кислоту (ТГФК); участвует переносе одноуглеродных фрагментов, при недостаточном поступлении фолиевой кислоты с пищей развивается мегалобластная анемия, поражение слизистых оболочек, глосситы, нарушение заживления ран.
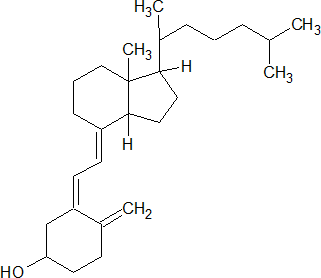
Холекальциферол (витамин D3) – жирорастворимый витамин группы D, производное 7-дегидрохолестерола
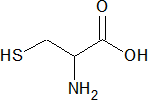
Цистеин – заменимая серосодержащая аминокислота входит в состав белков, пептидов (глутатиона) и др.
Цитидинтрифосфат (ЦТФ) – нуклеотид, содержащий цитидин и три остатка фосфорной кислоты.
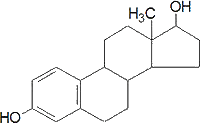
Эстрадиол – производное холестерина, стероидный гормон из группы женских половых гормонов эстрогенов, секретируемый фолликулами яичников.
1.3. Вопросы для самоконтроля по теме раздела
✓ Перечислите функции белков.
✓ Перечислите методы выделения и очистки белков из биообъектов.
✓ Дайте определение понятиям: высаливание, хроматография, электрофорез, кристаллизация.
✓ Перечислите физико-химические свойства аминокислот.
✓ Составьте формулы аминокислот, образующихся в результате постсинтетической химической модификации (оксилизин, селеноцистеин, ɣ-карбоксиглутаминовая кислота, 3,5-дийодтирозин).
✓ Перечислите химические реакции для открытия и определения аминокислот в гидролизатах белков.
✓ Перечислите физико-химические свойства белков.
✓ Дайте определение понятиям: денатурация, иозоэлектрическая точка, изоионная точка, лактамная (кетонная) форма, лактимная (енольная) форма.
✓ Перечислите методы определения первичной структуры белков.
✓ Опишите вторичную структуру белка.
✓ Дать определение понятиям: протомер (мономер, субъединица), олигомер (мультимер), изофермент, комплементарность.
✓ Назовите примеры простых белков
✓ Приведите примеры природных пептидов.
✓ Опишите гемопротеины.
✓ Опишите флавопротеины.
✓ Опишите нуклеопротеины.
✓ Опишите липопротеины.
✓ Перечислите фосфопротеины.
✓ Дать определение понятиям: гликоконьюгаты, гликобиология, гликопатология, гликотерапия.
✓ Опишите интерфероны и иммуноглобулины
✓ Опишите трансферрин и гемосидерин.
✓ Перечислите методы выделения нуклеиновых кислот из биообъектов.
✓ Составьте формулы минорных нуклеотидов пуринового ряда (инозин, ксантин, гипоксантин, 7-метилгуанозин).
✓ Перечислите минорные пиримидиновые основания.
✓ Каковая первичная структура нуклеиновых кислот?
✓ Какова вторичная структура нуклеиновых кислот?
✓ Дайте определение понятию «Фермент» (энзим).
✓ Назовите области применения ферментов.
✓ Дать определение понятиям: холофермент, простетическая группа, апофермент, кофермент, активный центр фермента, аллостерический центр, синзимы.
✓ Приведите примеры изоферментов.
✓ Опишите механизм действия ферментов.
✓ Что такое энергия активации, константа диссоциации фермент-субстратного комплекса, явление насыщения, константа Михаэлиса, уравнение Лайнуивера-Бэрка.
✓ Перечислите основные свойства ферментов.
✓ Что такое относительная и абсолютная специфичность ферментов?
✓ Приведите примеры стереохимической специфичности.
✓ Каковы типы ингибирования ферментов?
✓ Дайте определение понятиям: индуцированный синтез ферментов, конститутивные ферменты, летальный синтез, проферменты (зимогены), ингибирование по принципу обратной связи, ретроингибирование, активация предшественником, компартментализация.
✓ Как рассчитать удельную активность фермента, молекулярную активность фермента?
✓ Какова международная классификация ферментов?
✓ Перечислите основные направления медицинской энзимологии.
✓ Дайте определение понятию «Липиды».
✓ Какова классификация липидов?
✓ Перечислите функции липидов.
✓ Дайте определение понятиям: «Жирная кислота», «Высшая жирная кислота».
✓ Приведите примеры диеновых и и триеновых жирных кислот.
✓ Составьте формулу тетраеновой жирной кислоты.
✓ Составьте формулу триацилглицерола (ТАГ) с остатком олеиновой, линолевой и пальмитиновой кислот.
✓ Напишите пример формулы липида из класса «Воски».
✓ Составьте общий план строения фосфолипидов.
✓ Составьте общий план строения сфинголипидов.
✓ Перечислите биологические функции глицерофосфолипидов.
✓ Перечислите биологические функции сфингофосфолипидов.
✓ Составьте формулу липида с остатком N-ацетилнейраминовой кислоты, дайте ему название.
✓ Перечислите стероидные соединения. Что является признаком стероидных соединений?
✓ Составьте формулу холестерина и дайте характеристику этому соединению.
✓ Составьте формулу желчной кислоты и её коньюгата, объясните биологическую роль желчных кислот.
✓ Дайте определение понятию «Витамины». Какова классификация витаминов?
✓ Перечислите методы определения витаминов в биожидкостях.
✓ Дайте характеристику витамину «Аскорбиновая кислота». Какими методами можно обнаружит этот витамин в биологических объектах?
✓ Дайте характеристику витамину «Тиамин» (строение витамина а кофермента, биологические функции, признаки авитаминозов, особенности применения в медицине).
✓ Опишите особенности химической структуры и биологические свойства рибофлавина.
✓ Опишите особенности химической структуры и биологические свойства цианокобаламина.
✓ Составьте описание особенностей структуры, биологической активности и признаков гипо- и авитаминоза для ретинола.
✓ Составьте описание особенностей структуры, биологической активности и признаков гипо- и авитаминоза для кальциферола.
✓ Составьте формулу НАД и покажите его переход из окисленной формы в восстановленную.
✓ Составьте формулу ФАД и покажите его переход из окисленной формы в восстановленную.
✓ Перечислите витаминоподобные соединения.
✓ Назовите известные вам антивитамины.
✓ Какова биологическая роль нижеперечисленных соединений: ПАБК, пангамовая кислота, инозитол, убихинон, S-метилметионин, липоевая кислот, холин
✓ Какова классификация гормонов?
✓ Дайте характеристику гормонов гипоталамуса.
✓ Дайте характеристику гормонов гипофиза.
✓ Дайте характеристику гормонов паращитовидных желез.
✓ Дайте характеристику гормонов щитовидной железы.
✓ Дайте характеристику гормонов поджелудочной железы.
✓ Дайте характеристику гормонов надпочечников.
✓ Дайте характеристику женских половых гормонов.
✓ Дайте характеристику мужских половых гормонов.
✓ Опишите структуру и биологические свойства простагландинов.
✓ Опишите аденилатциклазную мессенджерную систему.
✓ Опишите гуанилатциклазную мессенджерную систему.
✓ Опишите Ca2+– мессенджерную систему.
✓ Опишите механизм действия на клетку адреналина.
✓ Опишите механизм действия на клетку инсулина.
✓ Опишите механизм действия на клетку тестостерона.
✓ Опишите типичное проявление авитаминоза (по выбору).
✓ Опишите типичное проявление гипофункции железы (по выбору).
✓ Опишите типичное проявление гиперфункции железы (по выбору).
✓ Что такое эйкозаноиды?
✓ Объясните биологические эффекты простагландинов, лейкотриенов и тромбоксанов.







