С. Н. Филимонов
Клиника, диагностика и лечение основных ревматических болезней
УСЛОВНЫЕ СОКРАЩЕНИЯ
АГ – артериальная гипертензия
АД – артериальное давление
АЛАТ – аланиновая аминотрансфераза
АНА – антинуклеарные антитела
АНФ – антинуклеарный фактор
АНЦА – антинейтрофильные цитоплазматические антитела
АПФ – ангиотензин-превращающий фермент
АСАТ – аспарагиновая аминотрансфераза
АТ – антитела
АТА – антитопоизомеразные антитела
АФЛ – антитела к фосфолипидам
АФЛС – антифосфолипидный синдром
АЦА – антицентроизомерные антитела
АЭА – антитела к эндомизию класса IgA
ВИЧ – вирус иммунодефицита человека
ВОЗ – Всемирная организация здравоохранения
ГКС – глюкокортикостероид
ДВС – диссеминированное внутрисосудистое свертывание
ДЗСТ – диффузные заболевания соединительной ткани
ЖКТ – желудочно-кишечный тракт
ИБС – ишемическая болезнь сердца
ИЭ – инфекционный эндокардит
КФК – креатинфосфокиназа
ЛС – лекарственные средства
ЛФК – лечебная физкультура
МКБ-10 – Международная классификация болезней 10-го пересмотра
МРТ – магнитно-резонансная томография
МСЭ – медико-социальная экспертиза
НК – недостаточность кровообращения
НПВС – нестероидное противоспалительное средство
ОРЛ – острая ревматическая лихорадка
ПМК – пролапс митрального клапана
ПсА – псориатический артрит
ПЦР – полимеразная цепная реакция
РА – ревматоидный артрит
РеА – реактивный артрит
РКО – Российское кардиологическое общество
РНП – рибонуклеопротеин
РФ – ревматоидный фактор
СВ – системный васкулит
СКВ – системная красная волчанка
СОЭ – скорость оседания эритроцитов
СРБ – С-реактивный белок
ССД – системная склеродермия
ССС – сердечно-сосудистая система
УП – узелковый полиартериит
УФО – ультрафиолетовое облучение
ФК – функциональный класс
ФПП – функциональные пробы печени
ФЭГДС – фиброэзофагогастродуоденоскопия
ХПН – хроническая почечная недостаточность
ХРБС – хроническая ревматическая болезнь сердца
ЦИК – циркулирующий иммунный комплекс
ЦНС – центральная нервная система
ЦОГ-1 – циклооксигеназа-1
ЦОГ-2 – циклооксигеназа-2
ЧСС – частота сердечных сокращений
ЭКГ – электрокардиография
ЭхоКГ – эхокардиография
CREST-синдром – синдром при сочетании кальциноза (С), синдрома Рейно (R), эзофагита (Е), склеродактилии (S) и телеангиоэктазии (Т)
HLA – (human leucocyte antigens) человеческие лейкоцитарные антигены
IgA – иммуноглобулин класса A
IgG – иммуноглобулин класса G
IgM – иммуноглобулин класса M
IL-1 – интерлейкин-1
IL-2 – интерлейкин-2
IL-6 – интерлейкин-6
pANCA – перинуклеарные антитела к антигенам цитоплазмы
ПРЕДИСЛОВИЕ
Выделение большого числа так называемых ревматических болезней, объединенных по принципу преимущественного поражения опорно-двигательного аппарата, способствовало формированию современной ревматологии в качестве самостоятельного раздела медицины.
Понятие «ревматические болезни» охватывает разнообразные по происхождению заболевания преимущественно системного, реже локального, характера, протекающие со стойким или преходящим суставным синдромом. Обоснованием для объединения этих многочисленных болезней в одну группу явилось то, что в их основе лежит преимущественное поражение соединительной ткани, как плотной (дермы, сухожильно-связочного аппарата, хрящевой, костной ткани и др.), так и ее специальных типов (синовиальных и серозных оболочек, базальных мембран сосудов и эпителия и др.).
Перечисленные анатомические структуры наиболее часто вовлекаются в патологический процесс при ревматических болезнях, а их отличительной особенностью является системное поражение соединительной ткани воспалительного или дистрофического генеза. Степень тяжести заболеваний различна: от легкой локальной боли до тяжелых, опасных для жизни заболеваний (например, системная красная волчанка).
В пособии освещены вопросы клиники, диагностики и лечения основных ревматических заболеваний, с которыми чаще всего сталкиваются в своей практике врачи первого контакта (терапевт и врач общей практики).
Глава 1
РЕВМАТИЗМ. ОСТРАЯ РЕВМАТИЧЕСКАЯ ЛИХОРАДКА
Определение. Длительное время под ревматизмом понимались все заболевания, при которых страдали органы опоры и движения: суставы, мышцы, мягкие ткани и др. В последние десятилетия вместо термина «ревматизм» в этом значении стало употребляться словосочетание «ревматические болезни».
Другое значение термина «ревматизм» – самостоятельное заболевание, которое связано со стрептококковой инфекцией, с поражением суставов, сердца, нервной системы и других органов. Однако в современной медицинской литературе использование термина «ревматизм» в этом значении вытеснено общепринятым во всем мире термином «острая ревматическая лихорадка».
Острая ревматическая лихорадка (ОРЛ) – постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных бета-гемолитическим стрептококком группы A. ОРЛ проявляется в виде системного воспалительного заболевания соединительной ткани с преимущественным поражением сердечно-сосудистой системы (ССС) (кардит), суставов (мигрирующий полиартрит), центральной нервной системы (ЦНС) (хорея) и кожи (кольцевидная эритема, ревматические узелки) и развивается у предрасположенных лиц (главным образом в возрасте 7 – 15 лет) в связи с аутоиммунным ответом макроорганизма на антигены стрептококка группы А и перекрестной реактивностью антител (АТ) со схожими аутоантигенами тканей человека (феномен молекулярной мимикрии). В МКБ-10 соответствует рубрикам I00 – I02 «Острая ревматическая лихорадка».
Хроническая ревматическая болезнь сердца (ХРБС) – заболевание, характеризующееся поражением клапанов сердца в виде краевого фиброза клапанных створок или порока сердца (недостаточности и/или стеноза), сформировавшихся после перенесенной ОРЛ. В МКБ-10 соответствует рубрикам I05 – I09 «Хроническая ревматическая болезнь сердца».
Эпидемиология. Заболеваемость ОРЛ в России составляет 2,7 случая на 100 тыс. населения, ХРБС – 9,7 случая (в том числе ревматическими пороками сердца – 7,64 случая). Распространенность ХРБС у детей достигает 45 случаев на 100 тыс. населения, а у взрослых – 260 случаев. Лица мужского и женского пола заболевают с одинаковой частотой, преимущественно в возрасте 7 – 15 лет.
Настороженность врачей в отношении возможных вспышек ОРЛ должна быть постоянной в связи с неснижающимися показателями первичной заболеваемости ХРБС. Подавляющее большинство в данной категории составляют пациенты с приобретенными ревматическими пороками сердца. К концу последнего десятилетия прошлого века в России ежегодно выявляли на 2,5 тыс. больных с ХРБС больше, чем в начале регистрации (1994 г.).
К причинам, предрасполагающим к возможным вспышкам ОРЛ, относятся:
– недостаточное лечение больных с ангиной и фарингитом стрепток окковой этиологии;
– недостаточное знание клинических симптомов острой фазы болезни в связи с тем, что она редко встречается в настоящее время;
– ослабление настороженности врачей в отношении этого заболевания;
– неполное обследование больных с подозрением на ревматическую лихорадку;
– изменение вирулентности «ревматогенного» стрептококка.
Этиология. Острая ревматическая лихорадка развивается после заболеваний, вызванных «ревматогенными» штаммами бета-гемолитического стрептококка (М1, М3, М5, М18, М24), которые обладают высокой контагиозностью, тропностью к носоглотке, индукцией типоспецифических АТ. «Ревматогенные» стрептококки содержат эпитопы, способные перекрестно реагировать с различными тканями макроорганизма-хозяина: миозином и сарколеммальной мембраной, синовией и мозгом, т. е. теми структурами, которые вовлекаются в патологический процесс при ОРЛ.
Генетические факторы. В семьях больных ОРЛ и ХРБС склонность к гипериммунному противострептококковому ответу и распространенность заболевания и ревматических пороков сердца выше, чем в общей популяции, особенно среди членов семьи первой степени родства.
Патогенез. В сложном патогенезе развития классических проявлений ОРЛ наибольшее значение придается иммунному воспалению, иммунопатологическим процессам, в которых стрептококковые антигены и АТ принимают активное участие, однако и токсическая концепция вносит определенную лепту в понимание начальных проявлений ОРЛ. Таким образом, развитие ОРЛ определяется:
– прямым токсическим повреждением миокарда «кардиотропными» ферментами бета-гемолитического стрептококка группы А;
– иммунным ответом на артериальную гипертензию (АГ) бетагемолитического стрептококка группы А, приводящим к синтезу противострептококковых антител (АТ), перекрестно реагирующих с АТ поражаемых тканей человека (феномен молекулярной мимикрии).
Патоморфология. Выделяют четыре стадии патологического процесса в соединительной ткани: мукоидное набухание, фибр ин оидные изменения, пролиферативные реакции, склероз. Пролиферативные реакции сопровождаются образованием ревматической гранулемы (Ашоффа – Талалаева).
Классификация.
Клинические формы:
– ОРЛ;
– повторная ревматическая лихорадка.
Исходы:
– выздоровление.
– ХРБС:
без порока сердца;
с пороком сердца.
Недостаточность кровообращения:
– по классификации Н. Д. Стражеско и В. Х. Василенко (стадии 0, I, IIA, IIБ, III);
– по классификации Нью-Йоркской кардиологической ассоциации (функциональные классы 0, I, II, III, IV).
Клиника. По поводу ревматизма образно выразился французский врач Э. Ш. Ласег: «Ревматизм лижет суставы, плевру и даже мозговые оболочки, но больно кусает сердце». Смысл этого высказывания заключается в том, что поражение суставов, плевры и оболочек мозга хотя и может проявляться очень ярко, но не имеет отдаленных последствий. Поражение сердца, хотя и может протекать незаметно в начале болезни, но приводит к формированию пороков сердца – нарушению работы его клапанов, которые имеют серьезнейшие осложнения и значительно ухудшают прогноз.
Клинические проявления ОРЛ:
– основные: кардит, артрит, хорея, кольцевидная эритема, ревматические узелки;
– дополнительные: лихорадка, артралгия, абдоминальный синдром, серозиты.
В дебюте клиническая картина заболевания зависит от возраста пациентов. Через 2 – 3 нед. после перенесенной ангины у большинства детей заболевание начинается с внезапного повышения температуры до фебрильных цифр, появления симметричных мигрирующих болей в крупных суставах (чаще всего коленных) и признаков кардита (боли в левой половине грудной клетки, одышка, сердцебиение и др.). У остальных детей наблюдают моносиндромное течение с преобладанием признаков артрита или кардита, редко хореи.
Остро, по типу вспышки, ОРЛ развивается у школьников среднего возраста и солдат-новобранцев, перенесших эпидемическую ангину, вызванную бета-гемолитическим стрептококком группы A.
Для подростков и молодых людей характерно постепенное начало – после стихания клинических проявлений ангины появляются субфебрильная температура, артралгии в крупных суставах или только умеренные признаки кардита.
Повторная атака ОРЛ провоцируется инфекцией, вызванной бетагемолитическим стрептококком группы A и проявляется преимущественно развитием кардита.
Объективное обследование. Температурная реакция варьирует от субфебрилитета до лихорадки.
Обследование кожи. К основным признакам ОРЛ относятся кольцевидная эритема и подкожные ревматические узелки.
Кольцевидная эритема – бледно-розовые кольцевидные высыпания (диаметром от нескольких миллиметров до 5 – 10 см) на туловище и проксимальных отделах конечностей, но не на лице, не сопровождающиеся зудом, не возвышающиеся над поверхностью кожи, не оставляющие после себя следов; характерный, но редкий (4 – 17 % всех случаев ОРЛ) признак.
Подкожные ревматические узелки – округлые плотные малоподвижные безболезненные мелкие узелки, расположенные в местах прикрепления сухожилий в области коленных, голеностопных, локтевых суставов или затылочной кости; характерный, но крайне редкий (1 – 3 % всех случаев ОРЛ) симптом.
Несмотря на значительное снижение частоты кольцевидной эритемы и ревматических узелков у больных детей и их фактическое отсутствие у подростков и взрослых пациентов, специфичность данных синдромов при ОРЛ остается высокой, и они сохраняют свою диагностическую значимость.
Обследование суставов. При ОРЛ для суставного синдрома характерны:
– вовлечение в патологический процесс преимущественно коленных, голеностопных, лучезапястных, локтевых суставов;
– доброкачественность (деформации не развиваются), летучесть клинических проявлений, переменное, часто симметричное вовлечение суставов;
– преобладающая форма поражения – олигоартрит, реже – моноартрит;
– полиартралгии (мигрирующая боль в крупных суставах различной интенсивности) отмечаются в 10 – 15 % случаев, не сопровождаются ограничением движений, болезненностью при пальпации и другими симптомами воспаления;
– быстрое разрешение суставного синдрома на фоне приема нестероидных противовоспалительных средств (НПВС).
Исследование сердечно-сосудистой системы. Кардит – ведущий синдром ОРЛ, выявляющийся в 90 – 95 % случаев и определяющий тяжесть течения заболевания и его исход. Ведущим компонентом кардита считается вальвулит (преимущественно митрального, реже – аортального клапана), проявляющийся органическим сердечным шумом, возможно, в сочетании с миокардитом и перикардитом.
Аускультативные симптомы ревматического вальвулита
1. Систолический шум обусловлен митральной регургитацией. Оптимально выслушивается на верхушке сердца и проводится в левую подмышечную область. По характеру длительный дующий, связан с I тоном и занимает бо́льшую часть систолы. Имеет разную интенсивность, особенно на ранних стадиях заболевания. Не зависит от положения тела и фазы дыхания.
2. Мезодиастолический шум (низкочастотный) выслушивают на верхушке сердца в положении больного на левом боку при задержке дыхания на выдохе (при наличии острого кардита с митр альной регургитацией). Шум часто следует за III тоном или заглушает его.
3. Протодиастолический шум возникает при аортальной регургитации, начинается сразу после II тона, часто сочетается с систолическим шумом и имеет высокочастотный дующий убывающий характер. Шум лучше всего прослушивается вдоль левого края грудины после глубокого выдоха при наклоне больного вперед.
Для ОРЛ не характерно изолированное поражение аортального клапана, без возникновения шума митральной регургитации. Поражение сердца по типу миокардита и перикардита при отсутствии вальвулита считается маловероятным при ОРЛ и является показанием для проведения тщательной дифференциальной диагностики с кардитами иной этиологии (в первую очередь вирусной).
Важнейшая особенность вальвулита при первой атаке ОРЛ – четкая положительная динамика под влиянием активной антиревматической терапии. В преобладающем большинстве случаев на фоне лечения происходит нормализация частоты сердечных сокращений, восстановление звучности тонов, уменьшение интенсивности систолического и диастолического шумов, сокращение границ сердца, исчезновение симптомов недостаточности кровообращения.
Обследование ЦНС. При осмотре выявляют признаки малой хореи (в 6 – 30 % случаев): гиперкинезы, мышечная гипотония (вплоть до дряблости мышц с имитацией параличей), нарушения статики и координации, сосудистая дистония, психоэмоциональные нарушения (неустойчивость настроения, раздражительность, плаксивость и т. д.). Ревматическая хорея (малая хорея, хорея Сиденгама) диагностируется у 6 – 30 % больных детей и редко – у подростков. Чаще наблюдаются такие поражения у девочек и девушек. У 5 – 7 % пациентов хорея может выступать единственным признаком ОРЛ.
Поражения серозных оболочек в настоящее время встречаются редко, только при тяжелом течении первой атаки и/или повторной ревматической лихорадке, и проявляются преимущественно абдоминальным синдромом разной интенсивности с быстрым обратным развитием на фоне противовоспалительной терапии.
Осложнения. Исходом эндокардита служит формирование ревматических пороков сердца. Частота их развития после первой атаки ОРЛ у детей составляет 20 – 25 %. Преобладают изолированные пороки, чаще митральная недостаточность. Реже формируются недостаточность аортального клапана, митральный стеноз и комбинированный порок митрального и аортального клапанов. Примерно у 7 – 10 % детей после перенесенного ревмокардита развивается пролапс митрального клапана (ПМК).
У подростков, перенесших первую атаку ОРЛ, пороки сердца диагностируют в 30 % случаев. У взрослых пациентов данный показатель достигает 45 % случаев.
Максимальную частоту формирования ревматических пороков сердца (75 %) наблюдают в течение первых 3 лет заболевания. Повторные атаки ОРЛ, как правило, усугубляют выраженность клапанной патологии сердца.
Особенности течения ревматической лихорадки:
– клинический полиморфизм (разнообразие форм и вариантов течения);
– стертость клинической и лабораторной симптоматики (особенно у взрослых пациентов);
– часто встречающееся латентное течение, без яркой клинической манифестации;
– редко отмечаемая высокая активность течения процесса, чаще встречающиеся полиартралгии, нет полисерозитов, ревматических узелков, кольцевидной эритемы;
– преобладание нейроревматизма (хореи);
– преобладание продуктивного компонента воспаления;
– более благоприятное течение первой атаки ревматизма (реже заканчивается формированием порока сердца).
Диагностика. Лабораторные исследования. К обязательным методам лабораторного исследования относятся:
– общий анализ крови: увеличение скорости оседания эритроцитов (СОЭ) и положительный С-реактивный белок (СРБ);
– бактериологическое исследование: выявление в мазке из зева бета-гемолитического стрептококка группы A (может быть как при активной инфекции, так и при носительстве);
– определение содержания антистрептолизина-О, антигиалуронидазы и антидезоксирибонуклеазы B: повышенные или повышающиеся в динамике титры.
Дополнительные методы исследования могут потребоваться для дифференциальной диагностики и зависят от конкретной клинической ситуации (ревматоидный фактор (РФ), антиядерные АТ – отрицательные).
Инструментальные методы исследования. К обязательным методам относят:
– электрокардиография (ЭКГ) для уточнения характера нарушений сердечного ритма и проводимости (при сопутствующем миокардите);
– эхокардиография (ЭхоКГ) для диагностики патологии клапанов сердца и выявления перикардита.
Диагноз ОРЛ следует предполагать в случаях возникновения лихорадки, кардита и/или суставного синдрома через 2 – 3 нед. после ангины стрептококковой этиологии. Для подтверждения диагноза следует провести:
– общий анализ крови (увеличение СОЭ);
– ЭКГ (удлинение интервала P – Q);
– ЭхоКГ (признаки поражения клапанов);
– бактериологическое исследование мазка из зева (обнаружение стрептококка) или определение содержания антистрептококковых АТ (титры повышены).
При диагностике ОРЛ используется синдромный принцип, сформулированный отечественным педиатром А. А. Киселем (1940), который в качестве диагностических критериев выделил пять признаков болезни: кардит, мигрирующий полиартрит, хорею, кольцевидную эритему, ревматические узелки, обратив при этом внимание на важность их сочетания.
Американский кардиолог Т. Д. Джонс (1944) отнес эти признаки к «большим» диагностическим критериям, выделив дополнительно «малые» клинические и лабораторные параметры.
В настоящее время для диагностики ОРЛ применяют критерии Киселя – Джонса, пересмотренные Американской ассоциацией кардиологов в 1992 г. и модифицированные Ассоциацией ревматологов России в 2003 г. (табл. 1).
Наличие двух больших критериев или одного большого и двух малых критериев в сочетании с данными, подтверждающими предшествовавшую инфекцию, вызванную стрепток окками группы А, свидетельствует о высокой вероятности ОРЛ.
Примеры клинического диагноза:
– ОРЛ: кардит (митральный вальвулит), мигрирующий полиартрит. Недостаточность кровообращения (НК) I функционального класса (ФК), соответствует рубрике I01.1 по МКБ-10;
– повторная ревматическая лихорадка: кардит. Сочетанный митральный порок сердца. НК IIА (ФК II), соответствует рубрике I01.9 по МКБ-10;
– ХРБС: комбинированный митрально-аортальный порок сердца. НК IIБ (ФК III), соответствует рубрике I08.0 по МКБ-10.
Таблица 1
Диагностические критерии ОРЛ
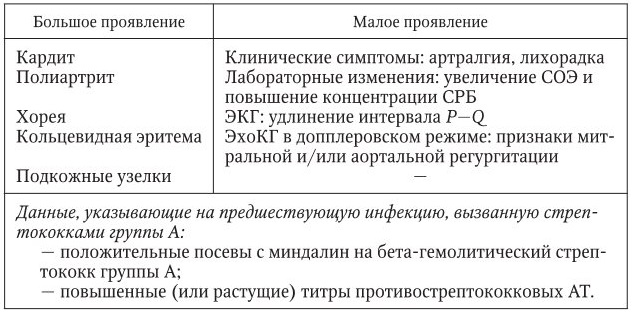
Активность заболевания. При определении активности заболевания используют совокупность клинических и лабораторных параметров.
I степень активности характеризуется моносиндромностью (невыраженный кардит либо малая хорея). Лабораторные показатели соответствуют норме или изменены незначительно.
II степень активности определяется преобладанием умеренно выраженных симптомов поражения сердца в сочетании с субфебрильной температурой тела, полиартралгиями или моно-, олигоартритом, возможна хорея, величина СОЭ в пределах 20 – 40 мм/ч. Отмечают умеренный лейкоцитоз и повышение титров противострептококковых АТ.
III степень активности характеризуется лихорадкой, острым полиа ртритом, миокардитом, высокими титрами противострептококковых АТ, возможны панкардит, серозит, нейтрофильный лейкоцитоз, увеличение СОЭ выше 40 мм/ч.
Дифференциальный диагноз. Наличие только одного из основных критериев ОРЛ (кардита, артрита, хореи) диктует необходимость исключать другие заболевания.
Дифференциальный диагноз ревматического кардита. Перечень нозологических форм, включаемых в алгоритм дифференциальной диагностики ревматического кардита, достаточно широк:
– инфекционный эндокардит (ИЭ);
– неревматические миокардиты;
– идиопатический ПМК;
– нейроциркуляторная дистония;
– кардиомиопатии;
– миксома сердца;
– первичный антифосфолипидный синдром (АФЛС);
– неспецифический аортоартериит;
– системная красная волчанка (СКВ).
Для ревматического кардита характерны:
– хронологическая связь с А-стрептококковой инфекцией глотки (фарингит, тонзиллит);
– латентный период – 2 – 4 нед.;
– молодой возраст больного;
– преимущественно острое или подострое начало;
– полиартрит или острые артралгии в дебюте болезни;
– «пассивный» характер кардиальных жалоб;
– наличие вальвулита в сочетании с миокардитом или перикардитом;
– высокая подвижность симптомов кардита;
– корреляция лабораторных и клинических признаков активности болезни.
Дифференциальный диагноз ревматического полиартрита. Опорными пунктами в дифференциальной диагностике ревматического полиартрита (до появления симптоматики кардита) с другими заболеваниями являются кратковременность и летучесть поражения преимущественно крупных и средних суставов, с быстрым ответом на противовоспалительную терапию и полной регрессией воспалительных изменений. Ревматический полиартрит дифференцируют от следующих заболеваний:
– реактивные артриты (РеА);
– ревматоидный артрит (РА) и ювенильный РА;
– синдром Стилла;
– СКВ;
– анкилозирующий спондилоартрит;
– геморрагический васкулит.
(Подробно см. соответствующие разделы учебного пособия.)
Постстрептококковый артрит может встречаться у лиц среднего возраста, развивается после относительно короткого (2 – 4 дня) латентного периода от момента перенесенной инфекции глотки гемолитическим стрептококком группы А, персистирует в течение длительного времени (около 2 мес.), протекает без кардита, недостаточно оптимально реагирует на терапию НПВС и полностью регрессирует без остаточных изменений.
Дифференциальный диагноз малой хореи. Основные трудности дифференциальной диагностики малой хореи связаны с ситуациями, когда она фигурирует в качестве единственного критерия ОРЛ. Дифференциальная диагностика проводится совместно с врачом-неврологом.
Дифференциальный диагноз детских аутоиммунных нейропсихических расстройств, ассоциированных с инфекциями, вызванными стрептококком группы A. В конце XX в. описан специфический синдром, обозначаемый аббревиатурой PANDAS (Pediatric Autoimmune Neuropsychiatric Disorders Associated with group A Streptococcal infections). В отличие от классической ревматической хореи для него характерны выраженные психиатрические нарушения – обсессивно-компульсивные расстройства (сочетание навязчивых мыслей и навязчивых движений), быстрое купирование психоневрологической симптоматики только при адекватной противострептококковой терапии.
Лечение. Цели: эрадикация бета-гемолитического стрептококка группы A, купирование воспалительного процесса, предупреждение у пациентов с перенесенным кардитом формирования ревматических пороков сердца, компенсация сердечной недостаточности у больных ревматическими пороками сердца.
Немедикаментозная терапия включает соблюдение постельного режима в течение 2 – 3 нед., диету, богатую витаминами и белком (не менее 1 г на 1 кг массы тела), с ограничением соли и углеводов.
Физиотерапевтическое лечение не показано.
Этиотропная терапия. Антибактериальная терапия. Бензилпенициллин применяют в течение 10 сут у взрослых и подростков в дозе 0,5 – 1,0 млн ЕД 4 раза/сут в/м, у детей – в дозе 100 – 150 тыс. ЕД 4 раза/сут в/м. В дальнейшем применяют пенициллины пролонгированного действия в режиме вторичной профилактики. При непереносимости пенициллинов показаны макролиды или линкозамиды (подробно см. в подразд. «Профилактика»).
Патогенетическая терапия. Противовоспалительная терапия. Глюкокортикостероиды (ГКС) применяют при ОРЛ, протекающей с выраженным кардитом и/или полисерозитами. Преднизолон назначают взрослым и подросткам в дозе 20 мг/сут, детям – в дозе 0,7 – 0,8 мг/кг в 1 прием утром после еды до достижения терапевтического эффекта (в среднем в течение 2 нед.). Затем дозу постепенно снижают (на 2,5 мг каждые 5 – 7 дней) вплоть до полной отмены. Общая длительность курса составляет 1,5 – 2,0 мес.