
О. Г. Сыропятов
Основы психофармакотерапии: пособие для врачей
Список сокращений
МКБ-10 Международная классификация болезней 10–го пересмотра
МАО моноаминооксидаза
МАО – А моноаминооксидаза типа А
ЦНС Центральная нервная система
ГАМК гамма – аминомасляная кислота
ВОЗ Всемирная Организация Здравоохранения
ИМАО Ингибиторы моноаминооксидазы
СИОЗС селективные ингибиторы обратного захвата серотонина
ЭПС экстрапирамидный синдром
5HT серотониновые рецепторы
D дофаминовые рецепторы
Α (α) альфа – адренергические рецепторы
H гистаминовые рецепторы
M мускариновые рецепторы
ТЦА трициклические антидепрессанты
АТФ, аденозинтрифосфорная кислота
АДФ аденозиндифосфорная кислота
цАМФ циклоаденозинмонофосфорная кислота
РНК рибонуклеиновая кислота
ГЭБ гематоэнцефалический барьер
Посвящается памяти коллеги, рыцаря науки, доктора медицинских наук Валентина Борисовича Литвинова

Литвинов Валентин Борисович, родился 6 июля 1935 года в Киеве. В 1960 году окончил Киевский медицинский институт им. А. А. Богомольца. С 1960 по 1962 гг. работал врачом – ординатором в Черкасской областной психоневрологической больнице.
Научно – практическая деятельность В. Б. Литвинова связана с психиатрией, психофармакологией, психотоксикологией и наркологией. С 1962 года по 1991 год – аспирант, младший научный сотрудник, старший научный сотрудник (руководитель научной группы по психотоксикологии), главний научный сотрудник Института фармакологии и токсикологии АМН Украины, доктор медичних наук.
С 1991 по 1992 годы заместитель директора по научной работе Научно – исследовательского института народной медицини Ассоциации народной медицини МЗ Украины. С 1992 по 1994 годы – советник по медицинским вопросам представителя Президента Украины в Московском районе г. Киева.
С 1994 по 1999 годы – заместитель Председателя, главный научный сотрудник Комитета по контролю за наркотиками, главный научный сотрудник Фармакологического комитета МЗ Украины.
С 2000 по 2006 годы работал в Украинском научно – исследовательском институте социальной и судебной психиатрии и наркологии МЗ Украины главным научным сотрудником отдела медико – социальных проблем терапии психических расстройств и руководителем лаборатории биохимии и патофизиологии зависимых состояний отдела проблем наркологии.
Основная направленность научной деятельности состояла в изучении проблем экспериментальной и клинической психиатрии и наркологии, а также психофармакотерапии. В. Б.Литвиновым опубликовано около 200 научных работ, получено 12 свидетельств об изобретениях и инновациях. Соавтор лекарственных препаратов: алоксим, корвалдин и др.
Раздел I. Психофармакологическая пропедевтика
Введение
Широкое распространение психических расстройств в популяции, недостаточное развитие психиатрической помощи и высокий уровень коморбидности психических и соматических расстройств делает актуальным знание основ психофармакотерапии врачами всех специальностей.
Современные тенденции развития психиатрии требует выявления, диагностики и лечения психических расстройств не только в психиатрических стационарах или в диспансерах, но и в общемедицинской практике. Это связано с деинституализацией психиатрии, сближением психиатрии с общей медициной и более гуманным отношением к больным – стремлением удалить привычные «ярлыки» психически больных. Современная международная классификация психических и поведенческих расстройств МКБ-10 нацелена на точную научную и достоверную статистическую и клиническую диагностику психических и поведенческих расстройств. Вместе с тем, в практике встречаются психические расстройства, не достигшие достаточной полноты симптоматики по МКБ-10, но требующие врачебного вмешательства. Такие расстройства могут квалифицироваться как субклинические психические расстройства и успешно лечиться врачами общей практики под руководством консультирующих психиатров в соответствии с «концепцией консультирования и взаимодействия». Своевременное назначение психотропных препаратов на ранних стадиях психического расстройства снижает затраты на лечение таких больных и предотвращает развитие таких тяжелых осложнений, как суициды и агрессия. Сочетание соматических заболеваний с психическими расстройствами также требует назначения психотропных средств.
Таким образом, актуальность изучения врачами общей практики психофармакотерапии диктуется современным уровнем развития медицины.
Понятие «psychopharmakon» впервые встречается в трудах богослова Lorichius (1548). В 1920 г. Macht определил понятие «психофармакология». Современная эпоха психофармакологии начинается с 50–х годов ХХ века и связана с введеним в практику первого нейролептика – хлорпромазина французскими учеными Delay и Deniker в 1952 г. ввели понятие «нейролептической» терапии.
История антидепрессантов начинается с 1957 г. с обнаружения антидепрессивных свойств у некоторых противотуберкулезных препаратов, относящихся по современным классификациям к группе ингибиторов моноаминоксидазы (МАО). Использовать этот «побочный» эффект для лечения депрессии предложил Klihn. В 1960 г. американский исследователь Axelrod установил механизм действия трициклических антидепрессантов (прямое влияние этих веществ на пресинаптический захват серотонина и норадреналина в синапсах нейронов ЦНС) и получил за эти исследования Нобелевскую премию.
В 1954 г. Sternbach синтезировал первый бензодиазепиновый транквилизатор хлордиазепоксид, высокую терапевтическую активность которого в отношении тревоги в том же году обнаружил Berger.
Антиманиакальные свойства лития, выявленные австралийским психиатром Cade в 1949 г., послужили основанием для выделения еще одной группы психотропных лечебных средств – нормотимиков.
Группа ноотропных препаратов начала формироваться в 1963 г., когда у некоторых производных ГАМК были выявлены свойства активировать когнитивные процессы.
Первый симпатомиметик – амфетамин – был синтезирован в 1935 г.
Таким образом, середина ХХ века была знаменательна созданием 6 важнейших классов психотропных средств: нейролептики (антипсихотические средства), антидепрессанты и нормотимики, транквилизаторы, ноотропы и стимуляторы. Введение в практику психотропных средств произвело переворот в лечении психических расстройств и послужило развитию новой научной дисциплины – психофармакологии.
Глава 1.1. Классификация психофармакологических средств и общие принципы терапии
Существуют химические, нейрофизиологические, электроэнцефалографические, фармакологические классификации психотропных средств. Однако, наиболее приемлемой является клиническая классификация, предложенная Delay (1976). Согласно этой классификации, все психотропные препараты делятся на три группы: 1) психолептики (нейролептики/антипсихотические средства, гипнотические вещества, транквилизаторы); 2) психоаналептики, или психостимуляторы (антигипнотические вещества – «пробуждающие амины», антидепрессанты и прочие стимуляторы); 3) психодизлептики, или психотомиметические вещества – галлюциногены.
Последние десятилетия ознаменовались значительным ростом новых психотропных средств, соединяющих различные психотропные эффекты с избирательностью действия на психопатологическую симптоматику. Большинство клиницистов продолжают пользоваться классификацией, предложенной в 1969 г. научной группой ВОЗ. В соответствии с этой классификацией все психотропные средства подразделяются на семь классов:
1) нейролептики/антипсихотические средства;
2) транквилизаторы/анксиолитики;
3) антидепрессанты;
4) нормотимики;
5) ноотропы/ноэтики;
6) психостимуляторы;
7) психодизлептики.
Собственно психотропным терапевтическим действием обладают препараты первых четырех классов. Ноотропы/ноэтики можно определить как группу «нейрофармакотерапии». В класс ноэтиков по современным представлениям входят ноотропы, психоэнергизаторы, психостимуляторы, нейропептиды и адаптогены. Психодизлептики не используются в клинической практике.
Все нейролептики/антипсихотические средства успокаивают, угнетают и тормозят нервную систему. Они купируют состояния психомоторного возбуждения, бред, галлюцинации и другие проявления психозов. По химическому строению это различные препараты, имеющие свой спектр психотропной активности и побочных эффектов. Соматические побочные эффекты весьма значительны у первых представителей этого класса веществ – производных фенотиазина. Неврологические осложнения – у производных бутирофенона. Требования к современным нейролептикам, помимо психотропной активности, включают минимум побочных эффектов. В связи с синтезом нейролептических препаратов с новыми свойствами предлагается использовать для этой группы лекарственных средств термин «антипсихотические» препараты.
Для сравнения антипсихотических препаратов Мосолов (2000) предложил учитывать свойства «идеального антипсихотического средства»:
• Широкий спектр биохимического и клинического действия.
• Одновременная эффективность при различных синдромальных вариантах и стадиях течения шизофрении.
• Быстрое купирование психомоторного возбуждения и галлюцинаторно – бредовой симптоматики при поддержании нормального уровня бодрствования больных.
• Коррекция негативной симптоматики.
• Возможность длительного применения без развития явлений привыкания.
• Возможность редкого приема (1 раз в день и реже).
• Хорошая переносимость (отсутствие экстрапирамидных и других соматоневрологических побочных эффектов).
• Минимальное число лекарственных взаимодействий.
Традиционно выделяют группу транквилизаторов, хотя еще в 1967 г. эксперты по психофармакологии ВОЗ предложили заменить это название термином «анксиолитики». Основное фармакологическое действие препаратов этой группы – воздействие на тревогу (anxiety). Помимо противотревожного действия препараты этой группы устраняют беспокойство, аффективную неустойчивость, мышечное напряжение и нарушения вегетативных функций. К сожалению, бесконтрольное применение транквилизаторов привело к их негативной оценке, которая обусловлена возможностью формирования зависимости и нестойкостью терапевтического эффекта. Последнее возражение против «химического решения психологических проблем» исходило от психотерапевтов, поскольку долгий и трудный процесс перестройки личностных особенностей пациентов решался простым назначением транквилизатора.
Антидепрессанты оказывают преимущественное действие на аффективную сферу (пониженное настроение). Спектр действия антидепрессантов различен. У одних препаратов вместе с антидепрессивным более выражено стимулирующее действие (мелипрамин, анафранил), у других – седативное (амитриптилин, леривон). Ингибиторы моноаминоксидазы (МАО) обладают стимулирующим действием и могут вызывать эйфорию. Препараты четырехциклической структуры (лудиомил, пиразидол) оказывают сбалансированное седативное и стимулирующее действие. Сбалансированным действием и минимальными побочными эффектами обладают антидепрессанты с серотонинергическим действием (СИОЗС). Особым психофармакологическим действием обладает тианептин (коаксил) – анксиолитический рединамизирующий антидепрессант. Для лечения больных с депрессией в общемедицинской практике следует выбирать препараты, имеющие минимальные побочные эффекты. Оптимальным спектром эффективности при минимальных побочных эффектах, по мнению Смулевича (2000; 2003) и других авторов, обладает коаксил и пиразидол.
Группу нормотимиков представляют препараты лития и антиконвульсанты (карбамазепин, соли вальпроевой кислоты и др.). Применение этих препаратов способствует предупреждению аффективных приступов.
Ноотропы — препараты, улучшающие метаболизм нервных клеток, что выражается в активации интегративных мозговых процессов и улучшении когнитивных функций.
К ноотропам относятся ноотропил, пиридитол, пантогам, оксибутират натрия, ноофен, пикамилон. Церебролизин обладает выраженным нейротрофическим действием.
Психостимуляторы обладают в основном активирующим действием, что определяет их назначение при различных астенических, апатических, ипохондрических состояниях. К психотоникам относятся фенамин, сиднокарб, сиднофен. Однако их применение ограничено из‑за возможного развития зависимости. Оказывают стимулирующий эффект и некоторые препараты растительного и животного происхождения – адаптогены: женьшень, элеуторококк, пантокрин и др.
Психодизлептические препараты – галлюциногены не используются в клинической практике, но могут применяться при аддиктивном поведении.
Многие психотропные препараты обладают перекрестным действием. Так, малые дозы нейролептиков можно использовать как транквилизаторы (тиоридазин, терален, френолон, эглонил). Это относится и к некоторым антидепрессантам (коаксил, леривон, пиразидол). Иногда трудно разграничить действие антидепрессантов и стимуляторов, поскольку некоторые антидепрессанты обладают стимулирующим действием (ИМАО). Современный уровень развития нейропсихофармакологии позволяет синтезировать препараты с заданными свойствами. Препараты последнего поколения, как антипсихотики, так и антидепрессанты обладают строгой избирательностью действия на те или другие нейромедиаторные структуры.
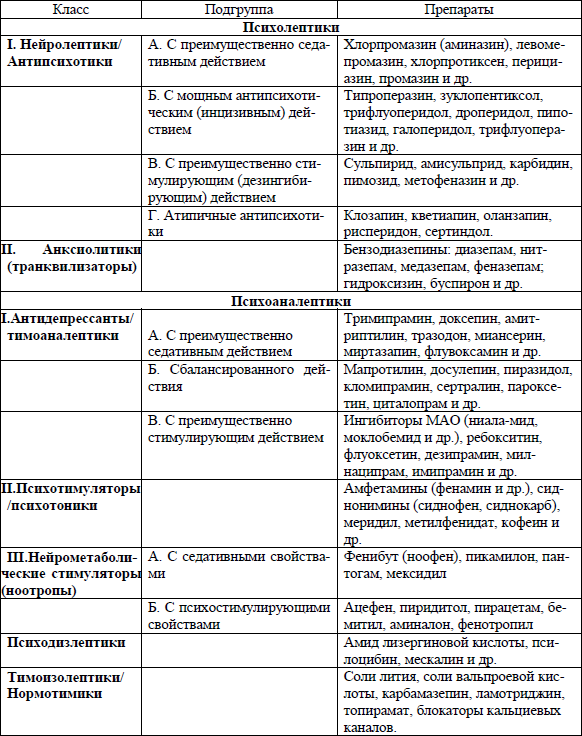
В таблице 1 представлена классическая классификация психофармакологических средств, предложенная С. Н. Мосоловым (2002).
Табл. 1. Клиническая классификация психофармакологических препаратов
Основные принципы психофармакотерапии
Эффективность лекарственной терапии психотропными средствами определяется соответствием выбора препарата клинической картине болезни, правильностью режима его дозирования, способом введения и длительностью терапии. Яничак с соавт. (1999) выделяют следующие семь принципов психофармакотерапии.
• Постоянное уточнение психического состояния пациента.
• Психофармакотерапия сама по себе, как правило, является недостаточной для полного выздоровления.
• Длительность лечения и время его начала определяется стадией болезни (например, острая фаза, обострение, рецидив).
• При разработке плана лечебных мероприятий всегда следует взвешивать соотношение предполагаемой пользы и степени риска негативных последствий терапии.
• В каждом последующем болезненном состоянии первичный выбор препаратов для данного пациента определяется имеющимися анамнестическими сведениями (в том числе и семейным анамнезом) о переносимости определенных лекарственных средств этим больным.
• Очень важно, чтобы терапия была направлена на определенные, ключевые для данного психопатологического состояния симптомы и сопровождалась оценкой их динамики на протяжении всего курса лечения.
• В процессе всего курса лечения необходимо наблюдать за возможным проявлением побочного действия лекарств. Подобный мониторинг часто предполагает лабораторные исследования, что обеспечивает контроль, как безопасности, так и оптимальной эффективности применяемых назначений.
Глава 1.2. Принципы лечения антипсихотическими лекарственными средствами (нейролептиками)
Терапевтическое действие традиционных нейролептических средств определяется, главным образом, по клинике нейролепсии. Психический компонент нейролепсии заключается в снижении психоэнергетического уровня, влечений, аффективности, снижении всего витального тонуса. Психомоторный компонент нейролепсии складывается из уменьшения спонтанности движений. Большинство нейролептиков обладает не только узким нейролептическим успокаивающе – угнетающим действием, но также и стимулирующим и активирующим.
Можно выделить четыре основных компонента действия нейролептиков в порядке возрастания:
1) седативное действие: аминазин – тизерцин – труксал;
2) общее глобарное антипсихотическое действие: аминазин – метеразин – мажептил;
3) антипсихотическое действие, направленное на галлюцинаторно – параноидные расстройства: аминазин – трифтазин – галоперидол;
4) антипсихотическое действие со стимулирующим компонентом: метеразин – этаперазин – френолон.
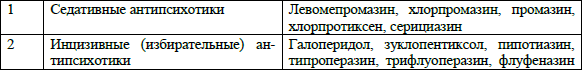
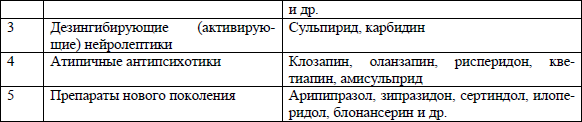
Наибольшее значение при выборе нейролептика и определении спектра его психотропной активности имеет соотношение двух параметров – глобального антипсихотического и первичного седативного эффектов (табл.2).
Табл. 2. Клиническая классификация современных антипсихотических средств по Мосолову (2004)
Самая обширная группа, выделенная по химическому строению, это производные фенотиазина (аминазин, пропазин, левомепромазин, дипразин, терален). Препараты этой группы обладают наибольшими побочными эффектами. Хлорпромазин (Chlorpromazine, Aminazini). Показания. Психомоторное возбуждение, гипоманиакальные и маниакальные состояния, острые галлюцинаторно – бредовые синдромы, психозы с проявлениями агрессивности; возбуждение при деменции и умственной отсталости; выраженная тревога, состояние страха, эмоционального напряжения; подготовка к анестезии, потенцирование анестезии; обезболивание родов, эклампсия; купирование тяжелой рвоты; иногда применяют для купирования эпилептического статуса (при неэффективности других методов лечения), фебрильная шизофрения. Противопоказания. Тяжелые депрессивные расстройства – препарат провоцирует и усугубляет симптомы депрессии; заболевания печени, почек (нефрит); нарушение функции кроветворных органов; микседема; прогрессирующие системные заболевания головного и спинного мозга; декомпенсированные заболевания сердечно – сосудистой системы; тромбоэмболическая болезнь; острый период черепно – мозговой травмы; беременность и грудное вскармливание. Побочные действия. Вялость, апатия, выраженные сонливость и слабость; головокружение; артериальная гипотензия; фотосенсибилизация и пигментация кожи; диспепсические расстройства; желтуха; агранулоцитоз; экстрапирамидные расстройства, поздние дискинезии. При парентеральном применении возможны раздражение тканей, болезненные инфильтраты в месте введения. Меры предосторожности. На время лечения не рекомендовано выполнение работы, требующей быстрой реакции, и употребление алкоголя. С осторожностью назначают при желчно– и мочекаменной болезни, остром пиелите, ревматизме, ревмокардите. С осторожностью назначают больным паркинсонизмом, эпилепсией, сахарным диабетом, при заболеваниях сердечно – сосудистой системы. В случаях появления гипертермии лечение препаратом следует немедленно прекратить из‑за возможности развитие злокачественного нейролептического синдрома. Не рекомендован одновременный прием препарата с леводопой, гуанетидином, солями лития, этанолом и этанолсодержащими препаратами. Дозы и применение. Внутрь. Начальная доза 25–75 мг/сут с постепенным увеличением до средней суточной дозы 300–600 мг после еды, разделенной на 4 приема. В/м. к необходимому количеству препарата добавляют 2–5 мл 0,25–0,5 % раствора новокаина или 0,9 % раствора натрия хлорида. Раствор вводят не более 3 раз в сутки. Суточная доза не более 600 мг/сут. При достижении эффекта переходят на прием препарата внутрь. В/в. назначается редко. К необходимому количеству препарата добавляют 10–20 мл 5% (иногда 20–40 %) раствора глюкозы или 0,9 % раствора натрия хлорида. Раствор вводят медленно в течение 5 мин однократно. Разовая доза 25–50 мг, не более 100 мг. Максимальная суточная доза 250 мг. При достижении эффекта переходят на прием препарата в/м или внутрь. Аминазин®. Драже по 25, 50 и 100 мг – № 10, 30, 50, 100. Растворы для инъекций, ампулы по 1, 2 и 5 мл, 25 мг/мл – № 10.
Менее токсичным и лучше переносимым препаратом является Терален (Alimemazine), обладающий также спазмолитическим, антигистаминным и противосудорожным эффектом. При введении препарата уменьшается сократительная активность миокарда. Гипотензивный эффект выражен незначительно, однако потенцируется действие других гипотензивных средств. Седативный эффект тералена отличается от действия аминазина ощущением довольства и благополучия. Наряду с седативным у тералена выражено снотворное действие. Обладает не только нейролептическим, но и антидепрессивным свойством. Показан при сенестопатических и ипохондрических состояниях, соматизированных психических расстройствах, тактильном галлюцинозе (зоопатический бред), сенестопатических депрессиях, тревожно – депрессивных состояниях с нарушением сна. При коморбидных психических расстройствах обычная доза тералена составляет 0,005–0,01 г/ сут. Противопоказания. Тяжелые заболевания печени и почек, закрытоугольная глаукома, аденома предстательной железы, беременность и грудное вскармливание. Побочные действия. Сонливость, сухость во рту, слабость, запор, парез аккомодации, задержка мочеиспускания. В редких случаях наблюдаются экстрапирамидные расстройства в виде гипокинезии, акатизии, тремора. Меры предосторожности. На время лечения необходимо исключить спиртные напитки. Пожилым пациентам рекомендуются меньшие дозы. Внутримышечные инъекции проводить в положении лежа. Дозы и применение. Средняя разовая доза 5–15 мг, суточная доза – 40–50 мг в 3–4 приема. Терален выпускается в таблетках по 0,005 г. Капли (4 % раствор) – в 1 капле 1 мг. Растворы для инъекций, ампулы 5 мг/мл.
Френолон (Frenoloni, Metofenazatum) – слабый седатик. Не вызывает вялости, подавленности, сонливости и мышечной слабости. Обладает стимулирующим и активирующим действием, что определяет его назначение при кататонических расстройствах. Терапевтический эффект препарата развивается постепенно и становится заметным через 2–5 дней после начала лечения. Благодаря хорошей переносимости, в отличие от аминазина, френолон может использоваться при некоторых видах тошноты и рвоты. В общемедицинской практике френолон может применяться при функциональных сердечно – сосудистых нарушениях, гипертонической болезни, гастродуоденальных заболеваниях, при патологическом климаксе. Препарат эффективен при психических расстройствах с нерезко выраженной галлюцинаторно – параноидной, неврозоподобной, ипохондрически – сенестопатической симптоматикой у пожилых и соматически ослабленных пациентов. В общемедицинской практике дозы френолона ограничиваются 0,005–0,02 г/сут. Побочные явления. Бессонница, отечность лица, головокружение; иногда появляется кожная сыпь. В редких случаях наблюдаются желтуха, изменение картины крови, светочувствительность. Наиболее частые осложнения – экстрапирамидные нарушения с преобладанием явлений акатизии. Препарат противопоказан при тяжелых заболеваниях печени и почек, заболеваниях сердца с нарушением проводимости, эндокардите, заболеваниях крови. Выпускается в таблетках по 0,005 и в 0,5 % растворе – 1 мл (в ампуле 5 мг.)
Тиоридазин (Thioridazini, Mellaril, Sonapax) – часто применяемый в общемедицинской практике нейролептик. Препарат легко переносится больными и обладает антидепрессивным эффектом. Преимущественно центральное холинолититическое свойство тиоридазина и быстрое выведение из организма позволяет применять его при аментивно – делириозных расстройствах у пожилых пациентов. Препарат показан при тревожно – бредовых, депрессивно – параноидных, сенестоипохондрических и невротических состояниях у пожилых и соматически ослабленных больных. Противопоказания. Коматозные состояния, аллергические реакции и изменение картины крови при применении других лекарств. При длительном применении тиоридазина возможно развитие токсической ретинопатии. В общемедицинской практике средняя суточная доза тиоридазина составляет 0,04–0,1 г. Выпускается в таблетках по 10 и 25 мг. Син. Тиорил® табл. 100 мг № 100; Ридазин®, табл. 10 мг и 25 мг тиоридазина, Табл. № 20.
Неулептил (Periciazinum, Neuleptil) обладает умеренным адренолитическим и холинолитическим эффектом, выраженной противорвотной активностью. Эффективен при личностных расстройствах с моторной расторможенностью, импульсивностью, дисфориях, нарушениях влечений, конфликтностью, истерическими стигмами. Показан при паранойяльных состояниях и заострении личностных черт в старости. Противопоказания. Тяжелая печеночная и почечная недостаточность, декомпенсированная сердечно – сосудистая недостаточность, токсический агранулоцитоз в анамнезе, закрытоугольная глаукома, порфирия, аденома предстательной железы, беременность и грудное вскармливание. Побочные действия. Экстрапирамидные расстройства, ортостатическая артериальная гипотензия, сухость во рту, запор, парез аккомодации, задержка мочеиспускания, эректильная дисфункция, аменорея, увеличение массы тела, галакторея, гинекомастия, гиперпролактинемия, гипертермия, холестатическая желтуха, фотосенсибилизация кожи, агранулоцитоз. Меры предосторожности. При появлении гипертермии немедленно отменить препарат. С осторожностью назначать больным эпилепсией и паркинсонизмом. На время лечения не рекомендовано выполнять работы, требующие быстрой реакции, и употреблять спиртные напитки. Усиливает эффект наркотических средств, анальгетиков, барбитуратов, алкоголя, гипотензивных средств и транквилизаторов. Рекомендуется в дозах 0,01–0,02 г. Начальная доза 2 – 10 мг в 3–4 приема/сут. Средняя суточная доза – 30–40 мг; максимальная доза – 50–60 мг. Дозы и применение. Выпускается в капсулах по 0,01 г. и в растворе. Неулептил® капсулы по 10 мг № 50 и № 500.В общемедицинской практике предпочтительно использовать капли (4 % раствор – в 1 капле 1 мг.); 30 и 125 мл.
Хлорпротиксен (Chlorprothixeni, Truxal). Обладает седативным, атипсихотическим и атидепрессивым эффектом. Показан при тревожно – депрессивных, депрессивно – параноидных и неврозоподобных состояниях. В общемедицинской практике используются малые дозы хлорпротиксена для нормализации сна (0,005–0,05 г/сут). Из побочных эффектов возможен ортостатический коллапс, нарушения аккомодации, тахикардия, дизартрия, сухость слизистых оболочек, нарушения потенции. Побочные эффекты ограничивают применение препарата у пожилых пациентов. Меры предосторожности. Прекращают лечение путем постепенного снижения дозы лекарства. На время терапии следует избегать приема алкоголя, воздействия экстремальных температур, инсоляции, потенциально опасных видов деятельности, требующих повышенного внимания и быстроты психомоторных реакций. Дозы и применение. 50–200 мг/сут внутрь, предпочтительно на ночь. В общемедицинской практике используются низкие дозы препарата – 0,015 г. Выпускается в таблетках по 0,015 и 0,05 г. № 50.
Галоперидол (Haloperidol, Haldol, Halophen, Senorm) – нейролептический препарат из группы бутирофенона. Главное свойство – влияние на бред и галлюцинации, купирование психомоторного возбуждения. Показания: паранойяльные, галлюцинаторно – параноидные и галлюцинаторные состояния при шизофрении, делириозные состояния, галлюцинаторно – бредовое и маниакальное возбуждение. Препарат не вызывает вялости и апатии. Кроме антипсихотического действия препарат эффективен при синдроме Жиля де ля Туретта, хорее Гентингтона, различных тиках, малой хорее, спастическом тортиколлисе и других гиперкинезах, при заикании и упорной икоте центрального происхождения. Доказано, что галоперидол безопасен для беременных, рожениц и для плода. Возможно также применение препарата при инфаркте миокарда и в постинфарктном периоде для снятия возбуждения и напряженности. Противопоказания. Заболевания ЦНС, сопровождающиеся пирамидными и экстрапирамидными расстройствами; депрессивные состояния; кома; беременность и грудное вскармливание; возраст до 3 лет; повышенная чувствительность к галоперидолу и другим производным бутирофенона, а также к конжутному маслу при применении деканоата. Побочные действия. Экстрапирамидные расстройства, большие эпилептические припадки, усиление психотических расстройств, депрессия, при применении в высоких дозах – артериальная гипотензия, тахикардия, изменение показателей ЭКГ; преходящие и незначительные лейкопения, эритропения, лейкоцитоз, диспепсические расстройства, нарушения функции печени, гинекомастия, гиперпролактинемия, нарушение менструального цикла, эректильная дисфункция, изменение либидо; сухость во рту, нарушения зрения, приапизм, задержка мочи, ларинго– и бронхоспазм, ретинопатия. Меры предосторожности. Препарат с осторожностью назначают при эпилепсии, декомпенсированных сердечно – сосудистых заболеваниях, тяжелых болезнях почек, предрасположенности к глаукоме, тиреотоксикозе, легочной недостаточности. Не рекомендовано выполнение работ, требующих быстрой реакции, и употребление алкоголя. Лекарственные взаимодействия. Галоперидол потенцирует действие антигипертензивных средств, опиоидных анальгетиков, барбитуратов, антидепрессантов, этанола. При одновременном применении галоперидола и антикоагулянтов наблюдается уменьшение эффекта последних. Противопоказано сочетание галоперидола с литием. Дозы и применение. В начале лечения при отсутствии выраженного возбуждения 1,5–3 мг/сут в 2–3 приема, через 30 мин после еды, с постепенным повышением дозы до получения терапевтического эффекта (от 10 до 60 мг/сут). Продолжительность лечения устанавливается индивидуально. Снижение дозы производят постепенно. Поддерживающие дозы 0,5–5 мг/сут. В/м. 2–5 мг 2–3 раза в сутки в течение нескольких дней до купирования психомоторного возбуждения с последующим переходом на прием препарата внутрь. В общемедицинской практике, во избежание развития экстрапирамидных синдромов, следует применять низкие дозы препарата – 0,75–1,5 мг. Выпускается в таблетках по 0,0015 и 0,005 г, во флаконах по 10,0 мл 0,2 % раствора (10 капель – 1 мг.). Ампулы по 1,0 мл 0,5 % раствора.
Галоперидол деканоат (Haloperidoli decanoati) Дозы и применение. 50–200 мг 1 раз в 2–4 нед, в/м. Галоперидол деканоат® растворы для инъекции, ампулы по 1,0 мл 50 мг/мл; № 1 и 5.
Зуклопентиксол (Zuclopenthixoli). Клопиксол (зуклопентиксол) является производным тиоксантена. Показания. Шизофрения и другие психотические расстройства с галлюцинаторно – параноидной симптоматикой. Обладает антипсихотическим и специфическим тормозящим действием. Неспецифический седативный эффект проявляется через два часа. Назначается пациентам с ажитацией, беспокойством, враждебностью или агрессивностью. В общемедицинской практике клопиксол назначается с осторожностью пациентам с судорожным синдромом, хроническим гепатитом и сердечно – сосудистыми заболеваниями. Возможно развитие экстрапирамидных симптомов. В большинстве случаев они корригируются снижением дозировок или назначением антипаркинсонических средств. Противопоказания. Острая интоксикация алкоголем, барбитуратами, опиатами; коматозные состояния; беременность, грудное вскармливание. Побочные действия. Головокружение, сонливость, экстрапирамидные нарушения, нарушение аккомодации, поздняя дискинезия; тахикардия, ортостатическая артериальная гипертензия; сухость во рту, запор. Меры предосторожности. С осторожностью назначается при заболеваниях печени, сердечно – сосудистых заболеваниях, судорожном синдроме. Не рекомендовано выполнение работы, требующей быстрой реакции, и употребление спиртных напитков. Дозы и применение. Внутрь 10–15 мг/сут. Клопиксол® Таблетки по 2, 10 и 25 мг; № 50 и 100.







