
Александр Панчин
Сумма биотехнологии. Руководство по борьбе с мифами о генетической модификации растений, животных и людей
С появлением новых данных – полных геномов человека и других животных – ситуация прояснилась. Если взять геномы человека, шимпанзе, мыши, утконоса и так далее, окажется, что какие-то участки последовательностей нуклеотидов даже у сравнительно далеких видов очень похожи – например, гены, необходимые для синтеза белков, входящих в состав рибосом. Это понятно: рибосомы возникли очень давно, у них были миллиарды лет, чтобы в процессе эволюции достигнуть такого совершенства, что их практически невозможно улучшить или изменить, не испортив один из важнейших клеточных процессов – синтез белков, за который они отвечают.
Мутации происходят в любых участках генома, поэтому хорошим критерием функциональности участка ДНК является то, что возникающие в нем мутации не закрепляются: носители новых генетических вариантов вымирают, не оставляя потомства, устраняются естественным отбором. Другие участки геномов имеют значительные расхождения между видами и даже внутри видов. Значит, мутации в этих участках, скорее всего, безвредны, то есть их функциональная роль как минимум невелика или не зависит от конкретной последовательности нуклеотидов. Например, если последовательность нужна только для физического разделения в пространстве двух участков ДНК. Это знание используется в современной медицинской генетике, когда ученые пытаются понять, какие изменения в ДНК человека приводят к тому или иному наследственному заболеванию85: наиболее подозрительными являются мутации в эволюционно неизменных участках ДНК.
В ряде современных работ оценили долю участков ДНК человека, мутации в которых вредны, и оказалось, что они составляют лишь около 6,5–10 % генома человека86, 87, что снова совпало с предсказаниями Оно! В далеком 1972 году он из теоретических соображений называл цифру в 6 %! У нас большой геном, но, по-видимому, в нем действительно довольно много лишнего. Важен не только размер генома, но и умение им пользоваться.
Еще один актуальный вопрос: насколько последовательности ДНК различаются между живыми организмами? Насколько похожи гены человека и шимпанзе? Гены человека и банана? Степень сходства (доля совпадающих нуклеотидов) будет варьировать в зависимости от выбранного участка ДНК. Ниже показаны сравнения (нуклеотидные выравнивания) генов, кодирующих белок гистон H1 человека и шимпанзе, а также человека и банана (звездочками помечены совпадающие нуклеотиды; знаками “-” – отсутствующие). Гистоны – это белки, на которые “наматывается” ДНК, чтобы компактно упаковаться в ядре. Это очень древние белки, возникшие на заре эволюции, необходимые для жизни всем эукариотам. Поэтому степень сходства между организмами по генам этого белка выше среднего – мутации в этих генах чаще всего вредны.

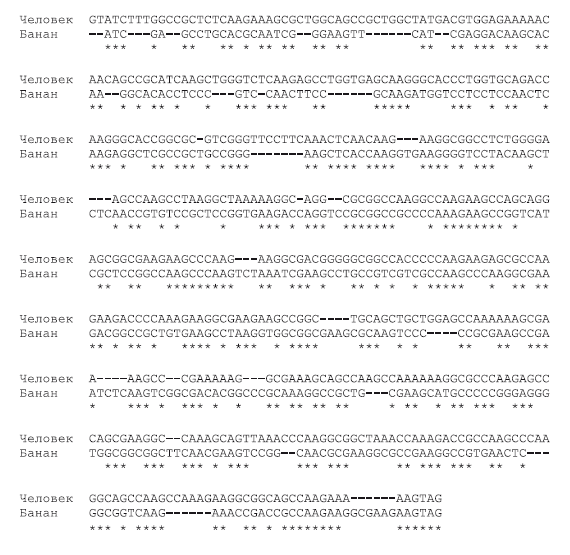
Можно заметить, что ген человека и ген шимпанзе почти идентичны: всего 5 отличий на 660 нуклеотидов! В среднем у человека с шимпанзе последовательности ДНК совпадают на 98,76 %88 (чуть ниже, чем получилось для приведенного сравнения), а вот геномы двух людей совпадают примерно на 99,9 %. Мы также видим, что ген гистона банана совпадает с геном человека лишь где-то на 50 %. Для сравнения, если мы возьмем две совершенно случайные последовательности ДНК, между ними будет около 25 % сходства. Шимпанзе ближе к человеку, чем к банану, не только по степени сходства генов, но и по набору генов в геноме. У банана будет много генов, которых нет у приматов (например, связанных с фотосинтезом), а у приматов будут гены, которых нет у растений (например, связанные с развитием нервной системы).
Полезно представлять, насколько маленьким может быть геном живого организма. Геном паразитической бактерии Mycoplasma genitalium составляет всего около 580 тысяч “букв” – это один из самых маленьких известных бактериальных геномов89. Еще меньше бывают геномы вирусов. Вирусы не принято называть “живыми”, ведь они не являются клетками и не могут самостоятельно размножаться. Вирусы – это паразитическая наследственная информация, использующая генетический аппарат клеток для синтеза своих белков, размножения и распространения.
Типичный геном вируса иммунодефицита человека (ВИЧ) составляет 9749 нуклеотидов90. Бывают и на удивление крупные вирусы с очень богатым генетическим материалом, например, геномы пандоравирусов могут достигать размера в 2,5 миллиона нуклеотидов91, а живут они в амебах – одноклеточных эукариотах. Также в амебах живет и другая группа крупных вирусов с милым названием мимивирусы, геномы которых достигают миллиона нуклеотидов, что для вирусов тоже очень много92.
ВИЧ – это ретровирус, но не подумайте, что это вирус шестидесятых (впервые вызываемый им синдром приобретенного иммунодефицита – СПИД – был диагностирован в 1981 году). Он называется ретровирусом потому, что его геном сделан не из ДНК, как у большинства вирусов и живых организмов, а из РНК. У ретровирусов есть белок “обратная транскриптаза”, который умеет делать транскрипцию наоборот, то есть синтезирует ДНК, комплементарную молекуле РНК. С помощью этого белка ВИЧ создает ДНК-версию своего генома и встраивает ее в геном человеческой клетки. Дальше инфицированная клетка начинает сама производить вирусный генетический материал и его белки. Синтезированные компоненты собираются в новые вирусные частицы и выходят из клетки.
Генетические последовательности можно записывать в виде текста и работать с ними как с последовательностью букв. Так их удобно анализировать: исследовать распространенность тех или иных мутаций в популяции, изучать закономерности эволюции, находить определенные гены и так далее. Ниже приведена последовательность гена, который кодирует обратную транскриптазу ВИЧ.

А вот аминокислотная последовательность обратной транскриптазы ВИЧ в стандартном однобуквенном коде.

Обратите внимание, что теперь мы должны использовать не 4 символа, а 20 – для обозначения аминокислот, а не нуклеотидов, и количество символов уменьшилось в три раза, ведь тройке нуклеотидов отвечает одна аминокислота. Мы досконально знаем, как устроен геном ВИЧ с точностью до нуклеотидов, а точнее, мы знаем последовательности геномов сотен разных его штаммов, причем все они выложены в свободный доступ. И вот странный факт: есть целое движение людей, отрицающих существование этого вируса!
Существуют методы, позволяющие установить последовательность нуклеотидов той или иной молекулы ДНК или РНК. В случае с молекулами РНК обычно сначала осуществляют обратную транскрипцию (с помощью обратной транскриптазы), чтобы получить молекулу ДНК, а уже саму молекулу ДНК “читают”. Чтение генетических последовательностей позволяет нам находить мутации или нуклеотидные замены – отличия между этими последовательностями. В случае с вирусами или бактериями это часто имеет прикладное значение и помогает установить, какие изменения генов привели к тому, что бактерия обрела устойчивость к антибиотику, а вирус – способность обходить защиту нашей иммунной системы или способность заражать представителей другого вида, который раньше вирусом не заражался.
Полезно знать, почему вирусы птичьего и свиного гриппа внезапно стали заражать человека, а также почему безобидная кишечная палочка с органической фермы в Германии встала на тропу инфекционной войны и сделалась патогенной. Если мы хотим подобрать лекарство, которое будет действовать против многих штаммов вируса или бактерии, желательно, чтобы оно взаимодействовало с какой-нибудь неизменной частью важного для них белка. Есть и другие вопросы, ответы на которые получают с использованием анализа ДНК (подробный рассказ о нем последует в двенадцатой главе).
Еще один пример использования анализа ДНК можно продемонстрировать на все том же вирусе иммунодефицита человека. В 1992 году в журнале Science была опубликована статья, описывающая драматичную историю, которая развернулась в США93. Семерым пациентам врача-стоматолога, больного СПИДом, поставили диагноз ВИЧ-инфекции. Причем пятеро из семи пациентов не имели очевидных факторов риска заражения: не занимались незащищенным сексом, не принимали внутривенно наркотики.
Учитывая, что через кабинет врача проходит довольно много людей, могло иметь место простое совпадение. Провели анализ генов, кодирующих вирусную оболочку ВИЧ из образцов пациентов, дантиста и группы людей из того же региона, зараженных ВИЧ, но не ходивших к данному стоматологу. Оказалось, что гены ВИЧ пяти из упомянутых пациентов очень похожи на гены ВИЧ врача, причем сходства было намного больше, чем с генами ВИЧ других людей.
Гены ВИЧ двух оставшихся пациентов сильно отличались от генов ВИЧ стоматолога, поэтому было заключено, что пять пациентов заразились в кабинете врача, а двое, скорее всего, где-то еще. ВИЧ мутирует так быстро, что, глядя на последовательности его генов у разных людей, заразившихся даже с небольшим интервалом времени, мы можем достоверно восстановить историю заражений. Примерно такой же сравнительный генетический подход используется для установления отцовства и иных родственных связей между людьми или для установления родства между живыми организмами разных групп. В последнем случае на основании степени сходства генетических последовательностей организмов строятся филогенетические деревья (что-то вроде родословной). Такие деревья показывают, что ближайший современный родственник человека – шимпанзе, что летучие мыши и дельфины генетически ближе к хомячкам и коровам, чем к птицам и рыбам.

Наверное, во избежание паники и распространения кариеса стоит подчеркнуть, что риск заражения ВИЧ в кабинете стоматолога ничтожно мал и связан с нарушением правил гигиены и несоблюдением стерильности медицинского оборудования.
Вот еще одна история о необычном применении методов генетического анализа. Вши, живущие в волосах человека, имеют существенные отличия от вшей, живущих на его одежде, – как в поведении, так и в устройстве тела. Отличаются они и генетически. Понятно, что до появления вшей, приспособленных к жизни в человеческой одежде, должна была появиться сама эта одежда, то есть, изучая генетические отличия человеческих вшей, можно примерно оценить, как давно люди стали одеваться. Для этого нужно лишь знать, сколько мутаций накопилось с момента расхождения двух популяций вшей, сколько новых мутаций возникает в геноме вшей за одно поколение и как быстро происходит смена поколений. Учитывая эти данные, эволюционный биолог Мелисса Тоупс с коллегами пришли к выводу, что одежду наши предки начали носить около ста тысяч лет назад94.
Сегодня мы знаем, что мутации в генах приводят к генетическому разнообразию. У людей на геном в три миллиарда нуклеотидов приходится около трех миллионов отличий между парами хромосом, доставшимися от папы и мамы, – разных аллелей95. Существование аллелей генов было предсказано задолго до открытия молекулы ДНК. Еще в середине XIX века чешский монах Грегор Мендель установил не только существование генов как дискретных единиц передачи наследственной информации, но и законы наследования этих генов, а также тот факт, что один и тот же ген может присутствовать в нескольких вариантах. Мендель пришел к этому выводу, изучив закономерности наследования признаков у гороха.
Горох бывает с красными цветками, а бывает с белыми. Горох способен самоопыляться. Если горох самоопыляется в течение нескольких поколений, можно вывести “чистые линии” гороха по признаку “окраска цветков”. Что такое чистая линия гороха? Это, например, такой горох с красными цветками, который при самоопылении всегда дает горох с красными цветками, то есть при скрещиваниях в рамках чистой линии признак сохраняется из поколения в поколение. Мендель обнаружил, что если скрестить чистые линии гороха с красными цветками и гороха с белыми цветками, то в первом гибридном поколении все потомки будут с красными цветками. Признак “красные цветки” Мендель назвал доминантным. Признак “белые цветки” был назван рецессивным.
Мендель выяснил, что если скрещивать особи гороха из первого гибридного поколения (все с красными цветами) друг с другом, то примерно ¾ их потомков унаследуют красные цветки, но ¼ унаследует белые. Это согласовывалось с наблюдением, что у внуков могут проявляться какие-то признаки их дедушек и бабушек, которые не проявлялись у родителей. В данном случае унаследованный признак белых цветков незаметно сохранялся в растениях гороха с красными цветками. Мендель исследовал более 29 тысяч особей гороха, и такая большая выборка позволила ему показать, что данное соотношение 3:1 доминантных признаков к рецессивным у “внуков” близко к математически точному. Это навело его на мысль, что в основе наследования генетической информации лежат некие дискретные невидимые невооруженным глазом сущности. Впоследствии эти сущности были изучены и названы генами.
Если бы Мендель изучал генетику людей и экспериментировал с чистыми линиями нашего вида (если бы это было возможно), он мог бы обнаружить много похожих эффектов, связанных с тем, что один вариант гена доминирует над другим. У людей зеленый цвет глаз, как правило, доминирует над голубым, а шестипалость над пятипалостью (просто мутация очень редкая). На самом деле это немного упрощенное представление, так как даже самые простые признаки редко определяются лишь одним геном. Но Менделю повезло – он выбрал очень удачную модель, максимально приближенную к идее “один ген – один признак”.
Открытие молекулы ДНК и ее роли в передаче наследственной информации заслуживает отдельного упоминания. Молекула ДНК была открыта в 1869 году швейцарским биологом Иоганном Фридрихом Мишером. Мишер научился выделять это вещество и дал ему название “нуклеин”, а также показал, что нуклеин обладает кислотными свойствами (ДНК – это дезоксирибонуклеиновая кислота). Примерно в это время возникли первые предположения, что молекула ДНК может быть связана с передачей наследственной информации, но никаких убедительных доказательств этому еще не было. ДНК была лишь одной из множества молекул, которые удалось обнаружить в живых клетках.
В 1928 году английский генетик и врач Фредерик Гриффит провел знаменитые эксперименты, показавшие возможность передачи наследственной информации в пробирке96. Гриффит использовал две разновидности бактерий пневмококков. Первая – патогенные пневмококки, которые вызывают смертельную инфекцию у мышей. Вторая – безобидные пневмококки. Гриффит показал, что убитые нагреванием патогенные пневмококки не вызывают инфекции, но если смешать мертвых патогенных пневмококков и живых непатогенных, то можно получить живых патогенных пневмококков. Очевидно, “патогенность” каким-то образом может передаваться от мертвых бактерий живым. Экстракт, содержащий мертвых патогенных пневмококков, сохранял какую-то сущность, некую молекулу, несущую наследуемый признак. Но ученых по-прежнему интересовал вопрос: что это за молекула?
К тому времени круг поиска сузился до трех типов молекул, которые в большом количестве присутствовали во всех живых организмах: ДНК, РНК и белки. В 1944 году американские биологи Освальд Эвери, Колин Маклеод и Маклин Маккарти провели простой и красивый эксперимент. В их распоряжении имелись ферменты, которые умели избирательно разрушать ДНК, РНК или белки. Были повторены опыты Гриффита с тем изменением, что экстракт мертвых патогенных пневмококков перед смешением с непатогенными живыми пневмококками обрабатывался одним из перечисленных типов ферментов. Оказалось, что, если обработать экстракт, полученный из мертвых патогенных пневмококков, ферментами, которые разрушат РНК или белки, передача наследственной информации все равно произойдет, и зараженная пневмококком мышка умрет. Но если разрушить ДНК, пневмококки остаются безобидными, мышка живет. Так было установлено, что “трансформирующим агентом” в эксперименте Гриффита являлась именно молекула ДНК97.
Уже эти опыты показали, что природа предусмотрела возможность обмена наследственной информацией между живыми организмами. Сегодня мы четко представляем, что бактерии могут активно усваивать фрагменты ДНК, которые остались от других существ98. Насколько процессы изменения ДНК распространены в природе и каково разнообразие различных мутационных процессов, включая обмен участками ДНК между разными организмами, мы рассмотрим в следующей главе.
Глава 6
Мой дедушка был вишней. Генетическое разнообразие жизни, механизмы мутагенеза, эволюция и селекция, принцип предосторожности
Экологические катастрофы, естественный отбор, селекция, антибиотики и устойчивость к ним, иммунная система позвоночных и бактерий, мобильные генетические элементы, мутации и горизонтальный перенос генов, генетическое разнообразие на нашей планете и даже инопланетная раса зергов – все это имеет некоторую взаимосвязь, которая обретает смысл в свете эволюции.
Американский экономист Нассим Талеб, выступая против ГМО, аргументировал принцип предосторожности с позиции математической статистики99. Талеб полагает, что распространение ГМО может привести к гибели всего человечества, да и вообще уничтожить существенную часть жизни на нашей планете в ходе экологической катастрофы, которая получила название экоцид. Аргумент Талеба заключается в том, что, даже если вероятность экоцида в результате внедрения отдельного ГМ сорта очень мала, последовательные многократные попытки создания ГМО могут этот риск значительно увеличить: рано или поздно мы создадим такой ГМО, который нас всех уничтожит.
Когда мы строим ядерный реактор, мы рискуем, ведь реактор теоретически может рвануть. Но не стоит рассматривать этот риск отдельно от опасностей, связанных с использованием альтернативных источников энергии. Почему бы не учесть негативные последствия от увеличения цен на электроэнергию или выбросов углекислого газа в атмосферу? Ведь отказ от ядерной энергетики в современных реалиях будет означать более интенсивное использование угля, нефти и газа. Когда человек осваивал огонь, он рисковал подпалить лес, в котором жил. Но где бы были мы сейчас, если бы наши предки отказались от использования огня? Учитывая все риски, рассмотрим ли мы опасность учета всех рисков? На эту тему есть отличная иллюстрация: металлический предупреждающий знак, на котором крупными буквами написано, что у знака острые края и поэтому его лучше не трогать.
В приведенном примере опасность для здоровья создается самим существованием предупреждающего о ней знака. Так и утверждения об опасности ГМО создают угрозу, что под давлением общественного мнения, которое формируют не столько ученые, сколько журналисты и политики, мы откажемся от важнейших технологий. Весьма вероятно, что дети, страдающие от нехватки витамина А, которых можно было бы спасти, погибнут, если золотой рис не получит одобрения. Есть риск, что люди, страдающие от диабета, умрут, если мы перестанем производить инсулин с помощью генетически модифицированных микроорганизмов. А ведь развитие сценария экоцида Талеба прежде всего касается быстро размножающихся и меняющихся одноклеточных!
Талеб упускает из виду биологическую сторону вопроса. Краеугольным камнем его аргументации является утверждение, что существуют принципиальные различия в рисках, связанных с использованием генной инженерии и селекции. Но кто сказал, что в природе не происходят те же самые процессы, которые используются при создании ГМО? И кто сказал, что продукты селекции или естественного отбора безопаснее продуктов генной инженерии?
Грандиозные экологические катастрофы случались в истории биосферы без участия человека. В результате появления фотосинтезирующих организмов несколько миллиардов лет назад произошли радикальные изменения в атмосфере Земли. Образовался кислород, страшный окислитель, к появлению которого многие формы жизни были не готовы. Но в итоге сформировались и вот уже миллиарды лет существуют организмы, использующие эффективный аэробный (кислородный) метаболизм вместо менее эффективного анаэробного. Содержание кислорода в воздухе с тех пор не оставалось постоянным. Сегодня кислород составляет 21 % атмосферы Земли, но за последние 550 миллионов лет его содержание менялось в пределах от 15 до 30 %100, и с этими колебаниями было связано появление и исчезновение гигантских насекомых, способных существовать только при высоких концентрациях кислорода.
Эксперименты в области генной инженерии производятся человеком в сравнительно небольшом объеме, в то время как природа порождает новых мутантов каждую секунду! Само существование жизни на нашей планете – один большой рискованный эксперимент, и генная инженерия к нему ничего принципиально нового не прибавляет. Давайте рассмотрим масштабы, в которых генетические изменения происходят в окружающей среде.
Самой многочисленной и разнообразной группой живых организмов на Земле являются прокариоты, к которым относятся бактерии и археи. Считается, что на нашей планете обитает около 1030 прокариот. По некоторым оценкам, количество их видов может достигать миллиарда101, но даже по самым скромным подсчетам речь идет о десятках миллионов видов. Между тем есть основания полагать, что только в кишечнике одного человека живет более триллиона клеток, относящихся к более чем пятистам видам бактерий102.
Разнообразие эукариот тоже огромно. Существуют миллионы разных видов насекомых (и других членистоногих), 85 тысяч видов моллюсков, 64 тысячи описанных видов позвоночных, более 25 тысяч видов круглых червей, 20 тысяч видов плоских червей, 17 тысяч видов кольчатых червей – и это перечислены даже не все крупные группы животных. Число разных видов грибов оценивается в 1,5–5 миллионов, а число видов наземных растений в 300–315 тысяч. Трудно представить, чтобы все это биоразнообразие спаслось от Великого потопа в одном Ноевом ковчеге, даже если исключить подводных обитателей. Конечно, все эти порой очень непохожие друг на друга организмы возникли не на пустом месте, а в результате многочисленных последовательных изменений ДНК предковых видов. Эти изменения в ДНК происходят и сейчас, у нас на глазах.
Все организмы являются генетически модифицированными относительно своих предков. Это утверждение справедливо и для человека. Как уже упоминалось, между мной, вами и любым другим представителем вида Homo sapiens, за исключением однояйцовых близнецов, найдется около трех миллионов генетических отличий. Именно столько отличий было обнаружено, когда в 2007 году прочитали один из первых полных геномов отдельного человека, ученого Крейга Вентера95, и сравнили хромосомы, которые он унаследовал от мамы и папы. Три миллиона – это только число точечных одиночных отличий лишь в один нуклеотид, не считая различных хромосомных перестроек, вставок и делеций участков ДНК. Учитывая, что на Земле живут миллиарды людей, будет сложно указать такой участок генома, который не претерпел бы изменений хотя бы у одного живого человека (если не считать участков, мутации в которых несовместимы с жизнью).
Упомянутые миллионы отличий появились не сразу, а накапливались на протяжении длительного времени. У человека в каждом поколении возникают десятки новых мутаций103. Ребенок не только получает некую уникальную комбинацию генетических вариантов от родителей, но еще около пятидесяти совершенно новых генетических вариантов, которых ни у кого из родителей не было.
Мутации в ДНК человека и представителей других видов неизбежны по целому ряду причин. Во-первых, фермент ДНК-полимераза, копирующий наследственную информацию, не умеет работать без ошибок: время от времени в растущую цепочку ДНК встраиваются неправильные нуклеотиды. Существуют разные ДНК-полимеразы, отличающиеся своей точностью, но даже самые надежные из них ошибаются хотя бы раз при копировании миллиона нуклеотидов104. Если бы не существовало никаких дополнительных механизмов устранения ошибок при синтезе ДНК, копирование столь крупного генома, как у человека, приводило бы к тысячам ошибок и возможность нашего существования была бы под вопросом.
К счастью, основные ДНК-полимеразы умеют отщеплять неправильно присоединенные нуклеотиды и исправлять собственные ошибки. Этот механизм тоже не абсолютно точный, но он снижает количество ошибок на порядок или, может быть, на два. Но сотни ошибок при каждом делении клеток – это все равно недопустимо много, особенно учитывая, как часто происходит деление. Для устранения нераспознанных ошибок существует система репарации – механизм, устраняющий неправильно спаренные нуклеотиды в двойной спирали молекулы ДНК.
Если в результате ошибки ДНК-полимеразы к растущей цепи молекулы ДНК был присоединен неправильный нуклеотид, возникает ситуация, когда стоящие друг напротив друга нуклеотиды в двойной спирали уже не являются комплементарными. Напротив А может стоять G, а не T, или напротив G – T, а не C. Это приводит к деформации молекулы ДНК. Специальные белки распознают подобные деформации и заменяют один из двух нуклеотидов таким образом, чтобы пара стала комплементарной (А напротив T, G напротив С). Разумеется, в этом процессе ферменты тоже могут ошибиться: оставить неправильный нуклеотид, а правильный заменить. В этом случае мутацию будет уже очень сложно устранить, ведь после такого исправления мы все равно получим комплементарную пару нуклеотидов. К счастью, система репарации умеет худо-бедно различать старую цепочку молекулы ДНК и вновь синтезированную и предпочитает сохранять старый вариант пары нуклеотидов. Но и этого недостаточно, чтобы полностью избежать мутаций.
Хорошая новость состоит в том, что для передачи по наследству мутация должна произойти не в любой клетке, а в клетке зародышевой линии, то есть либо в половой клетке, либо в клетке, которая впоследствии станет половой (после делений). При этом половые клетки проходят тщательный отбор. Миллионы сперматозоидов пытаются слиться с яйцеклеткой, но лишь один в итоге станет донором наследственного материала будущего плода. Естественно, серьезные нарушения в ДНК сперматозоида помешают ему победить в условиях столь жесткой конкуренции. Яйцеклетка достанется наиболее приспособленному (хотя не всякий генетический вариант, полезный сперматозоиду, полезен взрослому человеку!).
Яйцеклетки тоже проходят через “сито” естественного отбора. К 18–22 неделям развития женского плода в яичнике еще не рожденной девочки образуется несколько миллионов фолликулов, содержащих незрелые яйцеклетки. Их число впоследствии сокращается до нескольких сот тысяч к моменту половой зрелости, но только около четырехсот из них когда-либо получат шанс стать оплодотворенными.
Есть еще один барьер, препятствующий накоплению мутаций в клетках многоклеточных организмов, – апоптоз, или запрограммированная клеточная смерть. Если в клетке накапливаются повреждения ДНК, она может уничтожить саму себя, как доблестный самурай. Это очень важный механизм, так как чрезмерное накопление ошибок в генах может привести к тому, что клетка станет раковой, начнет неограниченно делиться, а ее потомки образуют зачаток опухоли. Клетки в такой опухоли начнут эволюционировать: новые мутации, способствующие более быстрому делению, будут закрепляться, и в итоге маленькая опухоль может перерасти в тяжелый случай агрессивного и метастазирующего рака.
Когда-то одна такая клетка из раковой опухоли шейки матки пациентки по имени Генриетта Лакс (Henrietta Lacks) положила начало клеточной линии, которая называется HeLa. Эти клетки живут в лабораториях и используются для исследований. Они очень быстро делятся и не стареют, поэтому их называют бессмертными. С момента своего появления клетки HeLa успели заметно измениться, и теперь их хромосомный набор заметно отличается от человеческого. В связи с этим американский биолог Ли Ван Вален даже предложил выделить эти клетки в отдельный вид одноклеточных организмов, произошедших из многоклеточного – человека.
Более очевидный пример такого видообразования – появление раковых клеток, вызывающих лицевую опухоль тасманийского дьявола. Эта опухоль передается от одной особи к другой через укусы105. Получается, раковая клетка настолько изменилась, что стала полноценным, независимым и опасным паразитом, перескакивающим с организма на организм. Аналогичный пример – трансмиссивная венерическая саркома собаки. Геном этих опухолевых клеток похож на геномы собачьих, но теперь это отдельный организм, размножающийся бесполым путем и передающийся от собаки к собаке через половой контакт106. Чем не замечательные, хоть и ужасные примеры появления новых видов в процессе эволюции?
Мутации в природе могут возникать по ряду внешних причин, напрямую не связанных с копированием молекулы ДНК. Так, ультрафиолетовое излучение (УФ) может повреждать ДНК. Такое повреждение чаще всего выражается в появлении тиминовых димеров – когда два соседних нуклеотида T сшиваются вместе. Это тоже приводит к деформации молекулы ДНК, что привлекает компоненты системы репарации. Есть ферменты, которые умеют химически исправлять такие димеры, однако в ряде случаев клеткам приходится прибегать к более универсальным методам исправления ошибок – вырезать дефектные и близлежащие к ним нуклеотиды поврежденной цепочки ДНК. Благодаря наличию второй (комплементарной) цепи ДНК у клетки есть возможность восстановить двойную спираль, но успешно исправляются далеко не все повреждения.
Пигмент меланин, придающий темный цвет коже, помогает организму защититься от вредного воздействия УФ. Поэтому среди жителей экваториальных стран преобладает темная кожа, а защитной реакцией на избыток солнечного света является загар – усиленная выработка меланина. Это очень важный защитный механизм, ведь ошибки в ДНК, вызванные УФ, могут приводить к меланоме – злокачественной раковой опухоли кожи. Учитывайте последнее, решая, стоит ли много загорать во время поездки на море или проявить умеренность.
Другой существенный источник повреждения ДНК – ионизирующее излучение. Оно может возникать в результате радиоактивного распада некоторых элементов, а также достигать наших клеток из космоса. Некоторые химические вещества, называемые мутагенами, тоже могут способствовать накоплению ошибок в ДНК. Вещества с подобным эффектом существуют, например, в табачном дыме: у курящих существенно увеличен риск рака легких. Это не значит, что все любители затянуться заболеют раком легких, но шанс получить его в течение жизни у них примерно в 10 раз выше, чем у некурящих (примерно 17 % против 1 % у мужчин и 12 % против 1 % у женщин107). Любопытно, что далеко не все противники ГМО спешат запрещать курение, вред которого доказан, а некоторые даже курят. Возможно, их утешает тот факт, что табак натурален?




